
集合管癌(Collecting duct carcinoma ,CDC)和肾髓质癌(Renal medullary carcinoma,RMC)是肾癌的两种罕见的侵袭性亚型,它们在远端肾单位具有相似的解剖起源。由于其稀有性,关于其流行病学和结果的数据有限[1]。
集合管癌(Collecting duct carcinoma ,CDC)
CDC占肾脏恶性肿瘤的1%以下,主要病理组织学特征包括多位于肾髓质、浸润性肾小管或肾小管上皮样改变、显著的核和有丝分裂异型性以及间质反应。淋巴结阴性且无转移的患者可以从手术中获益,而对于已有淋巴结受累或远处转移的患者,不建议进行手术,因其生存期<1年且围手术期死亡率较高。化疗可作为晚期患者的标准治疗和淋巴结受累患者的术后辅助治疗。转移性CDC中的靶向治疗目前发表了一些令人鼓舞的案例报告,其中包括VEGF受体抑制剂(舒尼替尼或索拉非尼)、mTOR抑制剂(替西罗莫司)、HER2/neu受体抑制剂(曲妥珠单抗)等。在吉西他滨与铂类联合化疗中加用贝伐单抗对单个转移灶的CDC患者有良好疗效。总之,目前铂类化疗是临床上疗效最好的转移性CDC治疗方法[2]。
肾髓质癌(Renal medullary carcinoma,RMC)
与CDC相比,RMC与镰状细胞特性密切相关,并与独特的分子变化相关,虽是罕见的肾癌亚型,但它恶性生物学行为较高,大多数患者在就诊时即发现转移。RMC肿瘤的特点是肾髓质的肿物,边界不清,通常表现为不同程度的出血和坏死。镜下可见典型的网状或筛网状结构,伴有明显的间质纤维化和混合性炎症浸润[3]。对于一般情况良好、转移负荷低或对全身治疗有反应的患者,应考虑先行根治性肾切除术[4]。抗血管生成治疗在RMC治疗中的作用是一个很有前途的研究领域,一些研究表明贝伐单抗,特别是联合化疗使用,可以延长生存期。PD1/PD-L1抑制剂的作用仍存在争议。另一个正在进行的研究领域是Zeste同源物增强子(EZH2),临床前数据显示,EZH2抑制导致SMARCB1表达缺失的细胞株凋亡和分化,并可能在RMC治疗中发挥作用[3]。RMC现在有一些新药物的试验,应该鼓励让病人参加临床研究。
2020 ESMO 数据
2020年ESMO上,Jeffrey Graham等发表摘要,使用SEER(surveillance, Epidemiology, and End Results)数据库对2004-2015年间诊断的CDC和RMC病例进行了回顾性分析,描述了这些肿瘤的流行病学特征及预后因素[1]。
该研究报道了273例CDC和74例RMC。RMC患者年龄更小(平均年龄27.4岁vs 59.1岁,p<0.001),其中非裔美国人更多(81.1%比23.1%,p<0.001)。与CDC相比,RMC在诊断时疾病进展更晚,约74.8%为IV期肿瘤,而CDC患者中IV期为48.4%(p<0.001)。RMC更有可能发生区域淋巴结转移(60.8% vs.38.1%,p<0.001)和远处转移(75.7% vs. 38.3%,p<0.01)。CDC组接受手术治疗者较多(83.8%vs. 65.8%,p<0.001)。RMC患者中化疗更为常见(67.6% vs. 28.9%,p<0.001)。CDC的中位生存期(OS)为19个月,而RMC为9个月。在对年龄、性别、种族和分期进行分析后,与CDC相比,RMC的生存率显著降低(HR 1.70,95%CI 1.09-2.66,p=0.02)。图1显示了CDC和RMC二者全因死亡、癌症特异性死亡、早期疾病的全因死亡以及IV期疾病全因死亡的比较。表1显示了中位生存情况[1]。
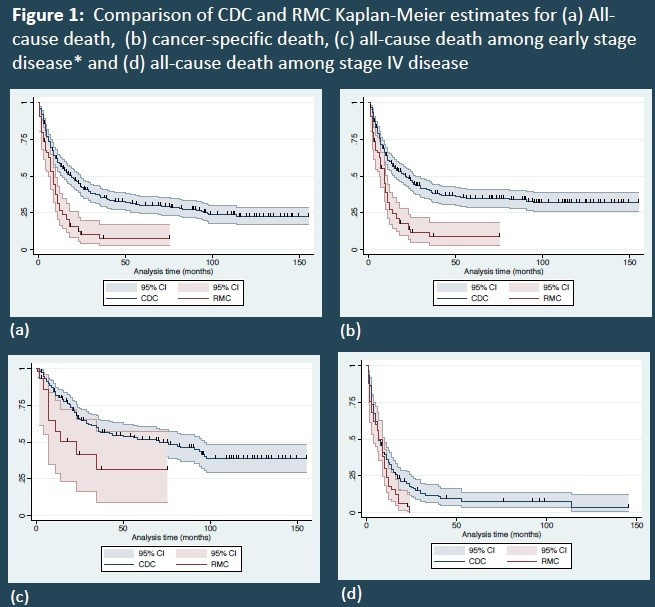
图1
CDC和RMC二者全因死亡、癌症特异性死亡、早期疾病的全因死亡以及IV期疾病全因死亡的生存分析对比
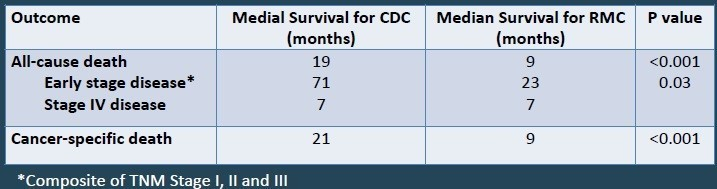
表1
中位生存期[1]
总结
结果与其他流行病学研究的数据一致[5]。尽管最近在其他肾癌亚型的治疗上取得了进展,但CDC和RMC的预后仍然很差。与CDC相比,RMC的预后不良,中位生存期小于1年。然而,对抗血管生成治疗、PD-1和EZH2抑制剂的进一步研究可能会有新的成果[3]。未来的研究应该集中在高危患者的早期发现、前瞻性临床试验以及在晚期患者中开发新的治疗策略。
参考文献:
1. Graham et al. Collecting duct and renal medullary carcinoma: A population based analysis. Abstract 726P, ESMO 2020.
2. N Pécuchet et al. Triple combination of bevacizumab, gemcitabine and platinum salt in metastatic collecting duct carcinoma. Ann Oncol. 2013 Dec;24(12):2963-7.
3. Elliott et al. Renal Medullary Carcinoma. Arch Pathol Lab Med. 2019 Dec;143(12):1556-1561.
4. Beckermann et al. Renal Medullary Carcinoma: Establishing Standards in Practice. JOP. 2017.
5. Abern et al. Characteristics and outcomes of tumors arising from the distal nephron. Urology. 2012.
致谢
感谢辉瑞医学部肿瘤一组王莹博士和医学信息部在文章撰写过程中提供材料和文献的帮助。
相关阅读
原创作者 管维
华中科技大学同济医学院附属同济医院 泌尿外科
主任医师
主要任职 :
欧洲泌尿外科学会(EAU)会员;中华医学会泌尿外科学分会机器人学组委员;中华医学会泌尿外科分会青年委员会肿瘤学组副组长;湖北省医学会泌尿外科分会肿瘤学组委员
专业方向 :
泌尿系统肿瘤的综合诊治,擅长腹腔镜及机器人辅助腹腔镜手术
本文原创作者为管维医师,已获得作者授权发布。
备注
其中未在中国大陆获批的治疗方法,请以CFDA批准适应症为准。本内容仅供医疗卫生专业人士学习使用,不构成实际治疗建议。
相关阅读
【RCC前沿·新时空】关注罕见类型肾癌-来自2020ESMO的一点提示
【RCC前沿·新时空】新型雷达的应用:循环肿瘤细胞在肾癌进展预测中的作用
【RCC前沿·新时空】见微知治——循环肿瘤细胞在肾癌疗效评价中的应用
【RCC前沿·新时空】循环肿瘤细胞指导的肾癌M0(i+)分期研究


