
简要介绍
肾癌
1. Ann Oncol(IF: 65.4):卡博替尼联合纳武利尤单抗和伊匹木单抗用于既往未接受治疗的晚期肾细胞癌:III期COSMIC-313研究的最终结果和生物标志物分析
前列腺癌
2. N Engl J Med(IF: 78.5):恩扎卢胺改善生化复发性前列腺癌患者的生存率
3. Lancet Oncol(IF: 35.9):转移导向治疗联合标准治疗与单纯标准治疗用于寡转移性前列腺癌的对比(WOLVERINE):来自X-MET协作组的系统综述和个体患者数据荟萃分析
4. Lancet Oncol(IF: 35.9):基于列线图的风险分类用于预测PSMA PET分期寡复发性前列腺癌患者对转移灶立体定向体部放疗的反应(PORTAL):一项国际回顾性队列研究
5. JAMA Oncol(IF: 20.1):挽救性局部治疗与根治性前列腺切除术治疗局限性放射性复发性前列腺癌的对比
6. JAMA Oncol(IF: 20.1):钠-葡萄糖共转运蛋白2抑制剂用于接受激素治疗的前列腺癌患者
7. Eur Urol(IF: 25.2):BRCA1或BRCA2致病性种系变异携带者的针对性前列腺癌筛查可检测出临床相关疾病:IMPACT研究的5年结果
膀胱癌
8. Eur Urol(IF: 25.2):肌层浸润性膀胱癌的优化管理:国际膀胱癌协作组的建议
肾癌
1. 卡博替尼联合纳武利尤单抗和伊匹木单抗用于既往未接受治疗的晚期肾细胞癌:III期COSMIC-313研究的最终结果和生物标志物分析
发表期刊:Ann Oncol
背景:COSMIC-313初步结果显示,在晚期肾细胞癌(RCC)患者中,一线卡博替尼联合纳武利尤单抗和伊匹木单抗较安慰剂联合纳武利尤单抗和伊匹木单抗显著延长无进展生存期。本文报告最终疗效和安全性结果以及探索性生物标志物分析数据。
患者与方法:这项Ⅲ期、双盲、1:1随机对照研究,在既往未接受过治疗的晚期透明细胞肾细胞癌成人患者中比较卡博替尼或安慰剂联合纳武利尤单抗和伊匹木单抗,其研究设计、受试者及主要终点PFS结果既往已报道。次要终点为意向治疗人群的总生存期(OS)。探索性生物标志物分析探讨免疫细胞类型及基因特征与临床结局的潜在关联。
结果:中位随访45.0个月后,卡博替尼三联治疗组更新的中位PFS长于安慰剂双联治疗组(16.6个月vs11.2个月;风险比[HR]0.82,95%置信区[CI]0.69-0.98)(图1)。中位OS无显著差异(HR 1.02,95%CI 0.85-1.23,P=0.84)(图2),安全性特征与既往分析一致(三联组和双联组分别有75%和43%的患者发生 3/4级治疗相关不良事件)(表1)。在M2型巨噬细胞水平较高的患者中,三联方案较双联方案显著改善PFS(图3)和OS(图4)。三联治疗组应答者表现为血管生成特征上调、免疫相关通路下调,而双联治疗组应答者则呈现强烈的免疫活化(图5和图6)。
结论:COSMIC-313长期结果继续证实,在纳武利尤单抗联合伊匹木单抗基础上加用卡博替尼可带来PFS获益,但未观察到OS获益,亦未出现新的安全性信号。探索性生物标志物分析提示,在M2型巨噬细胞高表达患者中,卡博替尼联合纳武利尤单抗和伊匹木单抗可改善生存。
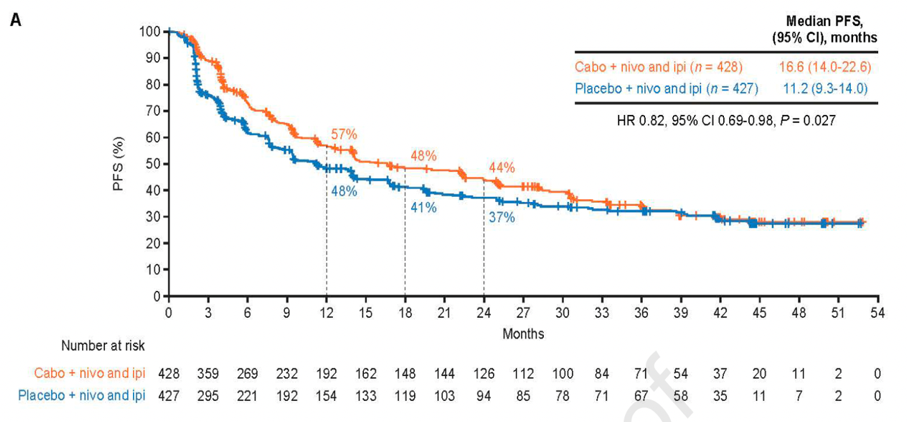
图1. 中位随访45.0个月后,卡博替尼三联治疗组与安慰剂双联治疗组的PFS比较
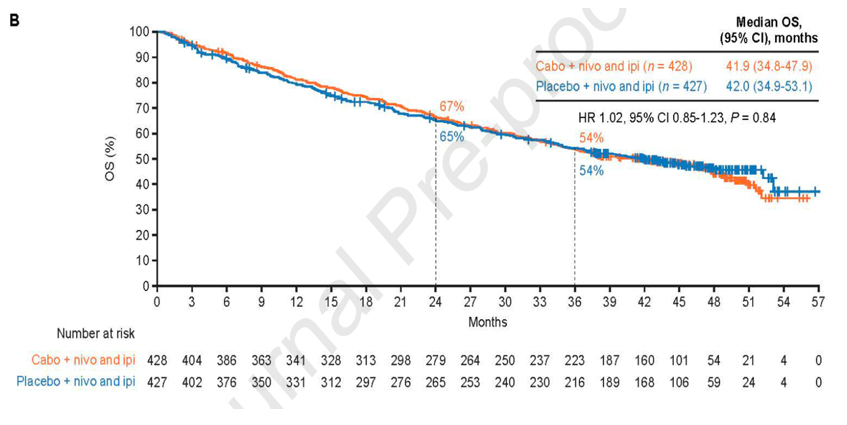
图2. 中位随访45.0个月后,卡博替尼三联治疗组与安慰剂双联治疗组的OS比较
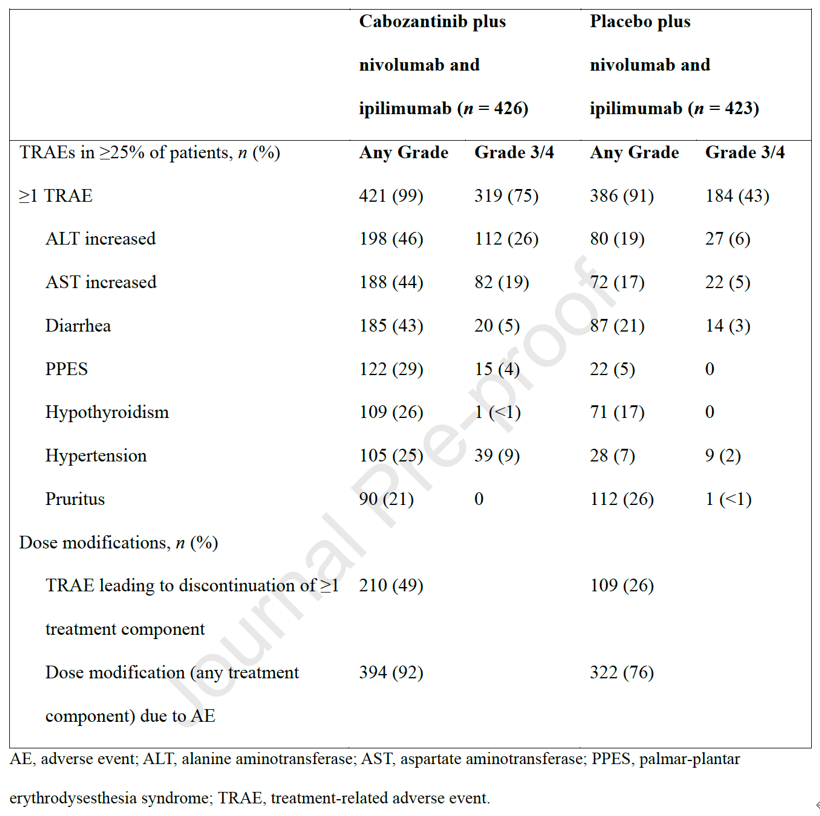
表1. 安全性人群的不良事件总结和剂量调整表
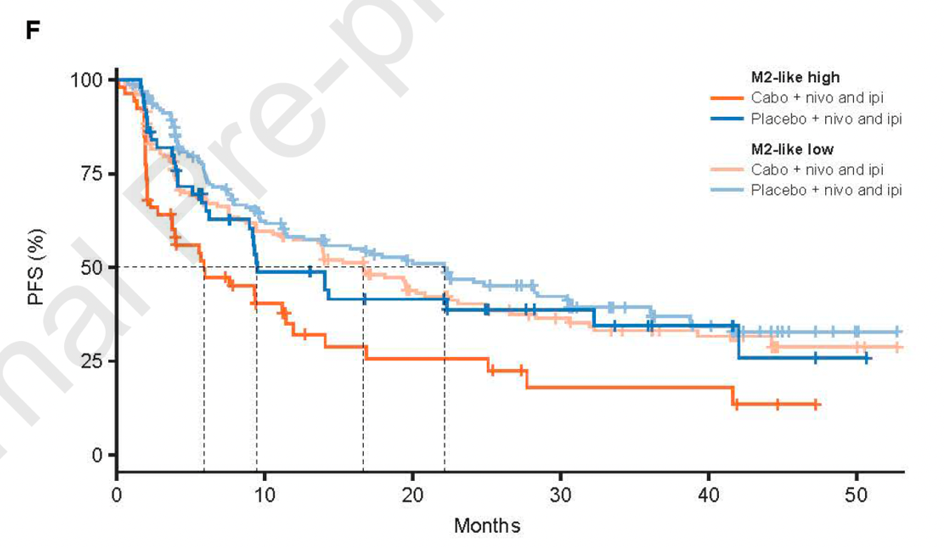
图3. 在M2型巨噬细胞水平较高的患者中,三联方案和双联方案的PFS比较
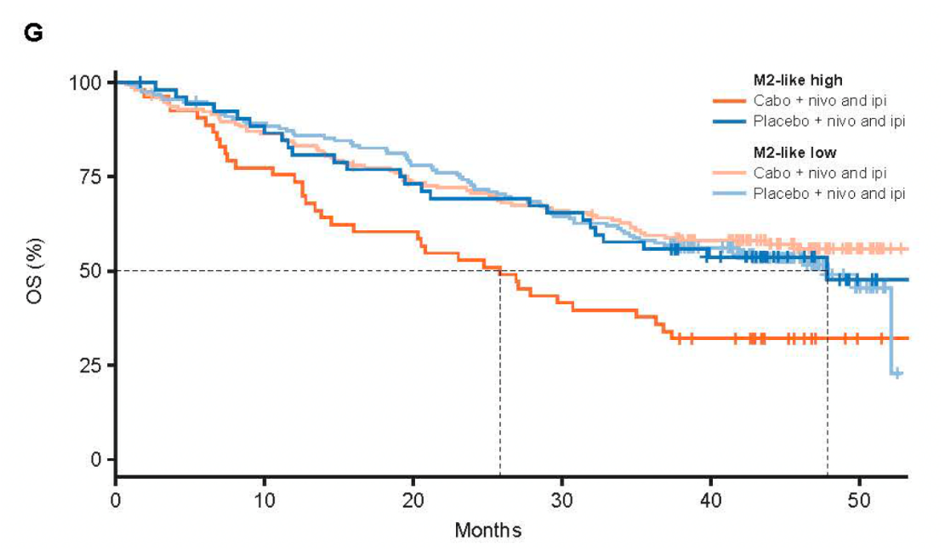
图4. 在M2型巨噬细胞水平较高的患者中,三联方案和双联方案的OS比较
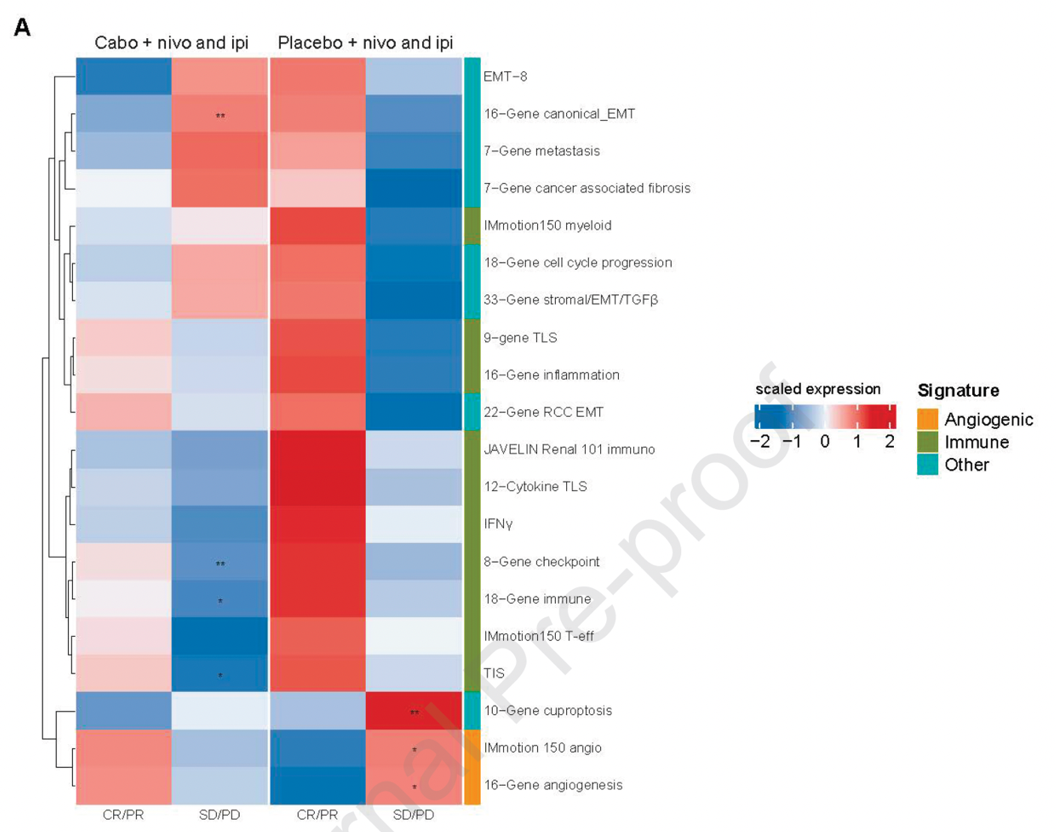
图5. 三联和双联治疗组应答者已发表基因特征的表达热图
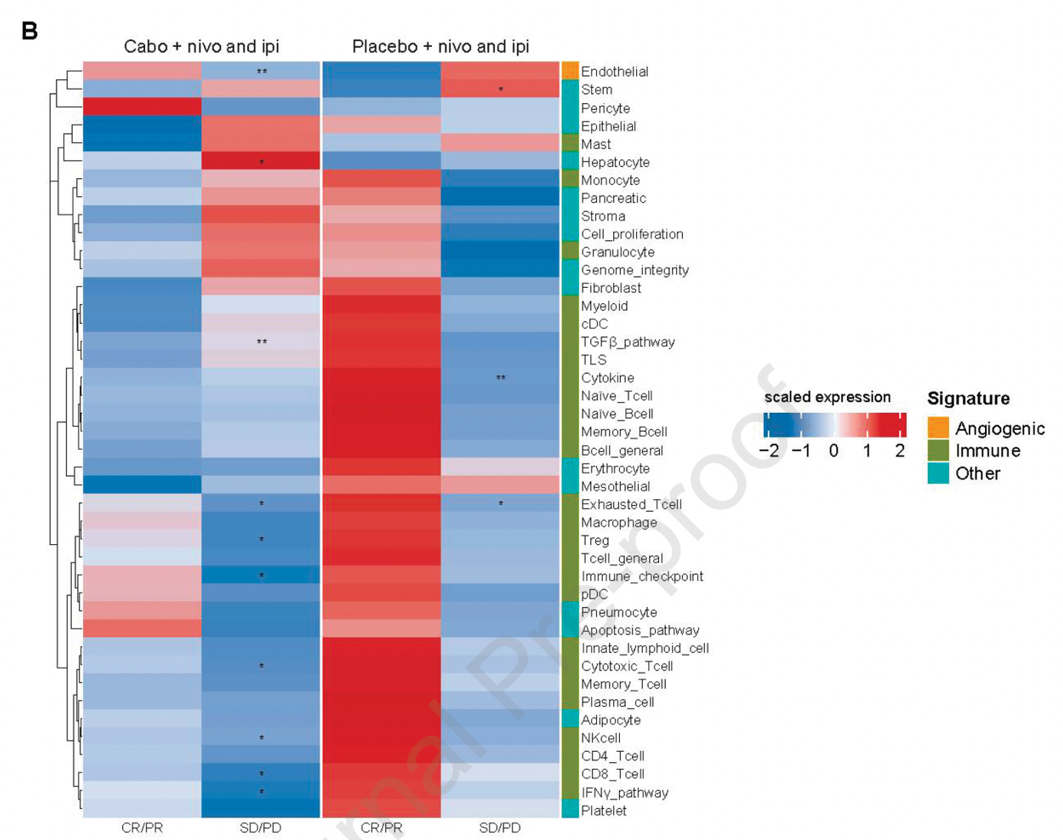
图6. 三联和双联治疗组应答者肿瘤免疫微环境的表达热图
前列腺癌
2. 恩扎卢胺改善生化复发性前列腺癌患者的生存率
发表期刊:N Engl J Med
背景:在Ⅲ期EMBARK试验中,对于生化复发前列腺癌患者,恩扎卢胺联合亮丙瑞林以及恩扎卢胺单药治疗的无转移生存期均长于亮丙瑞林单药治疗。总生存期的最终分析尚未报道。
方法:我们将高危生化复发的前列腺癌患者按1:1:1比例随机分配,接受恩扎卢胺联合亮丙瑞林(联合组)、亮丙瑞林单药(亮丙瑞林单药组)或恩扎卢胺单药治疗(单药组)。主要终点为无转移生存期,对比联合组与亮丙瑞林单药组。总生存期为α控制的关键次要终点。对预设次要终点的更新结果进行描述性总结,包括首次使用新抗肿瘤治疗的时间、首次症状性骨骼事件的时间,以及探索性终点即首次后续治疗的无进展生存期。
结果:联合组8年总生存率为78.9%(95%CI 73.9~83.1),亮丙瑞林单药组为69.5%(95%CI 64.0~74.3);死亡风险比为0.60(95%CI 0.44~0.80;P<0.001)(图7)。恩扎卢胺单药组8年总生存率为73.1%(95%CI 67.6~77.9),与亮丙瑞林单药组无显著差异(风险比0.83;95%CI 0.63~1.10;P=0.19)(图8)。预设次要终点的描述性更新结果与既往报道一致。安全性结果与无转移生存期主要分析一致。
结论:在高危生化复发前列腺癌患者中,恩扎卢胺联合亮丙瑞林治疗的总生存期显著长于亮丙瑞林单药治疗。总生存期分析显示,恩扎卢胺单药治疗并不优于亮丙瑞林单药治疗。
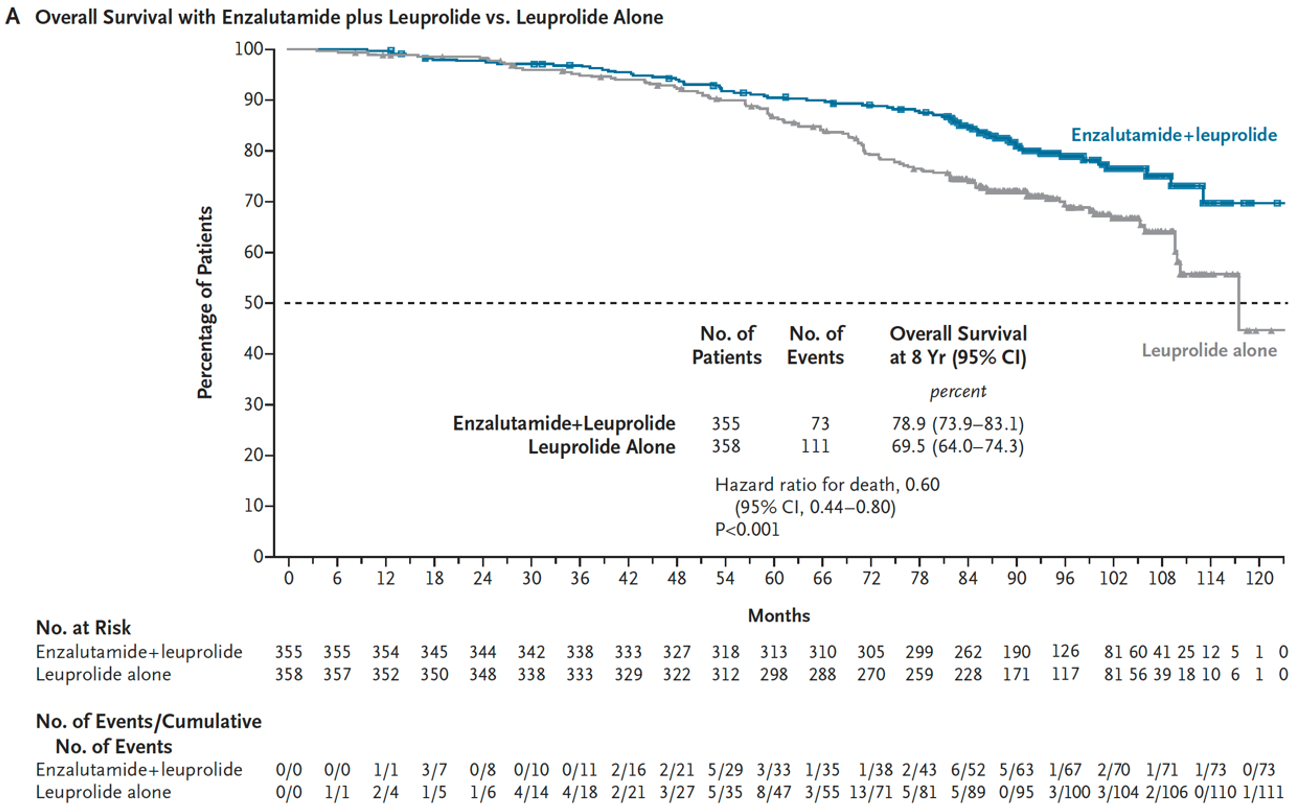
图7. 恩扎卢胺联合亮丙瑞林对比亮丙瑞林单药的总生存期
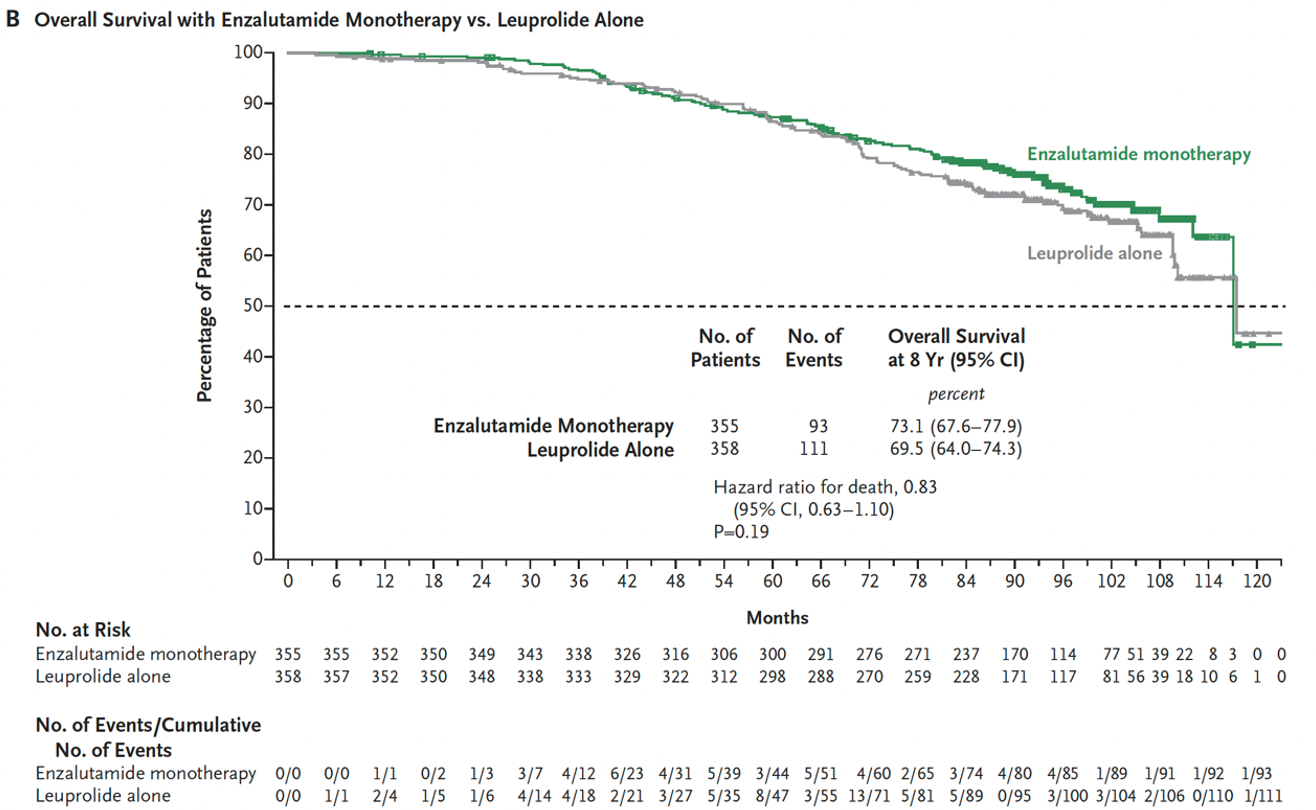
图8. 恩扎卢胺单药治疗对比亮丙瑞林单药治疗的总生存期
3. 转移导向治疗联合标准治疗与单纯标准治疗用于寡转移性前列腺癌的对比(WOLVERINE):来自X-MET协作组的系统综述和个体患者数据荟萃分析
发表期刊:Lancet Oncol
背景:寡转移疾病位于转移谱的近端。尽管缺乏1级证据,转移灶导向治疗(MDT)仍越来越多地用于寡转移疾病的治疗。本研究汇总多项试验的个体患者数据,评估转移导向治疗用于寡转移前列腺癌的疗效。
方法:本研究为系统评价与个体患者数据荟萃分析。系统检索Embase、PubMed、CENTRAL、MEDLINE及ClinicalTrials.gov,筛选纳入寡转移前列腺癌患者接受转移灶导向治疗的随机对照试验。纳入标准为:已发表的前瞻性随机试验,纳入寡转移前列腺癌患者(转移灶≤5个),且研究者记录了可用于评估无进展生存期和总生存期的足够数据。本次系统评价检索时间为建库至2023年11月3日,并于2025年5月4日更新。采用Covidence进行数据评价,由两名研究者(CT和ADS)独立筛选。使用Cochrane协作网偏倚风险评估工具(2.0版)评价研究质量。由研究者提供个体患者数据。共同主要终点为无进展生存期和总生存期。次要终点为影像学无进展生存期和无去势抵抗生存期。主要分析在“转移导向治疗+标准治疗(SOC)对比标准治疗”的随机研究亚组中进行。主要分析包括采用随机效应模型的试验层面分析,以及按试验分层的患者层面分析。本荟萃分析已在PROSPERO注册(CRD42023479078)。
结果:共筛选2975项研究,最终纳入7项Ⅱ期研究,包含574例男性患者。其中6项试验(472例患者)被用于评估转移导向治疗,患者随机分配至转移导向治疗+标准治疗组(n=248)或标准治疗组(n=224),中位随访时间40.7个月(IQR25.6~53.7)。转移导向治疗可改善无进展生存期(试验层面HR 0.44,95% CI 0.35~0.56,p<0.0001(图9a);患者层面HR 0.45,95% CI 0.35~0.57,p<0.0001(图9b))、影像学无进展生存期(试验层面HR 0.60,95% CI 0.42~0.85,p=0.0039(图10a);患者层面HR 0.59,95% CI 0.46~0.76,p<0.0001(图10b))以及无去势抵抗生存期(试验层面HR 0.58,95% CI 0.37~0.92,p=0.019(图11a);患者层面HR 0.58,95% CI 0.37~0.91,p=0.017(图11b))。转移导向治疗与总生存期的相关性:试验层面分析HR 0.63(95% CI 0.39~1.00,p=0.051)(图12a),患者层面分析HR 0.64(95% CI 0.40~1.01,p=0.057)(图12b)。
结论:本研究显示,转移导向治疗可改善寡转移前列腺癌患者的无进展生存期、影像学无进展生存期及无去势抵抗生存期。总生存期获益未达到统计学显著性,仍需进一步研究。
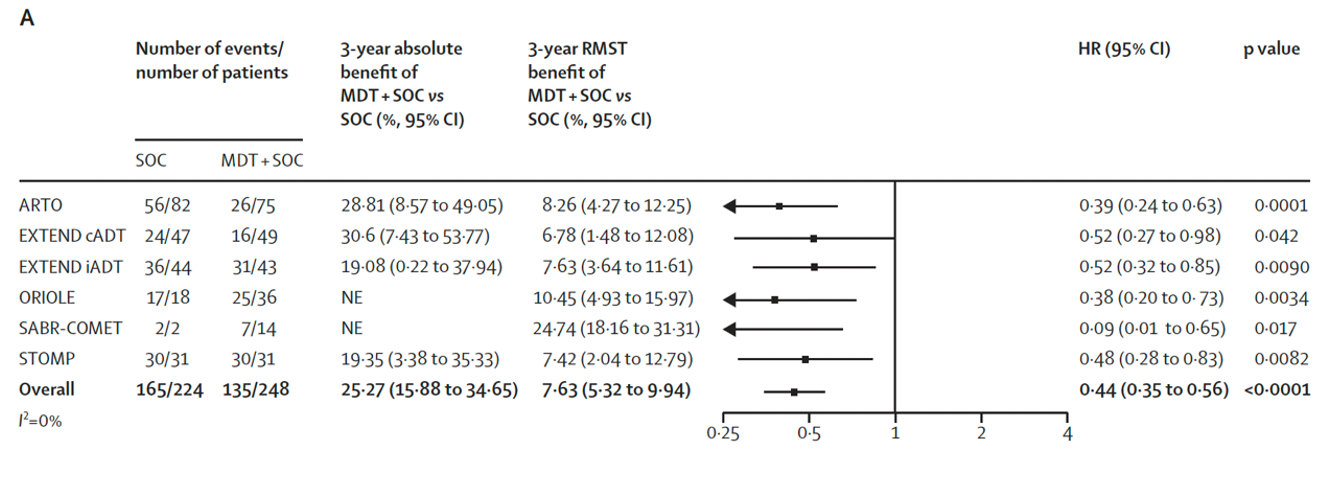
图9(a). 关于无进展生存期的转移导向治疗联合标准治疗对比单纯标准治疗相关性的试验层面荟萃分析
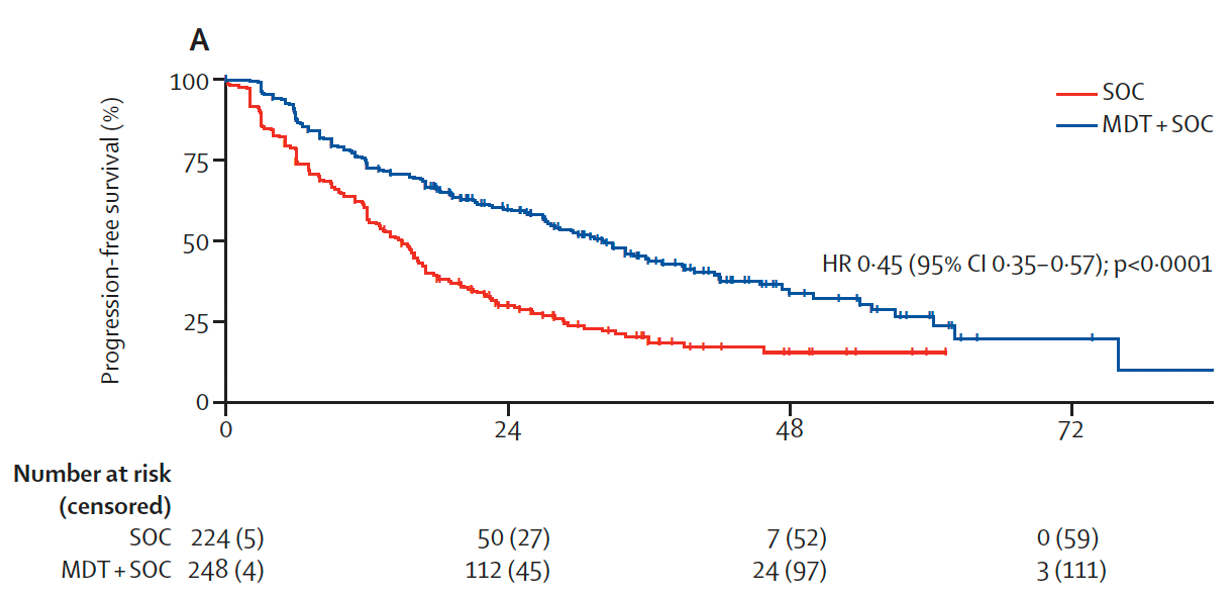
图9(b). 关于无进展生存期的转移导向治疗联合标准治疗对比单纯标准治疗相关性的患者层面分析Kaplan-Meier生存曲线
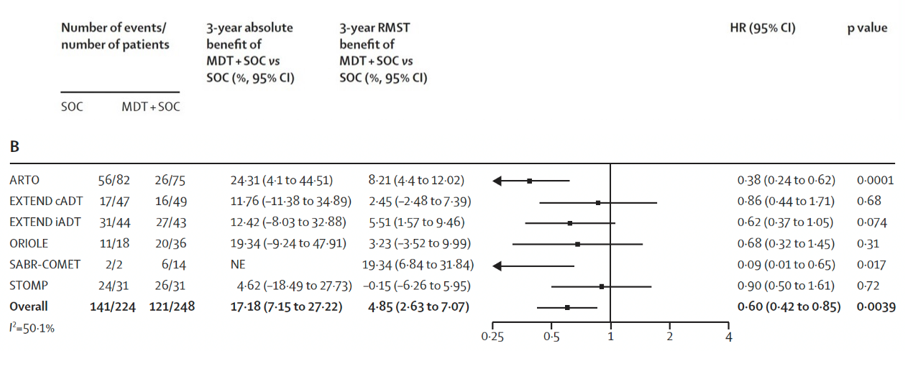
图10(a). 关于影像学无进展生存期的转移导向治疗联合标准治疗对比单纯标准治疗相关性的试验层面荟萃分析
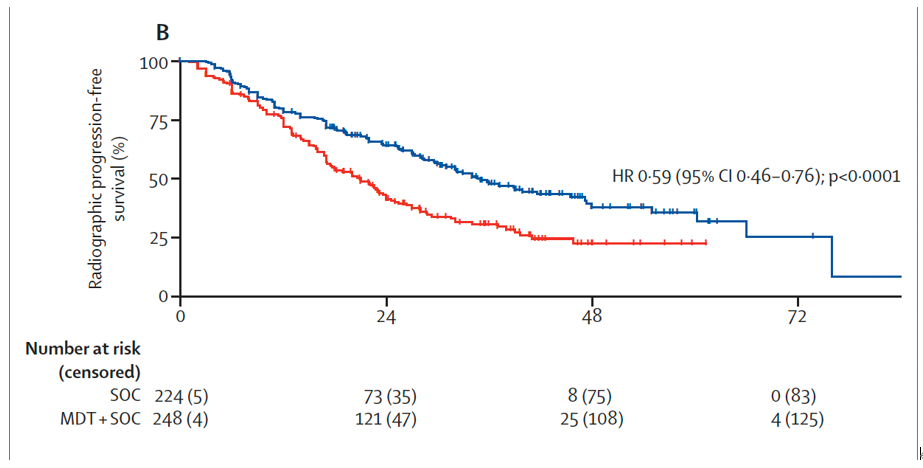
图10(b). 关于影像学无进展生存期的转移导向治疗联合标准治疗对比单纯标准治疗相关性的患者层面分析Kaplan-Meier生存曲线
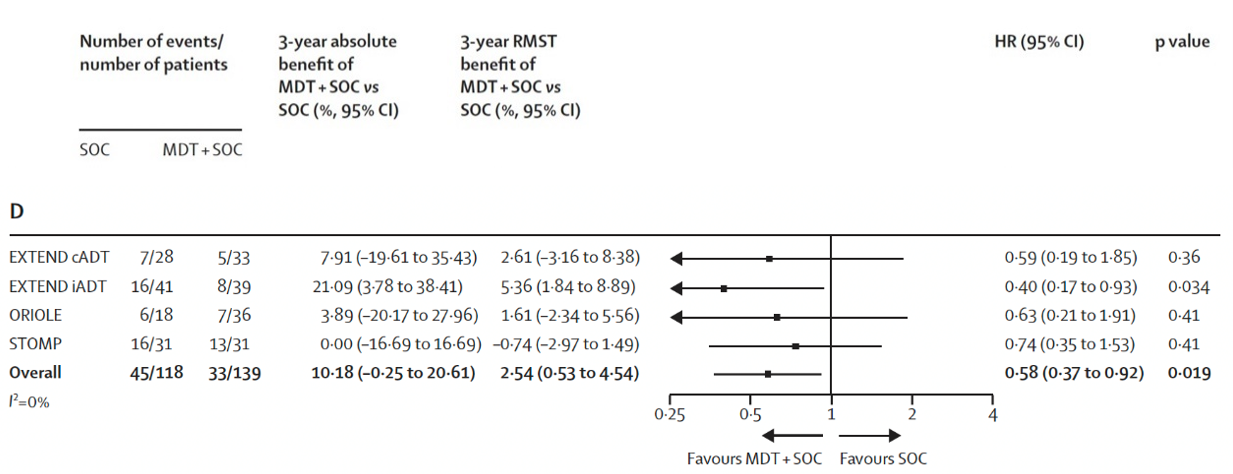
图11(a). 关于无去势抵抗生存期的转移导向治疗联合标准治疗对比单纯标准治疗相关性的试验层面荟萃分析
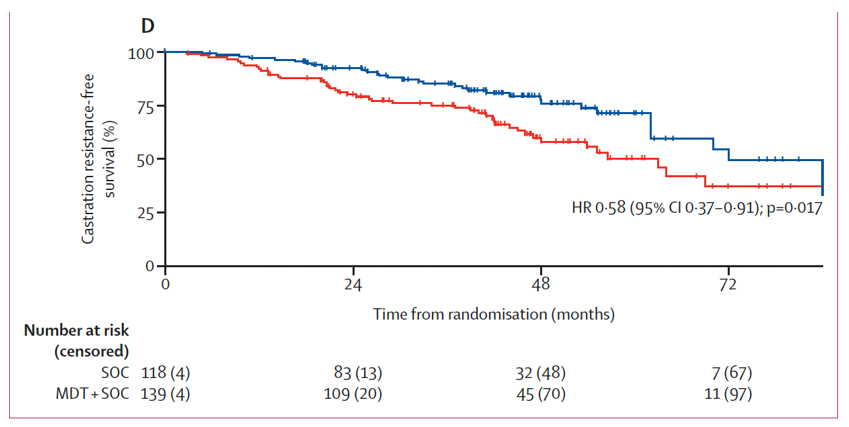
图11(b). 关于无去势抵抗生存期的转移导向治疗联合标准治疗对比单纯标准治疗相关性的患者层面分析Kaplan-Meier生存曲线
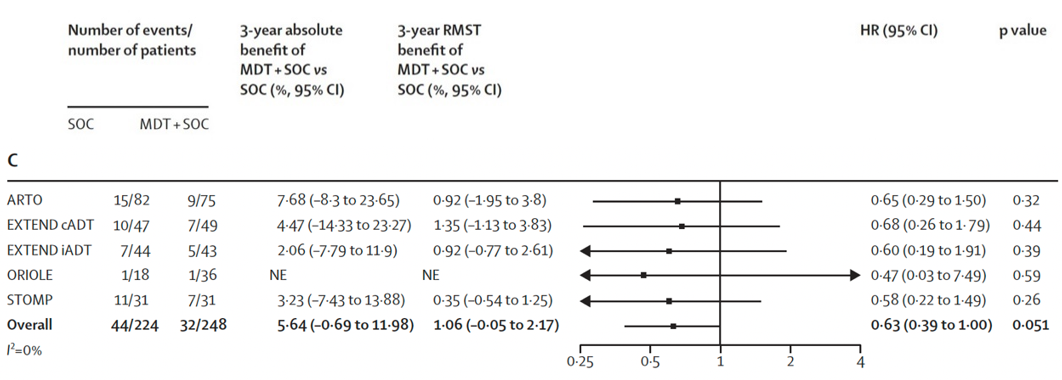
图12(a). 关于总生存期的转移导向治疗联合标准治疗对比单纯标准治疗相关性的试验层面荟萃分析
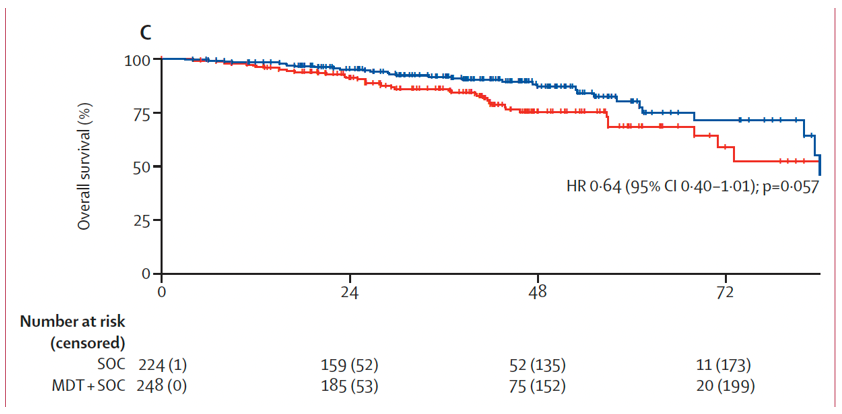
图12(b). 关于总生存期的转移导向治疗联合标准治疗对比单纯标准治疗相关性的患者层面分析Kaplan-Meier生存曲线
4. 基于列线图的风险分类用于预测PSMA PET分期寡复发性前列腺癌患者对转移灶立体定向体部放疗的反应(PORTAL):一项国际回顾性队列研究
发表期刊:Lancet Oncol
背景:转移导向治疗(MDT)可延迟寡复发性前列腺癌患者的雄激素剥夺治疗(ADT),但治疗结局存在差异,且缺乏风险分层工具。本研究旨在开发并验证一种列线图,用于预测无雄激素剥夺治疗生存期。
方法:本研究为一项国际回顾性队列研究,纳入欧洲(奥地利、意大利、拉脱维亚、荷兰、波兰和葡萄牙)10家医院及学术机构中18岁及以上、经组织学证实为前列腺癌(所有亚型)、既往接受过根治性局部治疗、发生异时性寡复发且激素敏感性疾病(前列腺特异性膜抗原[PSMA]PET检测发现≤5个盆腔淋巴结转移和/或远处转移)、接受所有病灶立体定向体部放疗且未接受辅助全身治疗的男性患者。主要终点为随访1年时仍无ADT治疗的患者比例。采用多变量Cox模型结合向后逐步剔除方法评估10项临床预测因素。通过自举法进行内部验证,评估模型性能(C指数和校准度),随后进行外部验证。
结果:共筛选2014年7月1日至2023年12月31日期间接受治疗的1461例男性患者,其中586例纳入开发队列(307例[52%]为盆腔淋巴结转移,279例[48%]为远处转移);中位随访时间为37个月(IQR24-58)。外部验证队列(以下简称验证队列)包含131例患者(57例[44%]为盆腔淋巴结转移,74例[56%]为远处转移),中位随访时间为43个月(24-57)。开发队列1年无ADT生存期为84.3%(95% CI 81.4-87.3)(图13a),验证队列为92.8%(88.4-97.4)(图13b)。ADT早期启动的独立预测因素包括:MDT前PSA水平较高(HR 1.05,95% CI 1.03-1.08)、PSA倍增时间较短(HR 0.97,95% CI 0.95-0.98)、3-5个病灶(HR 1.74,95% CI 1.33-2.28)以及远处转移(HR 1.45,95% CI 1.18-1.78)(表2)。开发队列的模型区分度为0.66(95% CI 0.65-0.68),外部验证队列为0.65(95% CI 0.55-0.75)。风险分层将患者分为低危、中危和高危三个预后组(p<0.0001)。
结论:该列线图可预测寡复发性前列腺癌患者接受MDT后的无ADT生存期。尽管个体水平的区分度中等,但风险组分层显示出有意义的区分能力,支持其在治疗选择中的潜在应用价值。
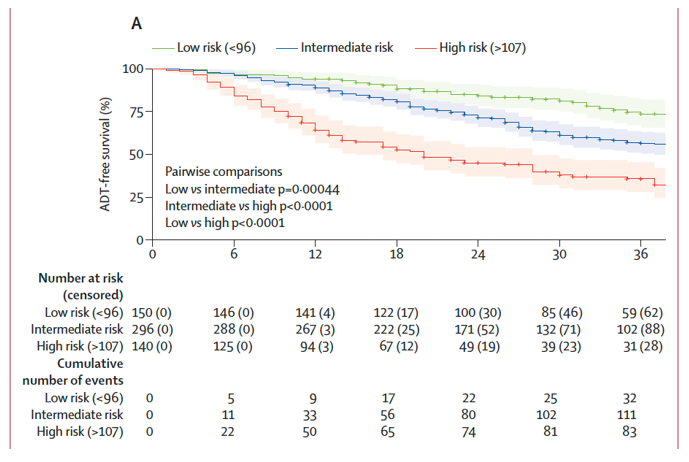
图13(a). 开发队列不同风险组的事后无雄激素剥夺治疗生存期曲线
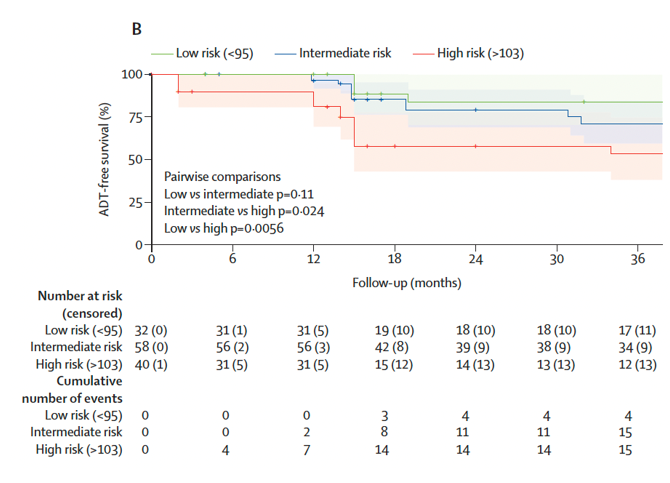
图13(b).外部验证队列中不同风险组的事后无雄激素剥夺治疗生存期曲线
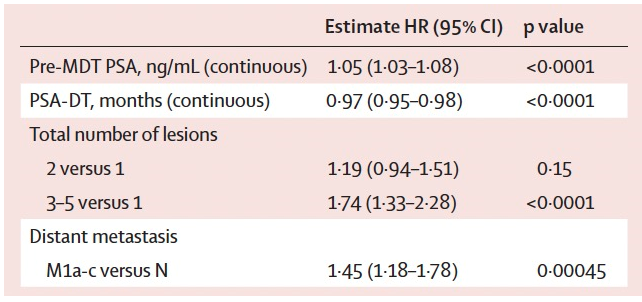
表2:基于填补数据集经内部验证后的多变量Cox回归分析结果
5. 挽救性局部治疗与挽救性根治性前列腺切除术治疗局限性放射性复发性前列腺癌的对比
发表期刊:JAMA Oncol
研究意义:既往接受放疗的复发性前列腺癌患者通常生存期较差。前列腺局限性复发患者可能适合挽救性局部治疗(sFT)或挽救性根治性前列腺切除术(sRP)。挽救性局部治疗(sFT)可提供良好的肿瘤控制,且毒性相对较低,但5年以上的结局尚未见报道,且目前尚无研究对比sFT与sRP的疗效。
研究目的:对比挽救性局部治疗(sFT)与挽救性根治性前列腺切除术(sRP)患者的肿瘤控制效果及围手术期并发症。
研究设计、研究地点及研究对象:本研究为一项国际多中心队列研究,采用匹配对照数据。接受sFT的患者来自前瞻性英国高强度聚焦超声(HIFU)评估与治疗注册研究、国际冷冻治疗评估注册研究(9个中心;2006-2024年)以及前瞻性英国局部复发评估与挽救治疗队列研究(6个中心;2014-2018年)。接受sRP的患者来自国际回顾性注册研究(8个国家的12个中心;2000-2021年)。纳入经活检证实、放疗后局限性复发前列腺癌患者(包括外照射放疗、近距离放疗或两者联合治疗后复发)。数据分析时间为2025年3月至7月。
暴露因素:采用高强度聚焦超声(HIFU)或冷冻治疗的挽救性局部治疗(sFT)与挽救性根治性前列腺切除术(sRP)。
主要结局指标:主要结局为最长10年的癌症特异性生存期。次要结局为总生存期、任何围手术期并发症(Clavien-Dindo分级1-5级)以及主要围手术期并发症(Clavien-Dindo分级3-5级)。在个体多重插补数据集中,采用1:1基数匹配对患者进行对比分析。匹配变量包括放射治疗方式、初始治疗与挽救治疗的间隔年限、欧洲泌尿外科协会复发风险组,以及挽救治疗前的年龄、前列腺特异性抗原(PSA)水平、前列腺体积、分级组、T分期和雄激素剥夺治疗(ADT)使用情况。
结果:共923例患者符合匹配条件(419例接受sFT,504例接受sRP)。接受sFT的患者中,325例(77.6%)采用HIFU治疗,其余采用冷冻治疗,其中241例(57.5%)接受象限消融治疗。接受sRP的患者中,376例(74.6%)采用开放手术,其余采用机器人辅助手术。sFT组与sRP组的10年癌症特异性生存期分别为92%(95%CI 86%-98%)和99%(95%CI 97%-100%),差异无统计学意义(限制平均时间损失为-0.09年;95%CI -0.22至0.03年;P=0.15;亚分布风险比为0.45;95%CI 0.05-4.00;P=0.47)(图14)。两组10年总生存期差异无统计学意义(限制平均生存期为 -0.13年;95%CI -0.86至0.60年;P=0.72)(图15)。接受sRP与任何并发症(调整后比值比24.20;95%CI 12.94-45.27;P<0.001)和主要并发症(调整后比值比9.31;95%CI 3.42-25.36;P<0.001)的发生风险显著升高相关。
结论与意义:本队列研究表明,sFT和sRP治疗局限性放疗后复发性前列腺癌均有效,而sFT的围手术期并发症更少。对于许多局限性放疗后复发性前列腺癌患者,sFT可能提供更有利的治疗获益比。
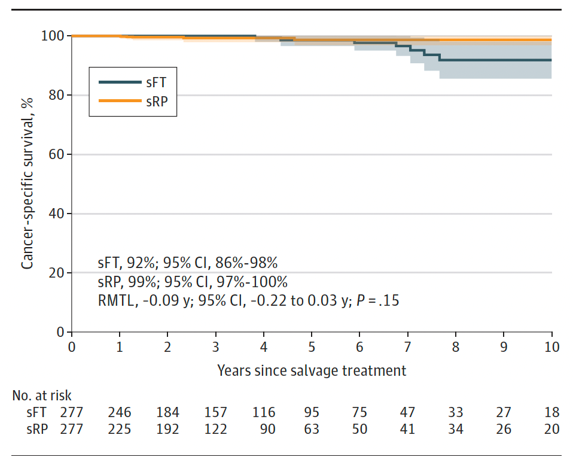
图14. 匹配队列中10年癌症特异性生存期的累积发生率曲线
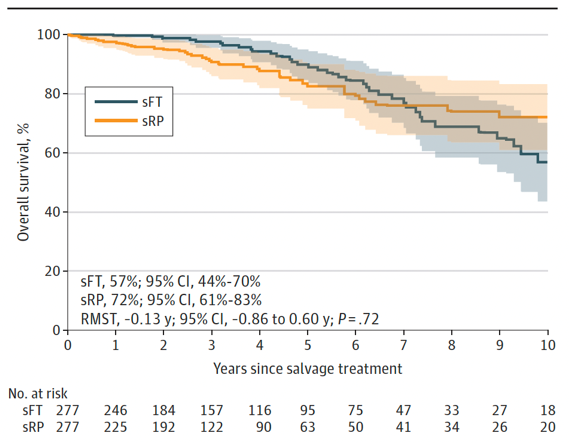
图15. 匹配队列中10年总生存期的Kaplan-Meier曲线
6. 钠-葡萄糖共转运蛋白2抑制剂用于接受激素治疗的前列腺癌患者
发表期刊:JAMA Oncol
研究意义:初步证据表明,用于糖尿病治疗的钠 - 葡萄糖协同转运蛋白2(SGLT2)抑制剂可能具有抗肿瘤作用,但其在前列腺癌中的潜在获益尚未被探索。明确其与接受激素治疗患者临床结局的关联,可为未来的辅助治疗策略提供依据。
研究目的:评估接受激素治疗的前列腺癌患者中,使用SGLT2抑制剂是否与临床结局相关。
研究设计、研究地点与研究对象:本项基于人群、采用月度队列的序贯目标试验模拟研究,使用来自香港医院管理局全区域电子健康记录数据(1993年1月1日至2025年4月30日),覆盖约750万人口。纳入诊断为前列腺癌并启动雄激素剥夺治疗(ADT)的成年男性患者。随访截至2025年4月,数据分析时间为2025年6月至10月。
暴露因素:激素治疗期间启动SGLT2抑制剂(主要为达格列净、恩格列净)并持续使用至少1个月。对照组为未使用SGLT2抑制剂的患者。
主要结局指标:主要结局为至ADT失败的时间。次要结局包括至新一代内分泌药物失败的时间、疾病特异性生存期及总生存期。采用互补双对数模型回归进行意向治疗分析和符合方案分析,提供风险比(HR)估计值。
结果:共14223例符合条件的患者(入组中位年龄74岁 [IQR68~80岁]),中位随访66个月(95% CI 65~67个月)。意向治疗分析显示,使用 SGLT2 抑制剂与 ADT 失败风险降低相关(HR 0.63;95% CI 0.41~0.95;P=0.03)(图16),也与新一代内分泌药物失败风险降低相关(HR 0.44;95% CI 0.20~0.97;P=0.04)(图17)。敏感性分析在不同对照亚组中均证实结果稳健(图18、19)。二甲双胍单药治疗与疾病进展无关,但可改善总生存期(HR 0.59;95% CI 0.42~0.83;P=0.002)。达格列净与恩格列净之间未观察到结局的统计学差异。
结论与意义:在这项采用目标试验模拟设计的队列研究中,前列腺癌患者使用 SGLT2 抑制剂与激素治疗失败延迟相关,提示其除降糖外可能具有潜在肿瘤学获益。这些结果支持 SGLT2 抑制剂在前列腺癌治疗中的潜在应用价值。
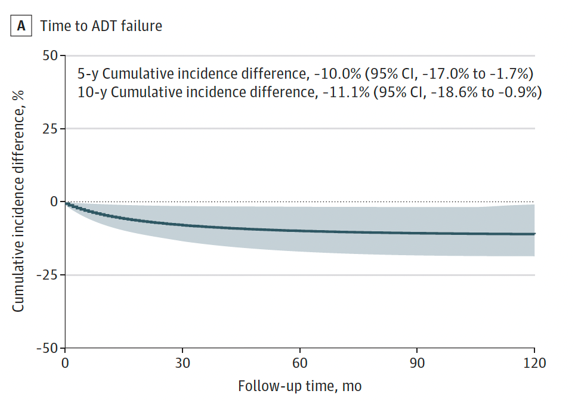
图16. 意向性治疗分析中钠-葡萄糖协同转运蛋白2抑制剂使用者与所有其他患者的雄激素剥夺治疗失败时间累积发生率差异
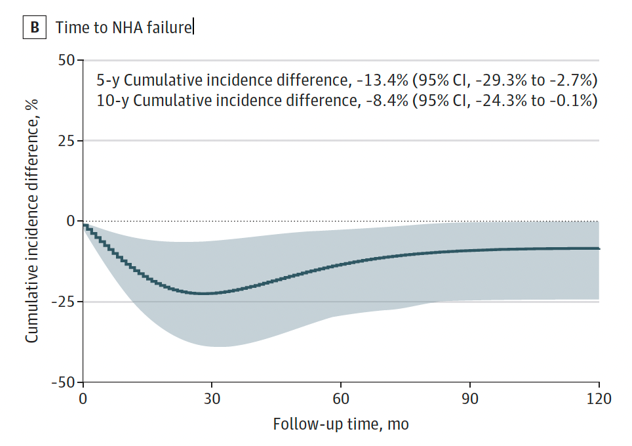
图17. 意向性治疗分析中钠-葡萄糖协同转运蛋白2抑制剂使用者与所有其他患者的新一代内分泌药物失败时间累积发生率差异
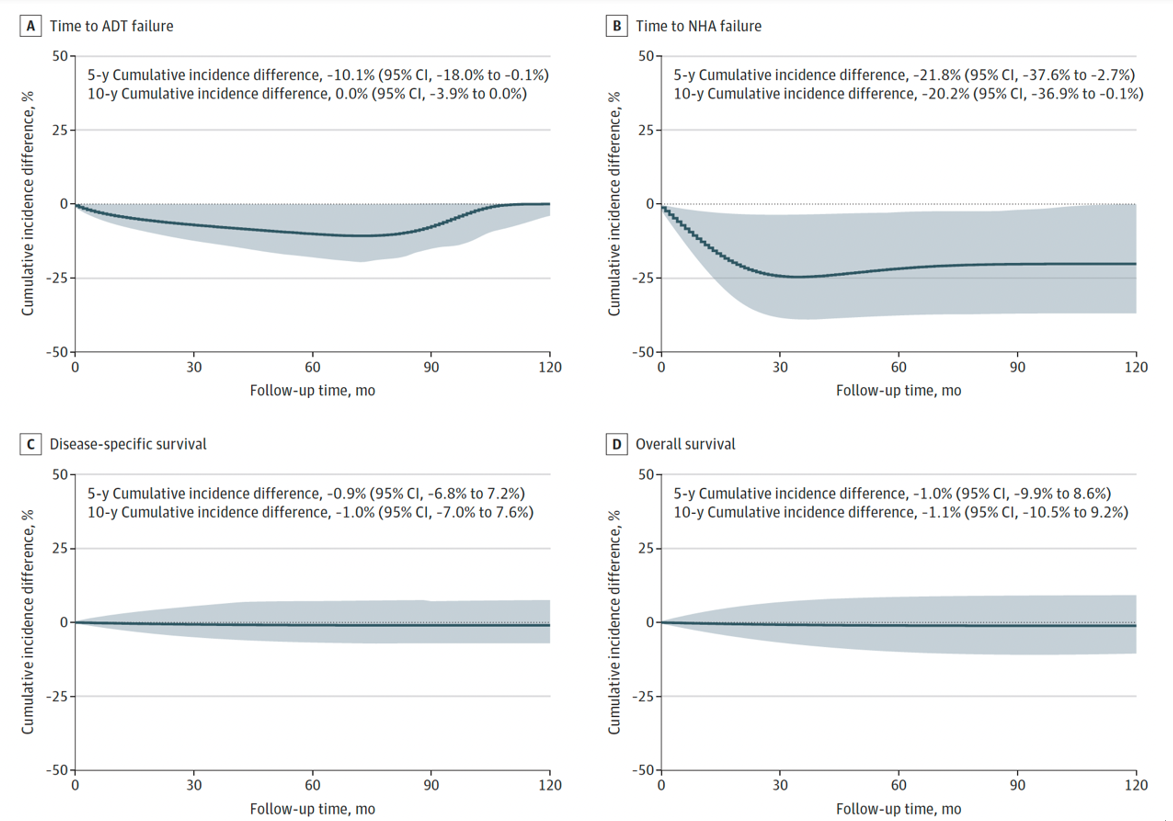
图18. 意向性治疗分析中钠-葡萄糖协同转运蛋白2抑制剂使用者与无糖尿病患者的累积发生率差异
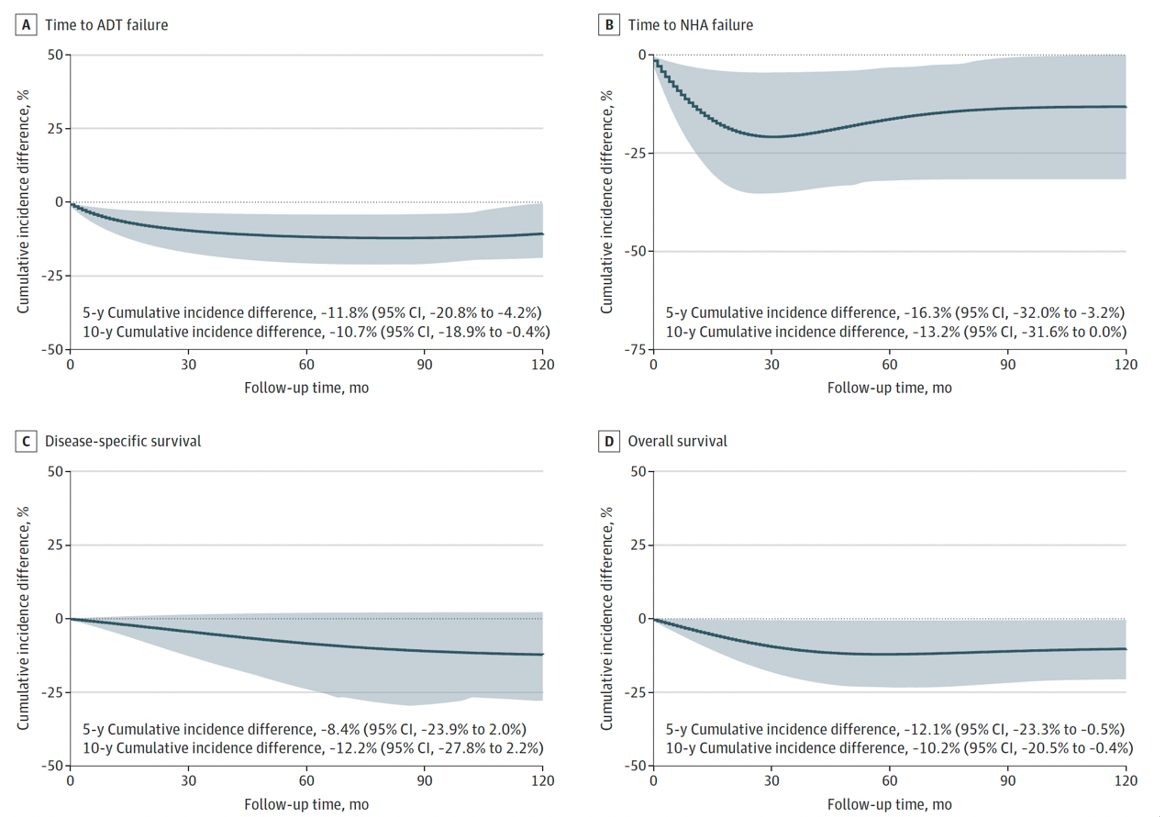
图19. 意向性治疗分析中钠-葡萄糖协同转运蛋白2抑制剂使用者与其他降糖药物治疗患者的累积发生率差异
7. BRCA1或BRCA2致病性胚系变异携带者的针对性前列腺癌筛查可检测出临床相关疾病:IMPACT研究的5年结果
发表期刊:Eur Urol
背景与目的:BRCA1和BRCA2致病性胚系变异(PGV)与前列腺癌(PC)发病风险升高相关。IMPACT研究评估了BRCA1/BRCA2致病性胚系变异携带者接受靶向前列腺特异性抗原(PSA)筛查的价值。本文报道IMPACT研究经过5轮PSA筛查后的结局。
方法:2005—2015年,从20个国家65个中心招募3063名40~69岁受试者(中位年龄54岁),分为两个队列:(1)BRCA1/BRCA2致病性胚系变异携带者(915例BRCA1、901例BRCA2);(2)年龄匹配的家族致病性变异非携带者(727例BRCA1非携带者、520例BRCA2非携带者)。每年进行PSA筛查,PSA>3.0ng/ml作为前列腺穿刺活检指征。本研究旨在通过5轮筛查,比较不同致病性变异状态在以下方面的差异:(1)前列腺癌及临床显著性前列腺癌(csPC,分级分组≥2)的发生率;(2)肿瘤分期与特征。
主要结果与局限性:BRCA1/BRCA2致病性变异携带者与非携带者的前列腺癌发生率无统计学差异。BRCA2致病性变异携带者的临床显著性前列腺癌发生率显著高于非携带者(3.1%vs1.3%;p=0.04)。在确诊前列腺癌的患者中,BRCA1/BRCA2致病性变异组达到美国国立综合癌症网络(NCCN)中危不利组/高危组标准的肿瘤比例高于相应非变异组(BRCA2:65% vs 32%,p=0.029;BRCA1:56%vs18%,p=0.0017)。无T4期或转移性前列腺癌病例。根治性前列腺切除术后病理显示,7/23例(26%)BRCA1致病性变异携带者、10/34例(26%)BRCA2致病性变异携带者存在肿瘤分级升高,而非携带者无分级升高。研究局限性包括穿刺依从性以及2005年以来前列腺癌诊断路径的变化。
结论与临床意义:在BRCA2致病性变异携带者中开展年度PSA筛查证实,与非携带者相比,其临床显著性前列腺癌发生率更高(图20),且可检出具有临床意义的肿瘤(图21)。本研究首次证实,对BRCA1致病性变异携带者进行PSA筛查可早期检出NCCN中危不利组/高危组前列腺癌(图21)。推荐对BRCA2致病性变异携带者进行系统性PSA筛查,BRCA1致病性变异携带者也应考虑筛查。
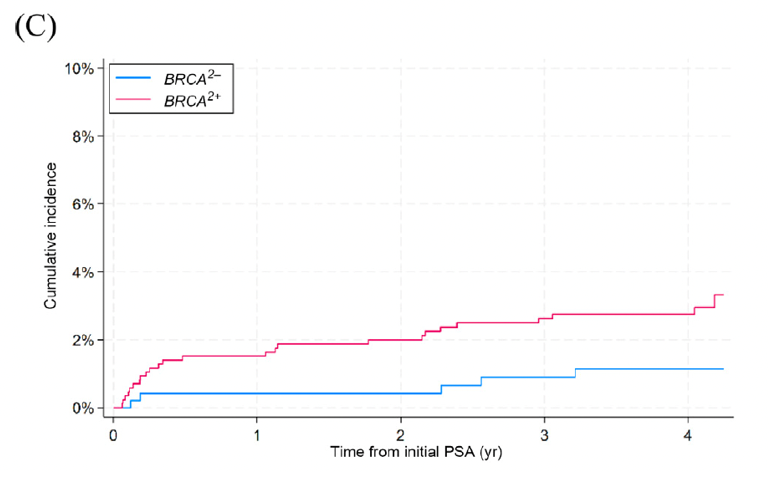
图20. 按BRCA2状态分层的临床显著性前列腺癌的累积发生率
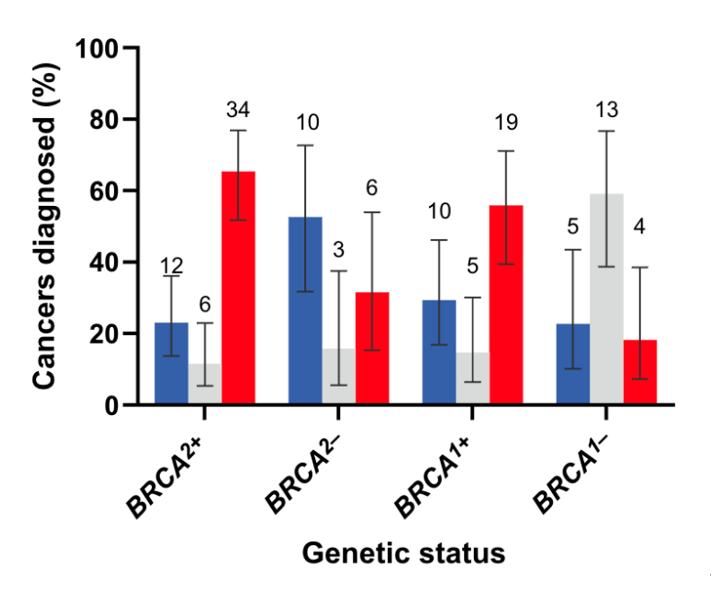
图21. 在五轮筛查中,以前列腺特异性抗原(PSA)>3.0ng/ml为阈值的筛查检出癌症的美国国家综合癌症网络风险分类。蓝色 = 极低危 / 低危;灰色 = 中危(有利型);红色 = 中危(不利型)/ 高危 / 极高危。
膀胱癌
8. 肌层浸润性膀胱癌的优化管理:国际膀胱癌协作组的建议
发表期刊:Eur Urol
背景与目的:随着肌层浸润性膀胱癌(MIBC)围手术期新治疗方案及保膀胱策略的不断涌现,其临床管理正快速发展。本文就临床实践及临床试验设计中MIBC患者的临床分期与最佳治疗时序提供指导意见。
方法:国际膀胱癌协作组(IBCG)召集全球膀胱癌领域专家制定MIBC管理推荐意见并指导临床试验设计。各工作组回顾文献并形成推荐草案,随后IBCG成员于2024年8月通过现场会议采用改良德尔菲法进行投票。会议中达成≥75%共识的推荐意见经进一步修订后予以发布。
主要结果与局限性:IBCG推荐对MIBC患者进行全面临床分期及多学科诊疗。现有回顾性对比研究提示,根治性膀胱切除术(RC)与三联治疗的肿瘤学疗效相近。单纯鳞状细胞癌或腺癌患者优选初始根治性膀胱切除术,其他组织学亚型推荐在根治性膀胱切除术前接受以顺铂为基础的新辅助治疗(表3a)。根治性膀胱切除术后应采用基于风险分层的辅助治疗策略(表3b)。目前除临床试验外,尚无经验证的预测生物标志物可用于指导MIBC临床决策(表3c)。IBCG推荐围手术期治疗试验采用时间 事件终点,保膀胱试验采用保留膀胱无事件生存期终点,并强调纳入患者报告的生活质量终点(表3d)。
结论与临床意义:国际膀胱癌协作组共识推荐为肌层浸润性膀胱癌的最佳治疗时序策略提供了实用临床指导。

表3(a). 国际膀胱癌小组关于肌层浸润性膀胱癌新辅助治疗的共识推荐

表3(b). 国际膀胱癌小组关于肌层浸润性膀胱癌辅助治疗的共识推荐

表3(c). 国际膀胱癌小组关于肌层浸润性膀胱癌患者选择的生物标志物的共识推荐

表3(d). 国际膀胱癌小组关于肌层浸润性膀胱癌试验设计与适宜终点的共识推荐
参考文献
- Motzer RJ, Albiges L, Aguirre SAT, et al. Cabozantinib plus nivolumab and ipilimumab in previously untreated, advanced renal cell carcinoma: final results and biomarker analyses from the phase III COSMIC-313 study. Ann Oncol. Published online February 18, 2026. doi:10.1016/j.annonc.2026.02.011
- Shore ND, Luz MA, De Giorgi U, et al. Improved Survival with Enzalutamide in Biochemically Recurrent Prostate Cancer. N Engl J Med. Published online October 19, 2025. doi:10.1056/NEJMoa2510310
- Tang C, Sherry AD, Hwang H, et al. Metastasis-directed therapy and standard of care versus standard of care for oligometastatic prostate cancer (WOLVERINE): a systematic review and individual patient data meta-analysis from the X-MET collaboration. Lancet Oncol. 2026;27(2):181-190. doi:10.1016/S1470-2045(25)00658-8
- Soeterik TFW, Miszczyk M, Peters M, et al. Nomogram-based risk classification for predicting response to metastasis-directed stereotactic body radiotherapy in PSMA PET-staged oligorecurrent prostate cancer (PORTAL): an international, retrospective cohort study. Lancet Oncol. Published online February 16, 2026. doi:10.1016/S1470-2045(25)00717-X
- Light A, Peters M, Arya M, et al. Salvage Focal Therapy vs Radical Prostatectomy for Localized Radiorecurrent Prostate Cancer. JAMA Oncol. Published online February 12, 2026. doi:10.1001/jamaoncol.2025.6448
- Shi R, Zhan Y, Ma R, et al. Sodium-Glucose Cotransporter 2 Inhibitors for Patients With Prostate Cancer Undergoing Hormone Therapy. JAMA Oncol. Published online January 8, 2026. doi:10.1001/jamaoncol.2025.5869
- Bancroft EK, Page EC, McHugh J, et al. Targeted Prostate Cancer Screening in Carriers of BRCA1 or BRCA2 Pathogenic Germline Variants Detects Clinically Relevant Disease: 5-year Results from the IMPACT Study. Eur Urol. Published online February 18, 2026. doi:10.1016/j.eururo.2026.01.031
- Gupta S, Li R, Hensley PJ, et al. Optimal Management of Muscle-invasive Bladder Cancer: Recommendations from the International Bladder Cancer Group. Eur Urol. Published online February 21, 2026. doi:10.1016/j.eururo.2026.01.029



