
肾细胞癌简称肾癌(RCC)是起源于肾小管上皮的恶性肿瘤,约占肾脏恶性肿瘤的90%,晚期RCC因肿瘤发生扩散、转移,外科手术已达不到根治目的,传统放化疗效果差,患者生存预后不佳。在细胞因子作为RCC全身系统性治疗药物的时代,晚期RCC的中位总生存期(mOS)仅为13个月。自2005年以来随着多种抗肿瘤新生血管形成的酪氨酸激酶抑制剂(TKI)不断问世,靶向治疗成为RCC主要的系统性治疗,晚期RCC一线靶向治疗后的mOS可延长至22个月。近10年来,多个免疫检查点抑制剂(ICI)陆续获批用于晚期RCC的一线和后线系统性治疗,使得患者生存期再次得以延长[1]。随着靶向、免疫等治疗药物的研究进展,晚期RCC治疗也取得了长足的进步。多项靶免联合治疗的大型III期研究相继取得成功,标志着晚期肾癌一线治疗现已全面进入靶免联合治疗时代。本文旨在探讨一线靶免联合疗法在晚期肾癌中的应用,为临床治疗决策提供参考。
一. 晚期肾癌靶免联合治疗组合中TKI类药物概况
1. 阿昔替尼
阿昔替尼是一种口服的、作用于血管内皮生长因子受体(VEGFR)1,2和3的强效和高选择性酪氨酸激酶抑制剂,抑制肿瘤生长、血管新生和肿瘤进展[2]。2015年4月,阿昔替尼在中国首次获批,用于既往接受过一种TKI或细胞因子治疗失败的进展期RCC的成人患者[3]。2025年4月,国家药品监督管理局(NMPA)正式批准阿昔替尼+特瑞普利单抗用于中高危不可切除或转移性RCC患者的一线治疗[4]。这是中国首个获批的靶免联合方案,填补国内领域空白的同时有力推动了中国晚期肾癌治疗与国际标准接轨。
1.1 RENOTORCH研究:中国数据改写临床实践
中国晚期肾癌治疗长期受限于“国际数据主导临床决策”,而RENOTORCH研究作为首个完全基于中国人群的III期靶免联合研究,不仅为阿昔替尼+特瑞普利单抗的获批提供了核心证据,更以本土高质量数据改变了国内肾癌一线治疗格局。
RENOTORCH研究是一项多中心、随机、开放标签的III期临床试验[5],覆盖全国47家研究中心。研究共随机入组421例中高危的不可切除或转移性RCC患者,以1:1随机分配至特瑞普利单抗+阿昔替尼组(n=210)或舒尼替尼组(n=211)。主要研究终点为盲态独立中心审查(BICR)评估的无进展生存期(PFS),次要研究终点包括研究者评估的PFS、IRC或研究者评估的客观缓解率(ORR)、缓解持续时间(DOR)、疾病控制率(DCR)、总生存期(OS)以及安全性等。
在主要终点方面,阿昔替尼+特瑞普利单抗组经BICR评估的中位PFS为18.0个月,2年PFS率为44.6%;舒尼替尼组中位PFS为9.8个月,2年PFS率为30.2%;显著降低35%的疾病进展或死亡风险(HR=0.65,95% CI:0.49-0.86,P=0.0028,图1)。此外,所有亚组均观察到阿昔替尼+特瑞普利单抗治疗组的PFS获益(包括国际转移性肾细胞癌数据库联盟[IMDC]风险组、疾病转移情况和既往肾切除术史等)。
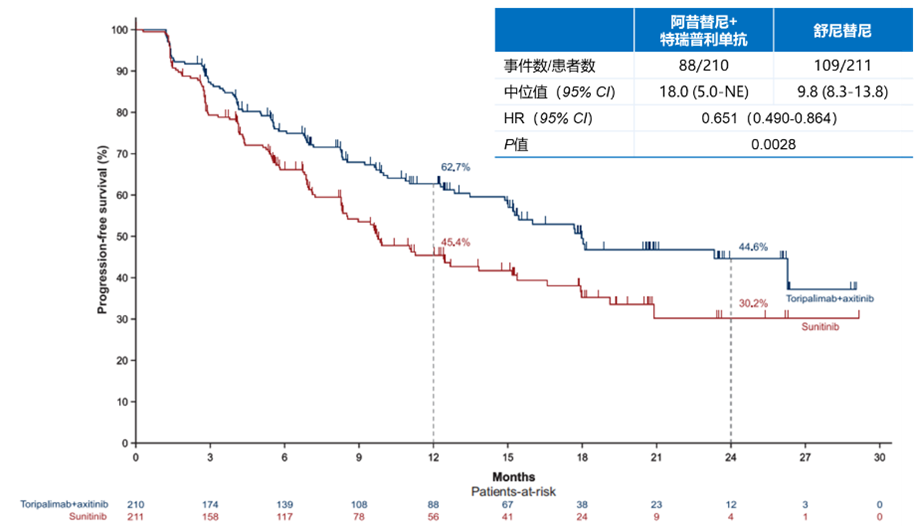
图1. 阿昔替尼+特瑞普利单抗组 vs 舒尼替尼组经BICR评估的PFS
在次要终点方面,阿昔替尼+特瑞普利单抗组经BICR评估的ORR显著优于舒尼替尼组(56.7% vs 30.8%,P<0.0001)。截至目前,阿昔替尼+特瑞普利单抗组未达到中位OS,舒尼替尼组中位OS为26.8个月,2年OS率分别为71.8%和63.2%;阿昔替尼+特瑞普利单抗组OS已展现出显著获益的趋势,死亡风险降低39%(HR=0.61,95% CI:0.40-0.92,P=0.0186,图2)。
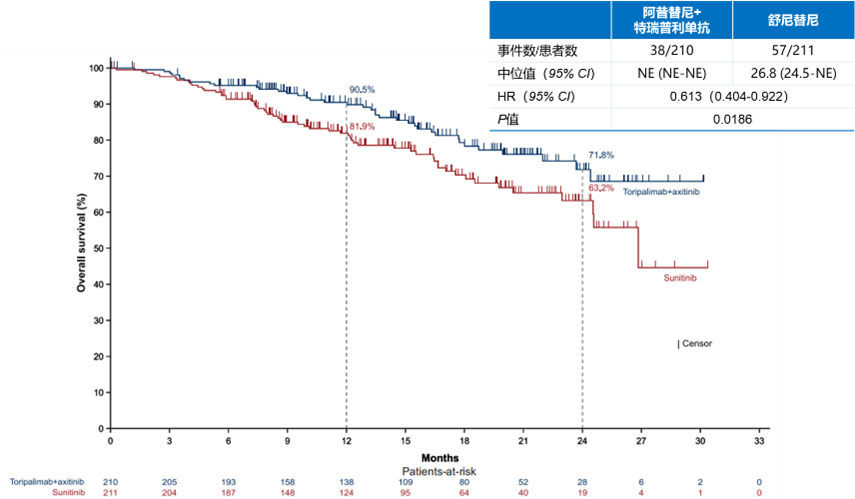
图2. 阿昔替尼+特瑞普利单抗组 vs 舒尼替尼组的OS
安全性方面,阿昔替尼+特瑞普利单抗组表现出良好的安全性,其中血液学毒性较对照组相比更小,未发现新的安全性信号。
2. 仑伐替尼
CLEAR研究是一项随机、开放标签、III期研究[9]。纳入晚期RCC初治患者,以1:1:1随机分配至三组,分别接受仑伐替尼+帕博利珠单抗组、仑伐替尼+依维莫司和舒尼替尼组。符合条件的患者1069例,其中仑伐替尼+帕博利珠单抗组患者355例,舒尼替尼组患者357例,大多数患者为中等风险。主要终点为OS,次要终点包括独立影像学审查(IIR)评估的PFS、ORR、DOR和研究者评估的第二次无进展生存期(PFS2)。
在主要终点方面,仑伐替尼+帕博利珠单抗组和舒尼替尼组的中位OS分别为53.7个月和54.3个月,36个月OS率分别为66.4%和60.2%,死亡风险降低21%(HR=0.79,95% CI:0.63-0.99,图5)。进一步的亚组分析结果显示,仑伐替尼+帕博利珠单抗仅仅在IMDC高危的患者中有OS获益,而在IMDC低危与中危患者中均无法获益,然而由于高危患者样本量较小,这一结果还需谨慎解读。
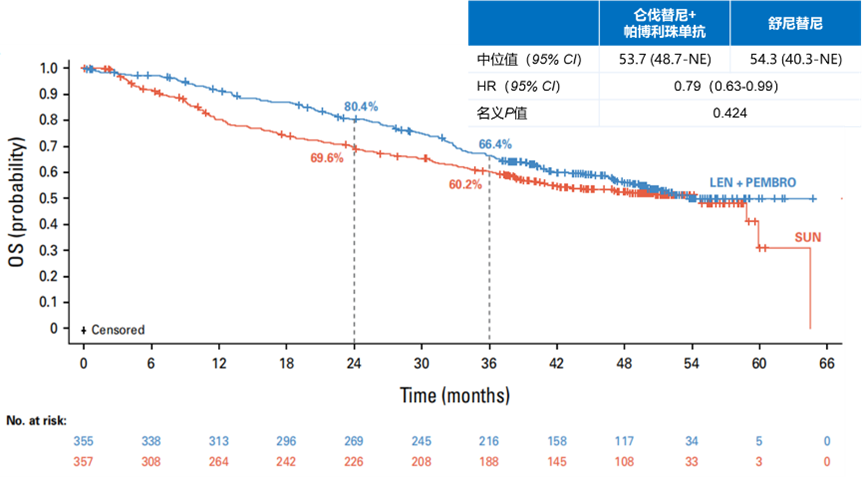
图5. 仑伐替尼+帕博利珠单抗组 vs 舒尼替尼组的OS
在次要终点方面,仑伐替尼+帕博利珠单抗组和舒尼替尼组的中位PFS分别为23.9个月和9.2个月,疾病进展或死亡风险降低53%(HR=0.47,95% CI:0.38-0.57,图6)。在所有IMDC和纪念斯隆凯特琳癌症中心(MSKCC)风险亚组中,仑伐替尼+帕博利珠单抗组的PFS均优于舒尼替尼组。
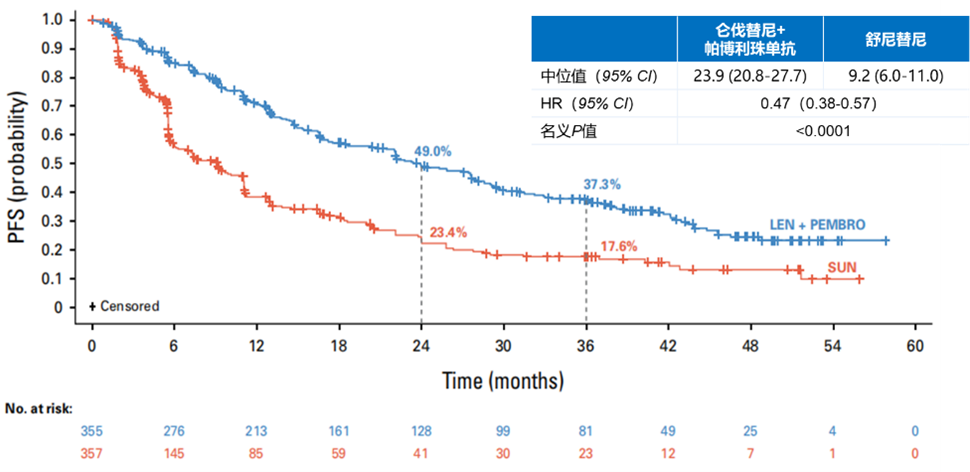
图6. 仑伐替尼+帕博利珠单抗组 vs 舒尼替尼组的PFS
安全性方面,仑伐替尼+帕博利珠单抗组中≥3级AE发生率更高,因AE导致的剂量调整比例更高。常见不良事件为腹泻、高血压、甲状腺功能减退、食欲下降等。
3. 安罗替尼
ETER-100研究是一项开放标签、随机对照、多中心的III期研究[10,11]。纳入转移性或不可切除晚期透明细胞RCC初治患者,以1:1随机分配至安罗替尼+贝莫苏拜单抗组(n=266)或舒尼替尼组(n=265)。纳入患者整体身体状态较优,转移灶数量较少。主要终点为BICR 评估的PFS。次要终点包括研究者评估的PFS、OS、ORR、DOR、DCR和安全性等。
在主要终点方面,初步分析结果显示,安罗替尼+贝莫苏拜单抗组较舒尼替尼组显著延长患者BICR 评估的PFS,中位PFS分别为18.96个月 vs 9.76个月,疾病进展或死亡风险降低47%(HR=0.53,95% CI:0.42-0.67,P<0.0001,图7)。
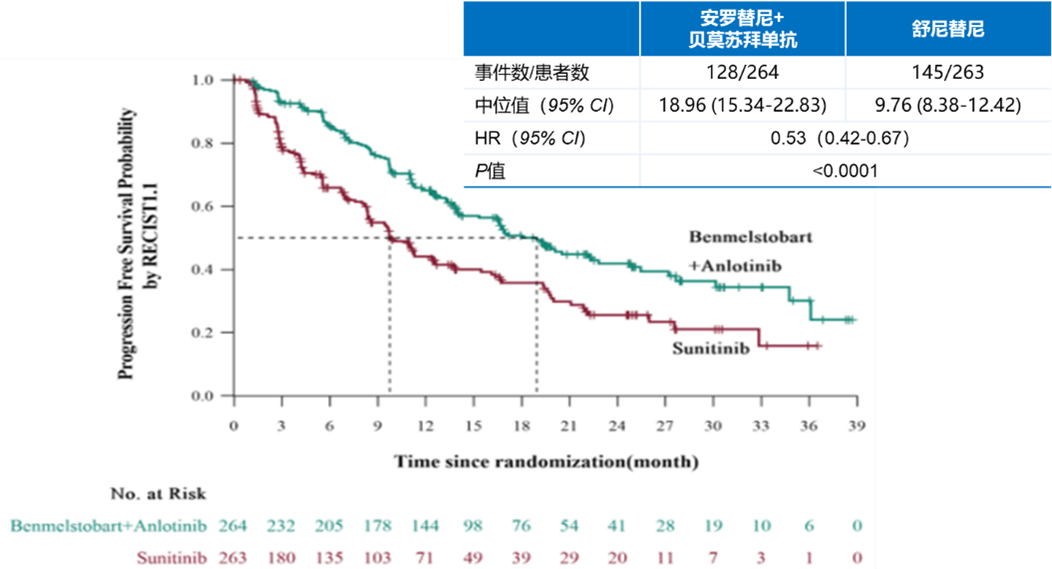
图7. 安罗替尼+贝莫苏拜单抗组 vs 舒尼替尼组经BICR评估的PFS
在次要终点方面,安罗替尼+贝莫苏拜单抗组较舒尼替尼组显著提高患者ORR(71.6% vs 25.1%,P<0.001)。两组中位OS均为未达到,安罗替尼+贝莫苏拜单抗组显示出OS获益趋势(HR=0.66,95% CI:0.48-0.92,P=0.0673,图8)。
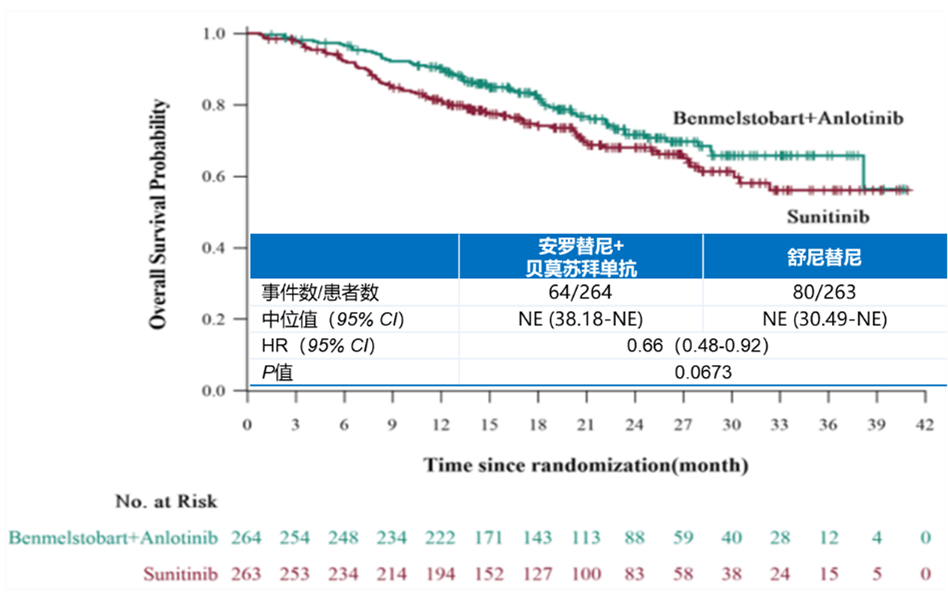
图8. 安罗替尼+贝莫苏拜单抗组 vs 舒尼替尼组的OS
最新亚组分析显示,在各个亚组中,安罗替尼+贝莫苏拜单抗组较舒尼替尼组的PFS和ORR均有显著获益趋势。其中IMDC中高危亚组患者的中位PFS分别为17.0个月 vs 9.7个月(P<0.001),ORR分别为70.0% vs 21.6%(P<0.0001);肝转移亚组患者的中位PFS 分别为11.9个月 vs 5.4个月(P=0.0121),ORR 分别为60.0% vs 7.4%(P<0.0001);骨转移亚组患者的中位PFS分别为19.5个月 vs 8.3个月(P=0.0154),ORR分别为63.2% vs 16.7%(P<0.0001)。
安全性方面,安罗替尼+贝莫苏拜单抗显示出良好的安全性,联合治疗与每种药物已知安全性一致。常见≥3级治疗相关不良事件(TRAE)为高血压、蛋白尿、高甘油三酯血症、手足综合征等。
4. 卡博替尼
CheckMate-9ER研究是一项开放标签、随机对照的III期研究[12]。 纳入晚期透明细胞RCC初治患者,不论IMDC情况。以1:1随机分配至卡博替尼+纳武利尤单抗组(n=323) 和舒尼替尼组(n=328)。主要终点为BICR 评估的PFS。次要终点包括OS、ORR和安全性等。
在主要终点方面,经过67.6个月随访后,卡博替尼+纳武利尤单抗组较舒尼替尼组延长BICR 评估的PFS,获益情况保持稳定,中位PFS分别为16.4个月和8.3个月,疾病进展或死亡风险降低42%(HR=0.58,95% CI:0.49-0.70,图9)。
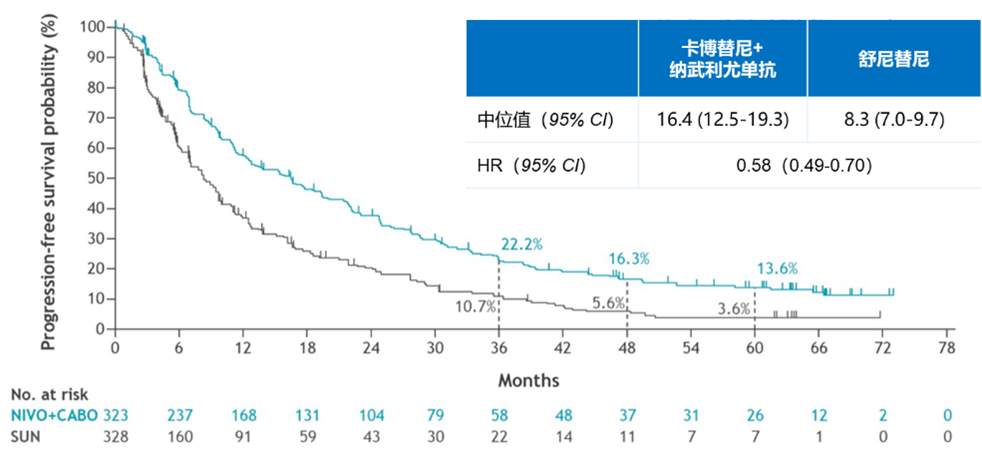
图9. 卡博替尼+纳武利尤单抗组 vs 舒尼替尼组经BICR评估的PFS
在次要终点方面,随着随访时间的延长,卡博替尼+纳武利尤单抗组的OS持续保持获益,两个治疗组的中位OS分别为46.5个月和35.5个月,死亡风险降低21%(HR=0.79,95% CI:0.65-0.96,图10)。此外,卡博替尼+纳武利尤单抗组的ORR优于舒尼替尼组(55.7% vs 27.4%),其中卡博替尼+纳武利尤单抗组治疗的患者中有13.9%达到CR,在剩余41.5%的部分缓解(PR)患者中,又有一半的患者缩瘤比例≥60%。安全性方面,两个治疗组≥3级TRAE的发生率分别为68%和55%,其中最常见的不良反应分别为腹泻、手足综合征、高血压、疲乏和甲减。
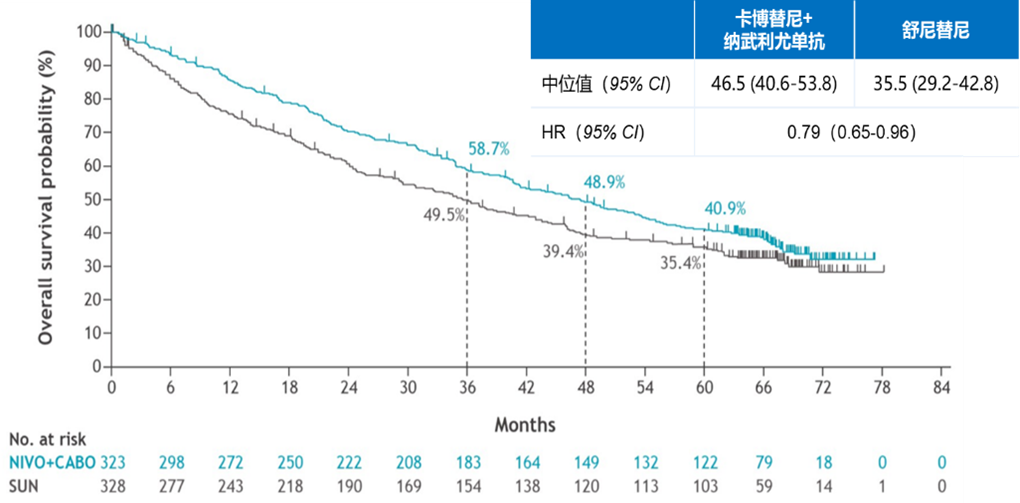
图10. 卡博替尼+纳武利尤单抗组 vs 舒尼替尼组的OS
亚组分析显示,在对患者的IMDC风险进行分层后发现,在IMDC低危患者中,卡博替尼+纳武利尤单抗仅能改善患者的PFS,但无法显著改善OS;而在IMDC中高危患者中,卡博替尼+纳武利尤单抗组同时显著改善患者的PFS和OS预后。然而,无论患者的IMDC分层如何,卡博替尼+纳武利尤单抗组均可显著缩瘤,ORR均显著高于舒尼替尼组。此外,在对基线期患者远端转移情况进行亚组分析后发现,纳武利尤单抗+卡博替尼不论在基线期存在肝转移、肺转移、骨转移的患者中均可显著改善生存预后。
此外,在卡博替尼+纳武利尤单抗组中,约43%的患者有机会接受后线治疗,而在舒尼替尼组中这一比例为55%;有机会接受≥3线治疗的患者比例在两组中分别为26%和31%。
二. 不同TKI类药物在靶免联合中的差异
在IMDC中/高危人群中,TKI联合免疫治疗疗效均优于TKI单药,成为该类人群的优选方案(表1)。然而,值得注意的是,由于ETER-100研究对照组采用了国产仿制舒尼替尼,因此部分结果如HR值等的参考性仍有待验证。此外,尽管CheckMate-9ER研究表明卡博替尼+纳武利尤单抗方案在中/高危人群中可有效控制疾病进展、延长患者生存期,但目前在中国未获批上市。最后,CLEAR研究尚存在一定的局限性:①尽管仑伐替尼+帕博利珠单抗组在PFS上有着所有研究中相对最好的表现,但在OS的表现上却不令人满意,这一结果表明,一线使用仑伐替尼+帕博利珠单抗可能会失去一定的后线治疗机会;②仑伐替尼+帕博利珠单抗中使用的仑伐替尼剂量为20mg,临床实践中亚洲患者可能无法耐受需要减量。
综上所述,虽然目前RENOTORCH研究的OS数据尚不成熟,但是从趋势来看,一线靶免联合治疗患者的OS高于舒尼替尼。总体而言,特瑞普利单抗联合阿昔替尼方案可使中国晚期RCC患者的OS进一步延长。阿昔替尼+特瑞普利单抗应用于中/高危RCC治疗,不仅是对现有治疗边界的拓展,更有望为该类患者带来新的治疗机会,具有重要的临床价值。
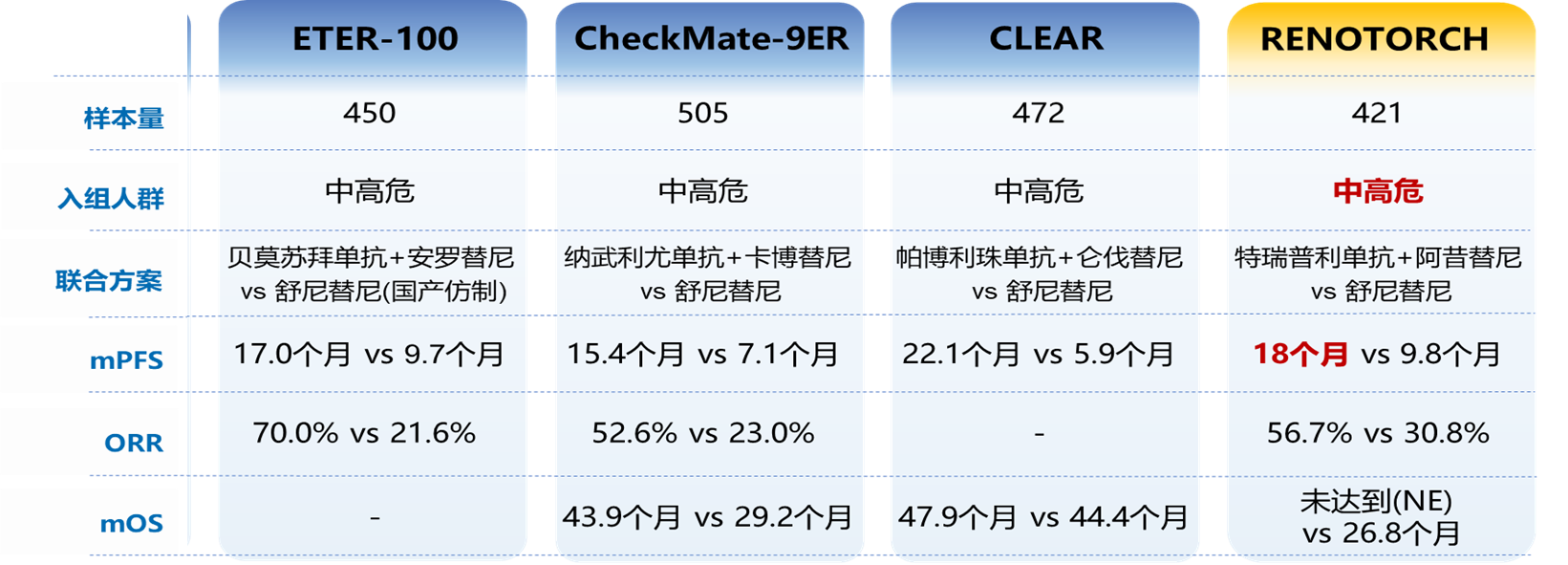
表1. 靶向联合免疫治疗RCT临床研究中高危亚组分析数据汇总
总结
在过去的十几年中,晚期肾癌治疗从细胞因子过渡到针对血管内皮生长因子的靶向治疗时代。随着免疫治疗的蓬勃发展,又为晚期患者带来了破晓曙光。在短短几年间,肾癌已经成为了热门瘤种,一线靶向联合免疫治疗也毫无争议地成为了晚期肾癌的治疗首选,而且还在不断发展与完善中。可以看到,更多全新治疗模式和策略还在不断探索中,未来或将改写晚期肾癌的治疗版图。
参考文献
- 中国抗癌协会泌尿男生殖系肿瘤专业委员会肾癌学组. 晚期肾透明细胞癌一线靶向治疗的优化选择中国专家共识(2022) [J]. 临床泌尿外科杂志, 2022, 37(5): 329-337.
- 阿昔替尼片说明书. 2025年04月23日.
- https://news.bioon.com/article/44628e213541.html
- 2025年04月25日药品批准证明文件送达信息 https://www.nmpa.gov.cn/zwfw/sdxx/sdxxyp/yppjfb/20250425151104133.html?type=pc&m=
- Yan XQ, Ye MJ, Zou Q, et al. Toripalimab plus axitinib versus sunitinib as first-line treatment for advanced renal cell carCInoma: RENOTORCH, a randomized, open-label, phase III study. Ann Oncol. 2024 Feb;35(2):190-199.
- https://www.fda.gov/drugs/drug-approvals-and-databases/fda-approves-pembrolizumab-plus-axitinib-advanced-renal-cell-carCInoma
- Brian I. Rini, et al. ASCO 2023. Abstract LBA4501.
- Plimack ER, Powles T, Stus V, et al. Pembrolizumab Plus Axitinib Versus Sunitinib as First-line Treatment of Advanced Renal Cell CarCInoma: 43-month Follow-up of the Phase 3 KEYNOTE-426 Study. Eur Urol. 2023 Nov;84(5):449-454.
- Motzer RJ, Porta C, Eto M, et al. Lenvatinib Plus Pembrolizumab Versus Sunitinib in First-Line Treatment of Advanced Renal Cell CarCInoma: Final PrespeCIfied Overall Survival Analysis of CLEAR, a Phase III Study. J Clin Oncol. 2024 Apr 10;42(11):1222-1228.
- Xinan Sheng, et al. ASCO 2025. Abstract 4536.
- Xinan Sheng et al, 2024 ESMO. Abstract LBA76.
- Motzer R, et al. 2025 ASCO-GU. Abstract 439.



