本品适用于患有以下疾病且体重 ≥ 35 kg的 12 岁及以上儿童和成人患者的常规预防治疗,以防止出血或降低出血发作的频率: 1
不存在凝血因子VIII抑制物的重型A型血友病(先天性凝血因子VIII缺乏,FVIII<1%)或
不存在凝血因子IX抑制物的重型B型血友病(先天性凝血因子IX缺乏,FIX<1%)。 1
血友病治疗新策略:重新实现止血平衡 2
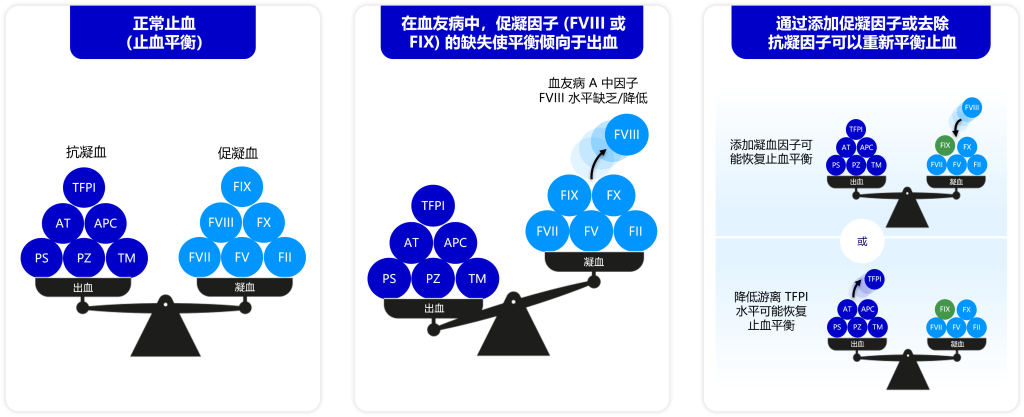
注意:此处仅显示血友病 A(缺乏/降低 FVIII 水平)用于说明目的。请对血友病 B (缺乏/降低 FIX 水平)进行相应理解。
AT=抗凝血酶; APC=活化蛋白 C; FII=因子 II; FIX=因子 IX; FV=因子 V; FVII=因子 VII; FVIII=因子 VIII; FX=因子 X; PS=蛋白 S; PZ=蛋白Z;
TFPI=组织因子途径抑制物; TM=血栓调节蛋白。
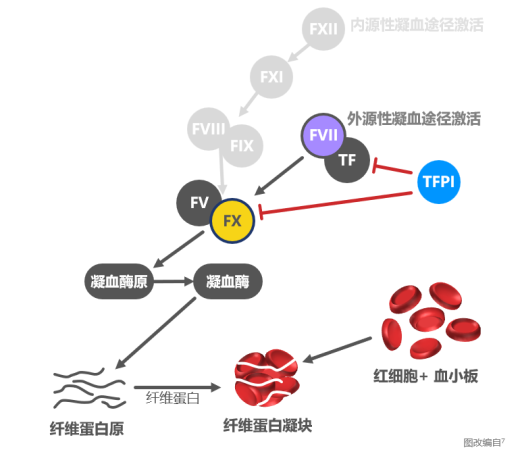
组织因子途径抑制物(TFPI)是凝血启动阶段的主要抑制物
TFPI 是一种 Kunitz 型丝氨酸蛋白酶抑制剂,可作为凝血过程的负性调控因子3,4
TFPI 是组织因子(TF)–FVIIa复合物的主要抑制物,此复合物可激活 FX 生成 FXa4,5
TFPI 亦可直接抑制 FXa 来调节凝血过程
FXa 是外源性与内源性凝血途径的共同通路,是产生凝血酶4,6以及启动凝血过程的关键步骤
TF: 组织因子; TFPI: 组织因子途径抑制物
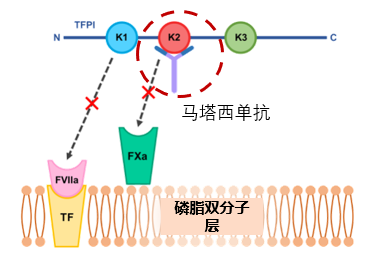
马塔西单抗通过靶向组织因子途径抑制物 (TFPI )Kunitz 结构域 2(K2),直接阻止 TFPI 介导的 FXa 抑制作用;而 TFPI 介导的 FVIIa/TF 复合物抑制作用取决于其对 FXa 的抑制作用,因此又可间接防止 FVIIa/TF 复合物失活,进而增强凝血功能,促进凝血酶生成,实现止血3,8
预充式注射器(PFS)装:150 mg(1 mL)/ 支1
1.推荐剂量仅供皮下给药,首次本品治疗时患者应处在无出血状态。如完整剂量需多次注射,则每次注射时换用不同的注射部位。 1
本品用于体重 ≥ 35 kg 的 12 岁及以上患者的推荐剂量如下:
- 负荷剂量
皮下注射 300 mg(分 2 次不同部位注射,每次 150 mg) 1 - 维持剂量
负荷剂量给药后 1 周,开始维持剂量给药,每周一次,即每周在同一天的任意时间皮下注射 150 mg。 1 - 治疗期间的剂量调整 :
经专业医护人员判定当前剂量不足以控制出血事件时,可考虑将体重 ≥50 kg 的患者的剂量调整为每周皮下注射 300 mg(关键性 III 期研究中有12%患者在6 个月后需要剂量调整至300mg;参见说明书中【临床试验】)。尚未充分确定本品在每周 300 mg 以上剂量下的安全性和有效性。 1 - 药物漏用
对于接受维持剂量 150 mg 治疗的患者:
如果漏用一剂,应在下次计划用药日前尽快补用,然后恢复每周常规 150 mg 皮下给药方案(采用与漏用剂量前相同的给药方案或是基于漏用剂量给药日期制定新的给药方案)。 1
如果补用漏用剂量时已超过末次给药 13 天,则应通过皮下注射给予负荷剂量 300 mg,随后恢复每周一次 150 mg 的皮下注射。 1
对于接受维持剂量 300 mg 治疗的患者:
如果漏服一剂或多剂,应尽快补用,然后恢复 300 mg 每周一次皮下给药方案(采用与漏用剂量前相同的给药方案或是基于漏用剂量给药日期制定新的给药方案)。 1 - 改为马塔西单抗注射液
从因子替代的常规预防治疗改为本品治疗:在停用凝血因子后可随时启用本品。 尚无患者从非因子类血友病药品改为本品治疗的数据。1 - 突破性出血的治疗指南
接受本品治疗的患者发生突破性出血时可使用因子 VIII 和因子 IX 产品进行治疗。不得追加本品剂量来治疗突破性出血事件(参见说明书中【注意事项】)。1
2.准备和给药:
- 本品应在专业医护人员的指导下使用。如果经专业医护人员认可,且患者或其护理者已接受适当的皮下注射技术培训,患者可自行注射或由其护理者注射本品。
- 有关完整的注射前准备和给药说明,请参阅说明书中的使用说明。 1
皮下给药之前,从冰箱中取出本品,置于室温15至30分钟,避免阳光直射。请勿使用热水或微波炉等其他方法加热本品。从冰箱中取出本品后,应在 7 天内使用或丢弃(参见说明书中【贮藏】)。 1 - 本品通过皮下注射给药,每周一次,可在一天中任意时间注射,可选择腹部或大腿进行注射。必要时,也可选择其他注射部位。本品在上臂(仅限预充式注射器)给药只能由护理者或医疗保健专业人员进行。本品不可在骨骼区域或皮肤瘀伤、发红、压痛或硬结区域,或有疤痕或妊娠纹的区域进行注射。本品不得静脉注射。每次注射,应轮换使用不同注射部位。 1
- 在使用本品治疗期间,最好在不同的部位注射其他皮下给药药品。 1
- 在给药前应目视检查有无不溶性微粒或变色情况。本品为澄清、无色至淡黄色溶液。如果溶液混浊、呈深黄色或含有薄片或颗粒,请勿使用。1
3. 手术和其他治疗干预时暂时停用
- 围手术期管理
尚未在重大手术环境中评估本品。在临床研究中,曾有患者接受小型外科手术,但手术期间未停止使用本品的常规预防治疗。 1
重大手术前,停用本品并根据当地标准治疗启用凝血因子进行治疗,同时采取措施管理围手术期可能增加的静脉血栓形成风险。对于接受重大手术的血友病患者的剂量指南,请查阅凝血因子的产品信息。恢复本品治疗前应考虑患者的整体临床情况,包括是否存在术后血栓栓塞的风险因素、其他止血产品和其他伴随用药的使用情况(参见说明书中【用法用量】- 药物漏用)。 1
- 急性重症患者的管理
在急性重症患者中使用本品的经验有限。本品使用期间若出现以下情况,如发生急性重症(如严重感染、脓毒症、外伤),期间凝血活化可能增加,同时专业医护人员认为这可能会增加本品给药相关风险,应考虑暂时停用本品。应按照当地标准治疗对急性重症的治疗情况进行管理,此时应根据使用本品的潜在风险权衡是否继续使用本品进行治疗。一旦患者达到了临床治愈,即可恢复本品治疗(参见说明书中【用法用量】- 药物漏用)。 1
4. 妊娠试验
在开始本品治疗前,确认有生育能力的女性未怀孕(参见说明书中【注意事项】和【孕妇及哺乳期妇女用药】)。 1
5.特殊人群
- 肝功能不全
轻度肝功能不全患者无需进行剂量调整(参见说明书中【临床药理】)。目前尚未在中度或重度肝功能不全患者中进行本品研究。1 - 肾功能不全
轻度肾功能不全患者无需进行剂量调整(参见说明书中【临床药理】)。目前尚未在中度或重度肾功能不全患者中进行本品研究。1 - 老年人
65 岁以上患者无需进行剂量调整(参见说明书中【临床药理】)。 1
无1
尚未开展关于本品的药物相互作用的临床研究。 1
本品是一种单克隆抗体 (mAb),预计将通过分解代谢途径清除。因此,与通过非分解代谢途径清除的伴随药品的相互作用不太可能对其清除产生影响。此外,预计马塔西单抗等生物制剂不会对细胞色素 P450 酶表达产生间接影响。 1
贮藏1
于2℃ 至8℃下,在原纸盒中保存以避光。
必要时,可在原纸盒中于室温(最高 30℃)下储存一次,最多储存 7 天。
一旦在室温下储存,请勿送回冰箱,并在7天后丢弃。
请勿冷冻。
请勿振摇。
有效期1
36个月。
不伴FVIII抑制物的血友病A或不伴FIX抑制物的血友病B
在入组 BASIS 研究(NCT03938792)(一项开放性、多中心、两阶段研究)的 116 例无 FVIII 抑制物的重度血友病A或无 FIX 抑制物的重度血友病B成人和儿童患者(年龄 ≥12 岁且体重 ≥35 kg)中确定了本品的有效性。重型血友病定义为凝血因子活性 <1%。本研究排除了有冠状动脉疾病、静脉或动脉血栓形成或缺血性疾病史的患者。1
表 1. 在 ≥12 岁不伴因子VIII或因子IX抑制物的患者中,本品常规预防治疗与因子替代的按需治疗的年出血率比较1
| 按检验层级顺序列出的终点 | 6 个月观察期接受因子替代 的按需治疗 (N = 33) | 12 个月研究药物治疗期的 马塔西单抗常规预防治疗 (N = 33) |
|---|---|---|
| 经治疗出血(主要) | ||
| ABR,基于模型 (95% CI) | 38.00 (31.03, 46.54) | 3.18 (2.09, 4.85) |
| 对比 OD 的比值 (95% CI) p 值 | 0.084 (0.059, 0.119) < 0.0001 | |
| 自发性出血,经治疗 | ||
| ABR,基于模型 (95% CI) | 30.93 (24.12, 39.67) | 2.44 (1.61, 3.69) |
| 对比 OD 的比值 (95% CI) p 值 | 0.079 (0.054, 0.114) < 0.0001 | |
| 关节出血,经治疗 | ||
| ABR,基于模型 (95% CI) | 32.86 (26.15, 41.29) | 2.83 (1.81, 4.44) |
| 对比 OD 的比值 (95% CI) p 值 | 0.086 (0.059, 0.125) < 0.0001 | |
| 总出血,经治疗和未经治疗 | ||
| ABR,基于模型 (95% CI) | 47.76 (39.60, 57.60) | 7.39 (5.08, 10.74) |
| 对比 OD 的比值 (95% CI) p 值 | 0.155 (0.116, 0.207) < 0.0001 | |
| 靶关节出血,经治疗 | ||
| ABR,基于模型 (95% CI) | 23.18 (17.20, 31.24) | 1.84 (1.06, 3.17) |
| 对比 OD 的比值 (95% CI) p 值 | 0.079 (0.051, 0.124) < 0.0001 | |
•p 值是基于比值=0.5 的零假设。
•ABR 的均值估计值、比值和置信区间 (CI) 来自负二项回归模型。
根据 ISTH 标准调整出血定义:经治疗出血 = 接受 FVIII 或 FIX 治疗的出血;
•总出血量 = 接受或未接受 FVIII 或 FIX 治疗的出血
•ABR = 年出血率;CI = 置信区间;OD = 按需治疗
表2. 在 ≥12岁不伴因子VIII或因子IX抑制物的患者中,本品常规预防治疗与既往因子替代的常规预防治疗的年出血率比较1
| 按检验层级顺序列出的终点 | 6 个月观察期间因子替代的 常规预防治疗 (N = 83) | 12 个月研究药物治疗期的马塔西单抗 常规预防治疗 (N = 83) |
|---|---|---|
| 经治疗出血(主要) | ||
| ABR,基于模型 (95% CI) | 7.85 (5.09, 10.61) | 5.08 (3.40, 6.77) |
| 对比 RP 的比值 (95% CI) | -2.77 (-5.37,-0.16)* | |
| 自发性出血,经治疗 | ||
| ABR,基于模型 (95% CI) | 5.86 (3.54, 8.19) | 3.78 (2.25, 5.31) |
| 对比 RP 的比值 (95% CI) | -2.09 (-4.23, 0.06) | |
| 关节出血,经治疗 | ||
| ABR,基于模型 (95% CI) | 5.66 (3.33, 7.98) | 4.13 (2.59, 5.67) |
| 对比 RP 的比值 (95% CI) | -1.53 (-3.70, 0.64)* | |
| 总出血,经治疗和未经治疗 | ||
| ABR,基于模型 (95% CI) | 8.84 (5.97, 11.72) | 5.97 (4.13, 7.81) |
| 对比 RP 的比值 (95% CI) | -2.87 (-5.61,-0.12)* | |
| 靶关节出血,经治疗 | ||
| ABR,基于模型 (95% CI) | 3.36 (1.59, 5.14) | 2.51 (1.25, 3.76) |
| 对比 RP 的比值 (95% CI) | -0.86 (-2.41, 0.70)* | |
•方案规定的非劣效性标准(该差异的 95% CI 上限)为:经治疗出血、自发性出血和关节出血为 2.5;靶关节出血为 1.2;总出血为 2.9
•ABR 的均值估计值、差异和置信区间 (CI)来自负二项回归模型。
根据 ISTH标准调整出血定义:经治疗出血 = 接受 FVIII 或 FIX 治疗的出血;
•总出血量 = 接受或未接受FVIII 或 FIX 治疗的出血
ABR = 年出血率;CI = 置信区间;RP =常规预防治疗
声明
关于马塔西单抗更多详细信息请参见完整版药品说明书。
辉瑞公司无法针对个体患者不良事件的诊断和处理提出任何临床建议,应当由临床医生根据患者的具体请况作出合理判断和采取相应措施。
在入组 BASIS研究的无抑制物的重型(凝血因子活性 <1%)血友病A或血友病B的青少年和成人患者中评价了本品的安全性。表 3总结了接受本品常规预防治疗的患者中观察到的不良反应(发生率≥3%)。1
表3.接受本品治疗的患者*报告的不良反应(发生率≥3%)1
| 不良反应 | 患者例数(N=116) |
|---|---|
| 注射部位反应 | 11 (9%) |
| 头痛 | 8 (7%) |
| 瘙痒 | 4 (3%) |
1.*在BASIS 试验为期 12 个月的研究药物治疗期
特定不良反应描述1
注射部位反应1
共计 11.2% 接受本品治疗的患者报告了注射部位反应。在本品临床研究中观察到的大部分注射部位反应均为一过性,严重程度报告为轻度至中度。未发生导致剂量调整或停药的注射部位反应。注射部位反应包括注射部位瘀青、注射部位红斑、注射部位血肿、注射部位硬结、注射部位水肿、注射部位疼痛、注射部位瘙痒和注射部位肿胀。
皮疹1
在不伴抑制物人群中,0.9% 的患者报告了非严重皮疹(1 级)。
血栓栓塞事件1
去除组织因子途径抑制物(TFPI)抑制可能会增加患者血液凝集的可能性,并加大患者个人的多因素血栓栓塞事件风险。以下患者使用本品可能会增加发生血栓栓塞事件的风险:
- 有冠状动脉疾病、静脉或动脉血栓形成或缺血性疾病史的患者;
- 当前患有伴组织因子表达增加的急性重症(例如严重感染、脓毒症、外伤、碾压伤、癌症)的患者。
尚未在既往有血栓栓塞事件史的患者中进行本品研究(参见说明书中【临床药理】),且在急性重症患者方面的经验有限。
其他抗组织因子途径抑制物(抗 TFPI)产品的使用与在相近时间点接受其他止血药(即旁路制剂)的患者发生血栓栓塞并发症有关。临床研究中未发现接受本品常规预防治疗的血友病患者发生血栓栓塞事件。接受本品治疗的患者可安全使用因子VIII和因子IX产品治疗突破性出血。如果接受本品常规预防治疗的患者需要使用因子VIII或因子IX产品时,建议根据产品说明书采用因子VIII或因子IX产品的最低有效剂量。
有血栓栓塞事件史或当前发生急性重症的患者如要使用本品,应考虑其获益与风险。对于有风险的患者,应监测其是否存在血栓形成的早期体征,并根据当前建议和标准治疗采取血栓栓塞预防措施。如果诊断结果表明发生血栓栓塞,应中断本品常规预防治疗,并针对临床指征进行管理。
超敏反应1
在接受本品治疗的患者中发生皮疹和瘙痒皮肤反应,这可能反映发生了药物超敏反应(参见说明书中【不良反应】)。如果接受本品治疗的患者进展为重度超敏反应,建议患者停用本品并立即就医。
临床研究
2025《Blood》
Marstacimab prophylaxis in hemophilia A/B without inhibitors: Results from the Phase 3 BASIS Trial
2023《British Journal of Haematology》
Long‑term safety and efficacy of the anti‑tissue factor pathway inhibitor marstacimab in participants with severe haemophilia: Phase II study results
2023《Haemophilia》
Safety, tolerability, pharmacokinetics and pharmacodynamics of a single dose ofmarstacimab in Chinese participants with severe haemophilia
2022《British Journal of Haematology》
A phase 1b/2 clinical study of marstacimab, targeting human tissue factor pathway inhibitor, in haemophilia
2018《Journal of Thrombosis and Haemostasis》
A first‑in‑human study of the safety, tolerability, pharmacokinetics and pharmacodynamics of PF‑06741086, an anti‑tissue factor pathway inhibitor mAb, in healthy volunteers
非临床研究
2023《The AAPS Journal》
Evolution of Antidrug Antibody Assays During the Development of Anti‑Tissue Factor Pathway Inhibitor Monoclonal Antibody Marstacimab
2022《Research and Practice in Thrombosis and Haemostasis》
2019《Haemophilia》
2019《The AAPS Journal》
2018《Journal of Pharmaceutical Sciences》
2025 EAHAD会议
2025 ISTH 会议
2025ASH会议
如需研究文献原文,请您联系辉瑞医学信息部: [email protected], 或通过辉瑞医学信息网站在线提问获取。
请注意:我们不建议超出国家药品监督管理局批准的药品说明书的应用或未在中国(不含港澳台)上市药品的应用。如我们所提供的文献信息及指南共识涉及该等内容,系出于传递科学知识的需要,不应视为对未在中国(不含港澳台)上市药品或已在中国上市但超出国家药品监督管理局批准的药品说明书的药品适应症/用法的推广。
Callaghan MU, Sidonio R, Pipe SW. Novel therapeutics for hemophilia and other bleeding disorders. Blood, 2018;132(1):23-30.
Cardinal M, Kantaridis C, Zhu T, et al. A first-in-human study of the safety, tolerability, pharmacokinetics and pharmacodynamics of PF-06741086, an anti-tissue factor pathway inhibitor mAb, in healthy volunteers. J Thromb Haemost, 2018;16(9):1722-1731.
Smith SA, Travers RJ, Morrissey JH. How it all starts: initiation of the clotting cascade. Crit Rev Biochem Mol Biol, 2015;50(4):326-336.
Ragni MV. Novel alternate hemostatic agents for patients with inhibitors: beyond bypass therapy. Hematology Am Soc Hematol Educ Program, 2017;2017(1):605-609.
Lwaleed BA, Bass PS. Tissue factor pathway inhibitor: structure, biology and involvement in disease. J Pathol, 2006;208(3):327-339.
Ellsworth P, Ma A. Factor-mimetic and rebalancing therapies in hemophilia A and B: the end of factor concentrates? Hematology Am Soc Hematol Educ Program, 2021;2021(1):219-225.
Jasuja R, Barakat A, Murphy JE, et al. An antibody to tissue factor pathway inhibitor (TFPI) restores hemostasis after the onset of bleeding in hemophilia A mouse injury models. Blood, 2016;128(22):3761.



