请仔细阅读说明书并在医师或药师指导下使用
本品适用于患有以下疾病且体重 ≥ 35 kg的 12 岁及以上儿童和成人患者的常规预防治疗,以防止出血或降低出血发作的频率:
不存在凝血因子VIII抑制物的重型A型血友病(先天性凝血因子VIII缺乏,FVIII<1%)或
不存在凝血因子IX抑制物的重型B型血友病(先天性凝血因子IX缺乏,FIX<1%)。
预充式注射器(PFS)装:150 mg(1 mL)/ 支
1. 推荐剂量仅供皮下给药,首次本品治疗时患者应处在无出血状态。如完整剂量需多次注射,则每次注射时换用不同的注射部位。
本品用于体重 ≥ 35 kg 的 12 岁及以上患者的推荐剂量如下:
负荷剂量
皮下注射 300 mg(分 2 次不同部位注射,每次 150 mg)
维持剂量
负荷剂量给药后 1 周,开始维持剂量给药,每周一次,即每周在同一天的任意时间皮下注射 150 mg。
治疗期间的剂量调整
经专业医护人员判定当前剂量不足以控制出血事件时,可考虑将体重 ≥50 kg 的患者的剂量调整为每周皮下注射 300 mg(关键性 III 期研究中有12%患者在6个月后需要剂量调整至300mg;参见【临床试验】)。尚未充分确定本品在每周 300 mg 以上剂量下的安全性和有效性。
药物漏用
对于接受维持剂量 150 mg 治疗的患者:
如果漏用一剂,应在下次计划用药日前尽快补用,然后恢复每周常规 150 mg 皮下给药方案(采用与漏用剂量前相同的给药方案或是基于漏用剂量给药日期制定新的给药方案)。
如果补用漏用剂量时已超过末次给药 13 天,则应通过皮下注射给予负荷剂量 300 mg,随后恢复每周一次 150 mg 的皮下注射。
对于接受维持剂量 300 mg 治疗的患者:
如果漏服一剂或多剂,应尽快补用,然后恢复 300 mg 每周一次皮下给药方案(采用与漏用剂量前相同的给药方案或是基于漏用剂量给药日期制定新的给药方案)。
改为马塔西单抗注射液
从因子替代的常规预防治疗改为本品治疗:在停用凝血因子后可随时启用本品。
尚无患者从非因子类血友病药品改为本品治疗的数据。
突破性出血的治疗指南
接受本品治疗的患者发生突破性出血时可使用因子 VIII 和因子 IX 产品进行治疗。不得追加本品剂量来治疗突破性出血事件(参见【注意事项】)。
2. 准备和给药
- 本品应在专业医护人员的指导下使用。如果经专业医护人员认可,且患者或其护理者已接受适当的皮下注射技术培训,患者可自行注射或由其护理者注射本品。
- 有关完整的注射前准备和给药说明,请参阅使用说明。
- 皮下给药之前,从冰箱中取出本品,置于室温15至30分钟,避免阳光直射。请勿使用热水或微波炉等其他方法加热本品。从冰箱中取出本品后,应在7 天内使用或丢弃(参见【贮藏】)。
- 本品通过皮下注射给药,每周一次,可在一天中任意时间注射,可选择腹部或大腿进行注射。必要时,也可选择其他注射部位。本品在上臂(仅限预充式注射器)给药只能由护理者或医疗保健专业人员进行。本品不可在骨骼区域或皮肤瘀伤、发红、压痛或硬结区域,或有疤痕或妊娠纹的区域进行注射。本品不得静脉注射。每次注射,应轮换使用不同注射部位。
- 在使用本品治疗期间,最好在不同的部位注射其他皮下给药药品。
- 在给药前应目视检查有无不溶性微粒或变色情况。本品为澄清、无色至淡黄色溶液。如果溶液混浊、呈深黄色或含有薄片或颗粒,请勿使用。
3. 手术和其他治疗干预时暂时停用
围手术期管理
尚未在重大手术环境中评估本品。在临床研究中,曾有患者接受小型外科手术,但手术期间未停止使用本品的常规预防治疗。
重大手术前,停用本品并根据当地标准治疗启用凝血因子进行治疗,同时采取措施管理围手术期可能增加的静脉血栓形成风险。对于接受重大手术的血友病患者的剂量指南,请查阅凝血因子的产品信息。恢复本品治疗前应考虑患者的整体临床情况,包括是否存在术后血栓栓塞的风险因素、其他止血产品和其他伴随用药的使用情况(参见【用法用量】- 药物漏用)。
急性重症患者的管理
在急性重症患者中使用本品的经验有限。本品使用期间若出现以下情况,如发生急性重症(如严重感染、脓毒症、外伤),期间凝血活化可能增加,同时专业医护人员认为这可能会增加本品给药相关风险,应考虑暂时停用本品。应按照当地标准治疗对急性重症的治疗情况进行管理,此时应根据使用本品的潜在风险权衡是否继续使用本品进行治疗。一旦患者达到了临床治愈,即可恢复本品治疗(参见【用法用量】- 药物漏用)。
4. 妊娠试验
在开始本品治疗前,确认有生育能力的女性未怀孕(参见【注意事项】和【孕妇及哺乳期妇女用药】)。
5. 特殊人群
肝功能不全
轻度肝功能不全患者无需进行剂量调整(参见【临床药理】)。目前尚未在中度或重度肝功能不全患者中进行本品研究。
肾功能不全
轻度肾功能不全患者无需进行剂量调整(参见【临床药理】)。目前尚未在中度或重度肾功能不全患者中进行本品研究。
老年人
65 岁以上患者无需进行剂量调整(参见【临床药理】)。
以下有临床意义的不良反应在说明书的其他部分进行描述:
- 血栓栓塞事件(参见【注意事项】)
- 超敏反应(参见【注意事项】)
临床试验经验
由于各临床试验间的试验条件差异很大,一种药物在临床试验中观察到的不良反应发生率不能直接和其他药物在临床试验中的不良反应发生率相比较,且有可能没有反映临床实践中的不良反应发生率。
在入组 BASIS 研究的无抑制物的重型(凝血因子活性 <1%)血友病A或血友病B的青少年和成人患者中评价了本品的安全性(参见【临床试验】)。患者(N=116)接受本品常规预防治疗,初始负荷剂量为 300 mg,随后从第 8 天开始接受每周一次 150 mg 皮下给药。在接受本品治疗的患者中,97% 患者的暴露持续时间为 6 个月或以上,75% 患者的暴露持续时间为至少 1 年。
1 例患者出现外周肿胀严重不良反应。
表 1 总结了接受本品常规预防治疗的患者中观察到的不良反应(发生率≥3%)。
表 1. 接受本品治疗的患者*报告的不良反应(发生率≥3%)
| 不良反应 | 患者例数(N=116) |
|---|---|
| 注射部位反应 | 11 (9%) |
| 头痛 | 8 (7%) |
| 瘙痒 | 4 (3%) |
1 *在 BASIS 试验为期 12 个月的研究药物治疗期
特定不良反应描述
注射部位反应
共计 11.2% 接受本品治疗的患者报告了注射部位反应。在本品临床研究中观察到的大部分注射部位反应均为一过性,严重程度报告为轻度至中度。未发生导致剂量调整或停药的注射部位反应。注射部位反应包括注射部位瘀青、注射部位红斑、注射部位血肿、注射部位硬结、注射部位水肿、注射部位疼痛、注射部位瘙痒和注射部位肿胀。
皮疹
在不伴抑制物人群中,0.9% 的患者报告了非严重皮疹(1 级)。
儿童人群
研究的儿童人群共包括 19 例青少年患者(12 至 < 18 岁)。本品的安全性特征在青少年和成人之间总体一致。
报告疑似不良反应
药品获得上市许可后,报告疑似不良反应非常重要。这样可继续监测药品的获益/风险平衡。专业保健医生应报告疑似不良反应。
免疫原性
观察到的抗药抗体的发生率很大程度上取决于分析方法的灵敏度和特异性。鉴于分析方法存在差异,无法将下述研究中抗药抗体(ADA)的发生率与其他研究(包括马塔西单抗的研究或其他马塔西单抗产品的研究)中ADA的发生率进行有意义的比较。
在BASIS研究的12个月研究药物治疗期,116例接受马塔西单抗治疗、ADA可评估的患者中,23例(19.8%)出现ADA。在 ADA 检测阳性的 23 例患者中,6 例患者 (26%) 产生了马塔西单抗的中和抗体 (NAb)。与整个治疗期间未产生抗马塔西单抗抗体的受试者相比,接受马塔西单抗治疗并产生抗马塔西单抗抗体的受试者的马塔西单抗稳态浓度降低,几何平均降低幅度为 24% 至 50%。
在 12 个月的治疗期间,未发现 ADA(包括 NAb)对马塔西单抗的安全性或有效性存在具有临床意义的影响。
无。
血栓栓塞事件
去除组织因子途径抑制物(TFPI)抑制可能会增加患者血液凝集的可能性,并加大患者个人的多因素血栓栓塞事件风险。以下患者使用本品可能会增加发生血栓栓塞事件的风险:
- 有冠状动脉疾病、静脉或动脉血栓形成或缺血性疾病史的患者;
- 当前患有伴组织因子表达增加的急性重症(例如严重感染、脓毒症、外伤、碾压伤、癌症)的患者。
尚未在既往有血栓栓塞事件史的患者中进行本品研究(参见【临床药理】),且在急性重症患者方面的经验有限。
其他抗组织因子途径抑制物(抗 TFPI)产品的使用与在相近时间点接受其他止血药(即旁路制剂)的患者发生血栓栓塞并发症有关。临床研究中未发现接受本品常规预防治疗的血友病患者发生血栓栓塞事件。接受本品治疗的患者可安全使用因子 VIII 和因子 IX 产品治疗突破性出血。如果接受本品常规预防治疗的患者需要使用因子 VIII 或因子 IX 产品时,建议根据产品说明书采用因子 VIII 或因子 IX 产品的最低有效剂量。
有血栓栓塞事件史或当前发生急性重症的患者如要使用本品,应考虑其获益与风险。对于有风险的患者,应监测其是否存在血栓形成的早期体征,并根据当前建议和标准治疗采取血栓栓塞预防措施。如果诊断结果表明发生血栓栓塞,应中断本品常规预防治疗,并针对临床指征进行管理。
突破性出血的治疗指南
接受本品治疗的患者发生突破性出血时可使用因子 VIII 和因子 IX 产品进行治疗。不得追加本品剂量来治疗突破性出血事件。必要时,专业医护人员应与患者和/或照护者讨论在接受本品常规预防治疗时使用凝血因子的剂量和时间表,包括使用尽可能低的有效剂量的凝血因子。请参阅所用凝血因子的产品信息。
超敏反应
在接受本品治疗的患者中发生皮疹和瘙痒皮肤反应,这可能反映发生了药物超敏反应(参见【不良反应】)。如果接受本品治疗的患者进展为重度超敏反应,建议患者停用本品并立即就医。
伴因子抑制物的患者
在一项针对未获批适应症的正在进行的临床研究中,接受本品治疗的伴抑制物血友病患者中,1 例 (2.9%) 患有重型血友病 B 且有外源因子 IX 过敏反应史的患者在治疗约 9 个月时发生了重度皮疹,该患者需要延长口服皮质类固醇缓解,并停止本品治疗。
本品对凝血检测结果的影响
本品治疗不会对包括活化部分凝血活酶时间 (aPTT) 和凝血酶原时间 (PT) 在内的标准凝血指标产生具有临床意义的影响。
辅料
聚山梨酯含量
本品含聚山梨酯 80。聚山梨酯 80 可能会引起超敏反应。
钠含量
1 mL 本品含有少于 1 mmol 钠 (23 mg),即基本上“无钠”。
妊娠
基于其作用机制,孕妇使用本品可能会对胎儿造成伤害(参见【临床药理】)。目前尚无关于孕妇使用本品的数据,无法评估药物相关的重大出生缺陷、流产或其他不良产妇或胎儿结局的风险。尚未对本品进行雌性动物生殖研究。尽管尚无关于本品的数据,但单克隆抗体可经主动转运穿过胎盘,因此本品可能会对胎儿造成伤害。
哺乳
关于本品是否可在人或动物乳汁中分泌,对母乳喂养孩子或乳汁分泌的影响,目前尚无相关数据。
已知人乳中存在内源性母体 IgG 和单克隆抗体。尚不清楚母乳喂养孩子中本品局部胃肠道暴露和有限的系统暴露带来的影响。
应考虑母乳喂养对发育和健康的益处,母亲对本品的临床需求以及本品或母体基础病症对母乳喂养婴儿的任何潜在不良影响。
避孕
建议有生育能力的女性患者在本品治疗期间和末次给药后后2个月内采取有效的避孕措施。
在开始本品治疗前,确认有生育能力女性的妊娠情况。
生育力
动物研究未显示对生育力的直接或间接有害影响(参见【药理毒理】)。目前尚无人类生育力相关数据。因此,尚不清楚本品对男性和女性生育力的影响。
已确定本品在12岁及以上不伴抑制物的血友病A或血友病B的儿童患者中减少出血发作或降低出血发作频率方面的安全性和有效性(参见【临床试验】)。一项开放、多中心 III 期研究中不伴抑制物的血友病患者(19例青少年和97例成人)的结果支持对该适应症使用本品。
尚未确定本品在12岁以下儿童患者中的安全性和有效性。
1 例 ≥ 65 岁的患者入组了无抑制物的A型或B型血友病的临床研究(参见【临床试验】)。本品的临床研究未纳入足够数量年龄≥ 65岁的患者,因此不能确定该人群对药物的反应是否与更年轻的患者不同。
尚未开展关于本品的药物相互作用的临床研究。
本品是一种单克隆抗体 (mAb),预计将通过分解代谢途径清除。因此,与通过非分解代谢途径清除的伴随药品的相互作用不太可能对其清除产生影响。此外,预计马塔西单抗等生物制剂不会对细胞色素P450 酶表达产生间接影响。
药效学
血友病患者使用本品可使总 TFPI (由游离 TFPI 和与马塔西单抗结合的 TFPI 组成)和凝血酶生成的下游生物标志物(如凝血酶原片段 1+2、凝血酶峰值和 D-二聚体)增加。在单次皮下注射后,观察到这些变化且持续了 7 天,并且在停药后可逆。
药代动力学
每周皮下注射一次 150 mg 马塔西单抗时,成人和体重 ≥35 kg 的青少年的平均估计马塔西单抗Cmin,ss 、Cmax,ss 和 Cavg,ss值见表 2。在 100 mg 至 450 mg(批准推荐剂量的 0.67 至 3 倍)剂量范围内,本品血浆浓度-时间曲线下面积 (AUC) 和血药峰浓度 (Cmax) 的增加比例大于剂量增加比例。
马塔西单抗的平均稳态蓄积比约为 4 至 5。预计本品将在约 60 天时达到稳态浓度,即每周一次给药的第 8 次或第 9 次皮下给药时。
表 2. 每周一次皮下注射150 mg(负荷剂量为 300 mg)马塔西单抗后的稳态血药浓度
| 参数 | 成人 | 青少年 |
|---|---|---|
| Cmin,ss (mcg/mL) | 13.7 (90.4%) | 27.3 (53.2%) |
| Cmax,ss (mcg/mL) | 17.9 (77.5%) | 34.7 (48.5%) |
| Cavg,ss (mcg/mL) | 16.5 (81.2%) | 32.1 (49.5%) |
• 数据以算术平均值(变异系数)表示。
• Cmin,ss = 稳态最小血药浓度; Cmax,ss = 稳态最大血药浓度; Cavg,ss = 稳态平均血药浓度
吸收
皮下给药后,马塔西单抗的生物利用度约为 71%。血友病患者多次皮下注射马塔西单抗,中位 Tmax 范围为 23 至 59 小时。马塔西单抗在手臂、大腿和腹部注射时,其生物利用度无临床意义的差异。
分布
马塔西单抗在血友病患者中的稳态表观分布容积为 8.6 L。
消除
马塔西单抗通过线性和非线性机制清除。马塔西单抗药代动力学呈非线性。这种非线性药代动力学行为是由形成 马塔西单抗/TFPI 复合物时发生的靶点介导的药物处置 (TMDD) 引起的。一旦靶点达到饱和,线性途径(即分解代谢)占主导地位。
基于群体药代动力学分析,预计 90% 的马塔西单抗将在末次给药后约 1 个月时被消除(50% 药物消除的中位时间约为 7 至 10 天)。
代谢
预计马塔西单抗以与内源性 IgG 相同的方式通过分解代谢途径代谢为小肽和氨基酸。
特殊人群
基于种族、血友病类型(A型和B型)、轻度肾功能不全eGFR 为 60-89 mL/min/1.73 m2)和轻度肝功能不全(总胆红素 >1× 至 ≤1.5× ULN),未观察到马塔西单抗药代动力学存在具有临床意义的差异。尚不清楚老年(>65 岁)、中度至重度肾功能不全 (eGFR <59 mL/min/1.73 m2) 和中度至重度肝功能不全(Child Pugh B 级和 C 级)对马塔西单抗药代动力学的影响。
体重
体重是影响马塔西单抗药代动力学的显著协变量。在 35-120 kg 体重范围内,马塔西单抗暴露量显示出随体重降低而增加的趋势。然而,无需根据体重调整剂量。
儿童患者
青少年(12 至 <18 岁)的马塔西单抗清除率 (CL) 与成人(18 岁及以上)相比低 29%。按体重校正后,未观察到青少年的马塔西单抗CL(L/hr/kg) 与成人存在具有临床意义的差异。
中国人群
一项I 期研究B7841010在不伴FVIII或FIX抑制物的重型血友病A或血友病B(分别为FVIII 或FIX 活性< 1%)的中国成人男性受试者(n=6)中评价了本品单剂皮下注射给药300 mg的药代动力学特征。该研究中所观察到的本品在中国患者中的药代动力学特征与非中国受试者中的特征基本相似。
不伴FVIII抑制物的血友病A或不伴FIX抑制物的血友病B
在入组 BASIS 研究 (NCT03938792)(一项开放性、多中心、两阶段研究)的 116 例无 FVIII 抑制物的重度血友病A或无 FIX 抑制物的重度血友病B成人和儿童患者(年龄 ≥12 岁且体重 ≥35 kg)中确定了本品的有效性。重型血友病定义为凝血因子活性 <1%。本研究排除了有冠状动脉疾病、静脉或动脉血栓形成或缺血性疾病史的患者。
筛选后,患者进入 6 个月的观察期,并根据入组研究前接受的因子替代的常规预防治疗入组两个队列:按需治疗队列或常规预防治疗队列。完成观察期的患者将接受 12 个月的本品治疗。观察期内,116 例接受本品治疗的患者中,有 33 例患者入组按需治疗队列,83 例患者入组 FVIII 或 FIX 常规预防治疗队列。完成 12 个月 BASIS 研究的患者有资格入组开放性扩展研究 (NCT05145127)。
患者接受本品初始剂量 300 mg(负荷剂量),随后接受维持剂量 150 mg,每周一次,持续治疗 12 个月。对于体重 ≥50 kg 且发生 2 次或以上突破性出血的患者,可以在 6 个月治疗后将本品剂量递增至 300 mg 每周一次。有 14 例 (12%) 接受了剂量递增。
在观察期按需治疗和常规预防治疗队列中经治疗出血的平均年出血率 (ABR)分别为38和7.85。按需治疗队列中的所有患者在研究开始时均有一个或多个靶关节,36%的患者在研究开始时有3个或更多个靶关节。在常规预防治疗队列中,57%的患者在研究开始时有一个或多个靶关节,16%的患者在研究开始时有3个或更多个靶关节。
基于治疗期本品经治疗出血的 ABR 与观察期的 ABR 的比较评估每个队列中本品的有效性。本研究的其他目的包括评估本品常规预防治疗对自发性出血、关节出血、靶关节出血和总出血发生率的影响。
在 BASIS 研究中接受本品治疗的 116 例患者中,平均年龄为 32 岁(范围 13-66 岁);19 例患者年龄为 12 至 <18 岁,均为男性。56 例患者为白人,58 例患者为亚裔,1 例患者为黑人或非裔美国人,1 例患者的种族信息未报告;12 例患者为西班牙裔或拉丁裔,104 例患者为非西班牙裔或拉丁裔。患者人群包括 91 例A型血友病患者和 25 例B型血友病患者。
在观察期接受因子替代的按需治疗的患者
表 3 列出了本品常规预防治疗与因子替代的按需治疗的疗效比较结果。本品常规预防治疗在经治疗出血、自发性出血、关节出血、总出血和靶关节出血的发生率方面优于因子替代的按需治疗。
表 3. 在 ≥12 岁不伴因子VIII或因子IX抑制物的患者中,本品常规预防治疗与因子替代的按需治疗的年出血率比较
| 按检验层级顺序列出的终点 | 6 个月观察期接受因子替代的按需治疗 (N = 33) | 12 个月研究药物治疗期的马塔西单抗常规预防治疗 (N = 33) |
|---|---|---|
| 经治疗出血(主要) | ||
| ABR,基于模型 (95% CI) | 38.00 (31.03, 46.54) | 3.18 (2.09, 4.85) |
| 对比OD的比值 (95% CI) p 值 | 0.084 (0.059, 0.119) < 0.0001 | |
| 自发性出血,经治疗 | ||
| ABR,基于模型 (95% CI) | 30.93 (24.12, 39.67) | 2.44 (1.61, 3.69) |
| 对比OD的比值 (95% CI) p 值 | 0.079 (0.054, 0.114) < 0.0001 | |
| 关节出血,经治疗 | ||
| ABR,基于模型 (95% CI) | 32.86 (26.15, 41.29) | 2.83 (1.81, 4.44) |
| 对比OD的比值 (95% CI) p 值 | 0.086 (0.059, 0.125) < 0.0001 | |
| 总出血,经治疗和未经治疗 | ||
| ABR,基于模型 (95% CI) | 47.76 (39.60, 57.60) | 7.39 (5.08, 10.74) |
| 对比OD的比值 (95% CI) p 值 | 0.155 (0.116, 0.207) < 0.0001 | |
| 靶关节出血,经治疗 | ||
| ABR,基于模型 (95% CI) | 23.18 (17.20, 31.24) | 1.84 (1.06, 3.17) |
| 对比OD的比值 (95% CI) p 值 | 0.079 (0.051, 0.124) < 0.0001 | |
• p 值是基于比值=0.5 的零假设。
• ABR 的均值估计值、比值和置信区间 (CI) 来自负二项回归模型。
根据 ISTH 标准调整出血定义:经治疗出血 = 接受 FVIII 或 FIX 治疗的出血;
• 总出血量 = 接受或未接受 FVIII 或 FIX 治疗的出血
• ABR = 年出血率;CI = 置信区间;OD = 按需治疗
接受因子替代的常规预防治疗的患者
表 4 列出了本品常规预防治疗与因子替代的常规预防治疗的疗效比较结果。通过评估经治疗出血的ABR以及自发性出血、关节出血、靶关节出血和总出血的发生率,证明本品常规预防治疗非劣效于因子替代的常规预防治疗。
表 4. 在 ≥12 岁不伴因子VIII或因子IX抑制物的患者中,本品常规预防治疗与既往因子替代的常规预防治疗的年出血率比较
| 按检验层级顺序列出的终点 | 6 个月观察期间因子替代的常规预防治疗 (N = 83) | 12 个月研究药物治疗期的马塔西单抗常规预防治疗 (N = 83) |
|---|---|---|
| 经治疗出血(主要) | ||
| ABR,基于模型 (95% CI) | 7.85 (5.09, 10.61) | 5.08 (3.40, 6.77) |
| 与RP的差异 (95% CI) | -2.77(-5.37,-0.16)* | |
| 自发性出血,经治疗 | ||
| ABR,基于模型 (95% CI) | 5.86 (3.54, 8.19) | 3.78 (2.25, 5.31) |
| 与RP的差异 (95% CI) | -2.09 (-4.23, 0.06) | |
| 关节出血,经治疗 | ||
| ABR,基于模型 (95% CI) | 5.66 (3.33, 7.98) | 4.13 (2.59, 5.67) |
| 与RP的差异 (95% CI) | -1.53 (-3.70, 0.64)* | |
| 总出血,经治疗和未经治疗 | ||
| ABR,基于模型 (95% CI) | 8.84 (5.97, 11.72) | 5.97 (4.13, 7.81) |
| 与RP的差异 (95% CI) | -2.87(-5.61,-0.12)* | |
| 靶关节出血,经治疗 | ||
| ABR,基于模型 (95% CI) | 3.36 (1.59, 5.14) | 2.51 (1.25, 3.76) |
| 与RP的差异 (95% CI) | -0.86 (-2.41, 0.70)* | |
• 方案规定的非劣效性标准(该差异的 95% CI 上限)为:经治疗出血、自发性出血和关节出血为 2.5;靶关节出血为 1.2;总出血为 2.9。
• ABR 的均值估计值、差异和置信区间 (CI) 来自负二项回归模型。
根据 ISTH 标准调整出血定义:
经治疗出血 = 接受 FVIII 或 FIX 治疗的出血;
• 总出血量 = 接受或未接受 FVIII 或 FIX 治疗的出血
ABR = 年出血率;CI = 置信区间;RP =常规预防治疗
药理作用
马塔西单抗是一种直接靶向组织因子途径抑制物(TFPI)的Kunitz结构域2 (K2)的人源单克隆IgG1抗体,可中和TFPI活性并增强凝血功能。TFPI是外源性凝血级联反应的主要抑制物,通过使活化凝血因子Ⅹa(FⅩa)/活化凝血因子Ⅶa(FⅦa)/组织因子(TF)复合物的蛋白酶功能失活,对外源性凝血途径中的凝血酶生成起到负调节作用。TFPI通过Kunitz结构域2(K2)与因子Ⅹa的活性位点结合并抑制其活性。
毒理研究
遗传毒性
本品尚未开展遗传毒性试验。
生殖毒性
雄性大鼠生育力与早期胚胎发育试验中,雄性大鼠于交配前至少4周和交配期间每周一次静脉注射马塔西单抗达1000 mg/kg/次[以AUC计,约为人临床剂量(每周300mg,皮下注射)下暴露量的212倍],未见对生育力的不良影响。在大鼠6个月和食蟹猴3个月重复给药毒性试验中,分别每周一次静脉注射给药马塔西单抗1000和500 mg/kg(以AUC计,分别约为人临床剂量下暴露量的201倍和219倍),未见对雌雄动物生殖器官的不良影响。
致癌性
本品尚未开展致癌性试验。
- 于2℃ 至8℃下,在原纸盒中保存以避光。
- 必要时,可在原纸盒中于室温(最高 30℃)下储存一次,最多储存 7 天。一旦在室温下储存,请勿送回冰箱,并在7天后丢弃。
- 请勿冷冻。
- 请勿振摇。
本品为预充式注射器包装。
每盒装有一支单剂量预充式注射器,包含柱塞和带针帽的不锈钢针头。
36个月。
JS20250043
国药准字SJ20250026
名 称:Pfizer Inc.
注册地址:66 Hudson Boulevard East, New York, NY 10001 United States of America
企业名称:Pfizer Manufacturing Belgium NV
生产地址:Rijksweg 12, Puurs-Sint-Amands 2870 BELGIUM
名称:辉瑞投资有限公司
地址:上海市南京西路1168号中信泰富广场36层
联系方式:400 910 0055
本使用说明包含了如何注射马塔西单抗注射液的信息。
在使用马塔西单抗预充式注射器之前以及每次获得续药处方时,请仔细阅读本使用说明,说明中可能会有新信息。
首次使用前,专业医护人员应向您或您的护理者演示如何正确进行注射前准备和注射本品。在给您演示如何注射本品之前,不要给自己或他人注射。
注射本品前您需要知道的重要信息
- 每支马塔西单抗预充式注射器均为单剂量预充式注射器(在本使用说明中简称为“注射器”)。马塔西单抗预充式注射器装有150 mg皮下注射用马塔西单抗。
- 请勿静脉注射本品。
- 您可以提前在日历上做标记,以帮助您记住何时注射本品。如果您或您的护理者对本品的正确注射方法有任何疑问,请致电专业医护人员。
- 使用本品时需严格遵医嘱。
- 本品并非由天然橡胶乳胶制成。
如何储存
- 将本品储存在 2℃ 至 8℃ 的冰箱中。
- 将本品储存在原纸盒中以避光。
- 必要时,可在原纸盒中于室温(最高 30℃)下储存1次,最多储存7天。本品经室温下储存后,不得送回冰箱。
- 如果本品从冰箱中取出超过 7 天,应丢弃(弃置)。
- 请勿冷冻本品。
- 请勿振摇本品。
- 请勿在马塔西单抗预充式注射器上印刷的有效期(EXP)后使用本品。
- 将本品和所有其他药物置于儿童接触不到的地方。
本品注射所需的用品
取以下用品置于干净平面上:
纸盒中含有的用品:
- 1 支马塔西单抗预充式注射器。
纸盒中不含的用品:
- 1 个酒精棉签。
- 1 个棉球或纱布垫。
- 1 个锐器处置容器,用于弃置注射器(请参阅“步骤 11 – 注射器弃置”和“注射器安全处置”须知部分)。
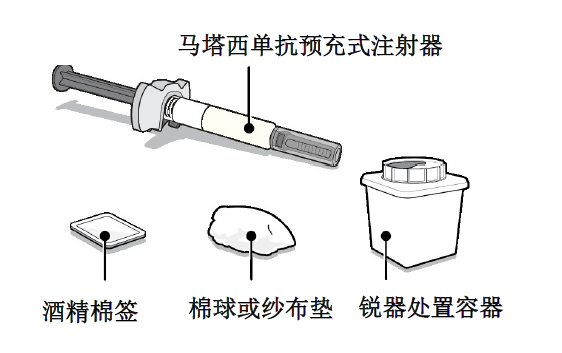
马塔西单抗预充式注射器
始终握住本品预充式注射器针筒,以防止损坏。
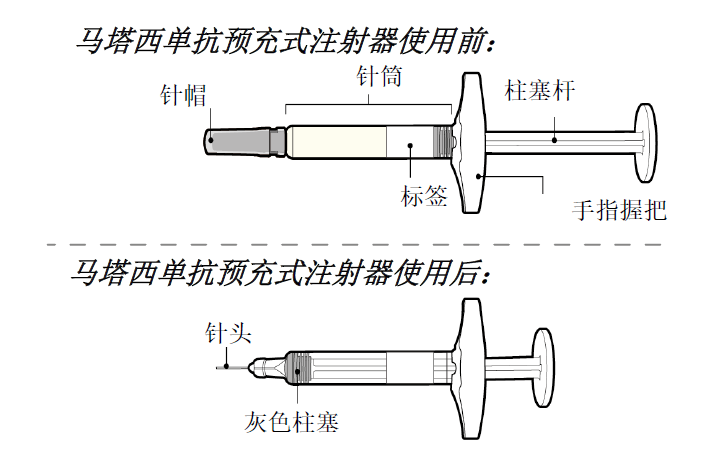
本品注射准备步骤:
步骤 1 - 准备工作
- 从纸盒中取出注射器,同时避免阳光直射。
- 确保在纸盒和注射器标签上印有商品名称。
- 检查注射器是否有可见损坏,如裂纹或泄漏。
- 洗手并擦干。
- 在准备注射之前,请勿取下针帽。
- 如果注射器损坏,或者注射器或装有注射器的纸盒掉落,请丢弃(弃置)。
- 在以下情况下请勿使用注射器:
○ 注射器储存期间受到阳光直射。但注射准备前和注射期间本品可暴露于室内光照。
○ 已冷冻或解冻或从冰箱中取出超过 7 天。
注:为了提高注射的舒适度,等待约 15 至 30 分钟,让纸盒中的注射器升温至室温,同时避免阳光直射。
请勿使用其他方法加热注射器,如请勿在微波炉或热水中加热注射器。
步骤 2 - 检查有效期
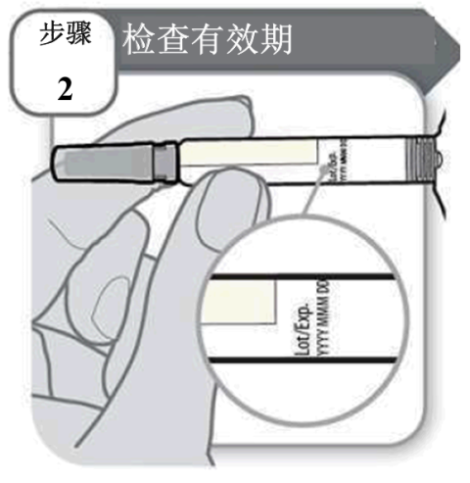
- 检查注射器标签上印刷的有效期。
- 请勿在超过有效期后使用。
步骤 3:检查药物
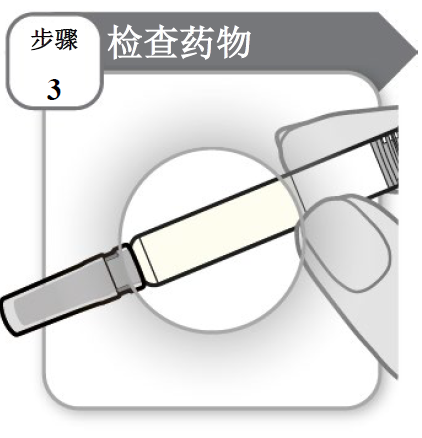
- 微微前后倾侧注射器。
- 仔细观察注射器里的药液。
○ 药液应澄清,无色至淡黄色。
○ 如果药液混浊、呈深黄色或含有薄片或颗粒,请勿使用注射器。
注:注射器中出现气泡属于正常现象。
如果您对本品有任何疑问,请联系您的专业医护人员。
步骤 4:选择并清洁您的注射部位
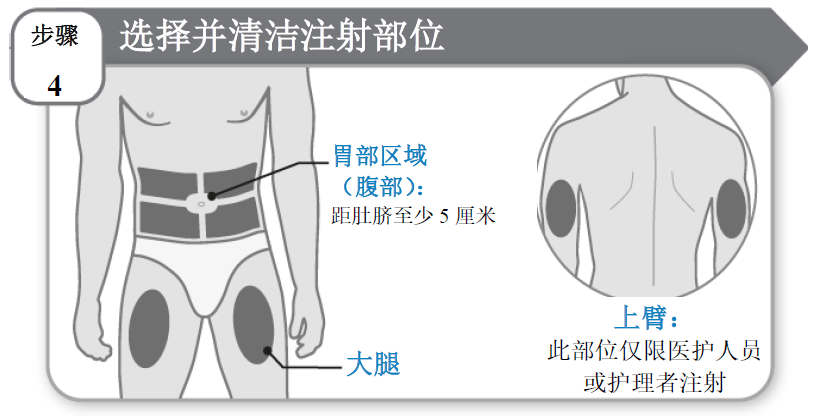
- 除非专业医护人员建议使用其他部位,应选择胃部区域(腹部)或大腿作为注射部位。本品也可在您的上臂注射,该注射操作仅限专业医护人员或护理者。距肚脐至少5厘米。
- 每次给自己注射本品时,均需改换(轮换)注射部位并远离皮下注射的任何其他药物。您可以选择身体的同一区域进行注射,但务必在该区域选择不同的注射部位。
- 用肥皂和水清洁注射部位,用酒精棉签进行清洁。
- 等待注射部位风干。请勿触碰已清洁的注射部位或向该部位扇风或吹气。
- 请勿将本品注射到骨骼区域或皮肤上瘀伤、发红、疼痛(压痛)或硬结区域。避免注射到有疤痕或妊娠纹的区域。
- 请勿静脉注射本品。
- 请勿隔着衣物注射本品。
步骤 5 - 取下针帽
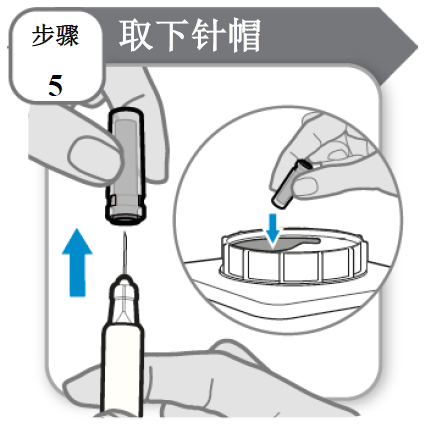
- 握住注射器针筒。
- 沿竖直方向小心地取下针帽。
- 立即将针帽放入锐器处置容器中。您不再需要它。
- 请勿触摸针头或让其接触任何表面。
注:针尖上有几滴药液是正常现象。
注意:请小心操作注射器,避免被针头意外刺伤。
注射本品
步骤 6 - 插入针头
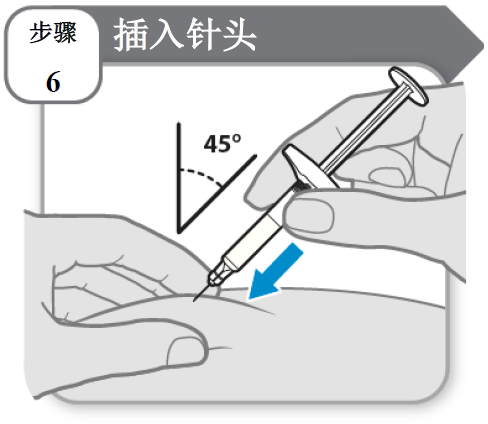
- 用拇指和其他手指捏紧已清洁的皮肤,让皮肤表面绷紧。
- 如图所示,以 45 度角将针头完全插入皮肤中。插入针头时,请勿握住或推动柱塞。
在整个注射过程中保持捏紧皮肤不放松。
注意:如果您将针头插入皮肤后想要改变注射位置,则需要丢弃(弃置)该注射器并换用新的马塔西单抗预充式注射器。
步骤 7 - 注射药物
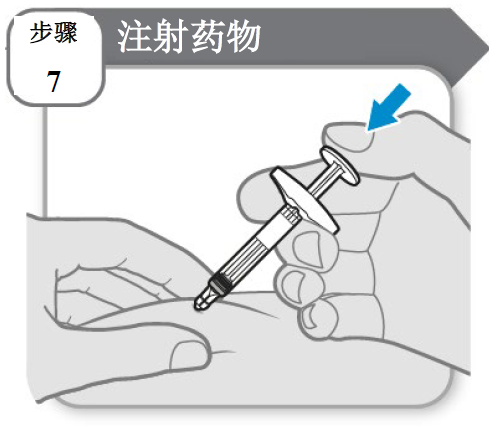
- 通过轻轻以相同力度向下推动柱塞杆缓慢注射所有本品,直至针筒排空。
注:待柱塞杆完全推下后缓慢数到 5 再将针头从皮肤拔出。
步骤 8 - 拔出针头
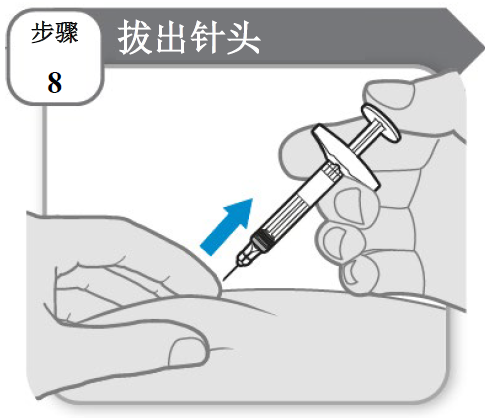
- 保持与插入时相同的角度,将针头和注射器从皮肤中拔出。
注:如果在皮肤上看到一小滴药液,请在下一次注射时多等一会儿再拔出针头。
步骤 9 - 检查注射器
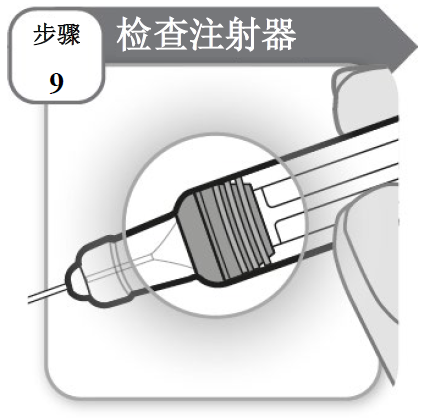
- 检查注射器,确保灰色柱塞位于所示位置。
如果灰色柱塞不在所示位置,则表示您未获得全剂量给药。请致电您的专业医护人员寻求帮助。
不得重新插入针头。
请勿另行注射。
步骤 10 - 注射后处理
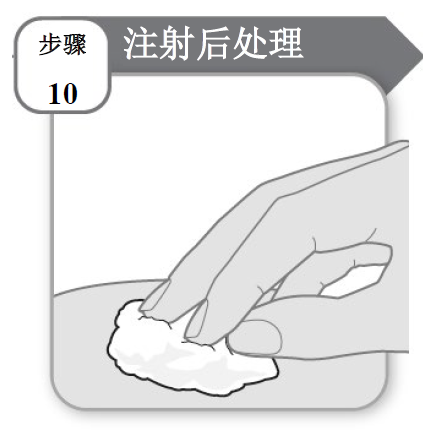
- 如果您看到一滴血,请用干净的棉球或纱布垫轻轻按压注射部位几秒钟。
- 请勿揉搓该区域。
注:如果出血不止,联系您的专业医护人员。
注:如果您的处方剂量要求注射 2 次本品,则重复步骤 1-10。每次给自己注射本品时,需改换(轮换)注射部位。您可以选择在相同的身体区域进行注射,但务必要选择该区域内不同的部位。
步骤 11 - 弃置
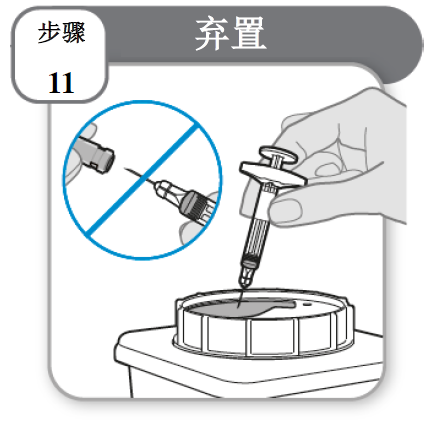
- 注射器使用后应立即放入锐器处置容器中。
不得重新盖上针帽。
- 请勿将注射器丢弃(弃置)到生活垃圾中。
注:如果您没有锐器处置容器,请参阅“注射器安全处置”须知部分。
注射器安全处置
- 务必要将注射器丢弃(弃置)到锐器处置容器中。请勿将注射器丢弃到生活垃圾中。
- 如果您没有锐器处置容器,您可以使用满足以下要求的家用容器:
○ 该容器由重型塑料制成,
○ 可用紧密贴合、防刺穿的盖子盖严,确保尖锐物不会从中掉出,
○ 使用时直立且稳定,
○ 防漏,
○ 贴有适当标识,警告容器内有危险废弃物。 - 请勿回收利用已用过的锐器处置容器。
2025年11月18日



