本品适用于成人偏头痛的急性治疗(有或无先兆)。1
一般人群用法用量
(1)用量1
- 本品推荐剂量为每次口服75 mg,按需服药。每日不超过一次。
- 尚未确定在30天内使用超过18次的安全性。
(2)用法1,2
- 本品推荐剂量为每次口服75 mg,按需服药。每日不超过一次。
- 图片说明:
 |
|
 |
|
- 视频说明:
肾功能损害人群用法用量
- 轻度、中度或重度肾功能损害患者无需调整用药剂量。1
- 重度肾功能损害患者频繁使用本品时应谨慎。1
- 终末期肾病(肌酐清除率[CLcr]<15 mL/min)患者应避免使用瑞美吉泮。1
- 一项临床研究中,分别将轻度(CLcr 60-89 mL/min)、中度(CLcr 30-59 mL/min)和重度(CLcr 15-29 mL/min)肾功能损害受试者与汇总的健康对照受试者中瑞美吉泮的药代动力学数据进行了比较,结果显示75 mg单次给药后,在轻、中度肾功能损害受试者中,总瑞美吉泮的暴露量(血浆浓度时间曲线下面积[AUC])增加不到50%。在重度肾功能损害受试者中,未结合瑞美吉泮的暴露量(AUC)是健康受试者的2.57倍。尚未在终末期肾病(CLcr<15 mL/min)患者中进行研究。1
肝功能损害人群用法用量
- 轻度(Child-Pugh A)或中度(Child-Pugh B)肝功能损害患者无需调整剂量。1
- 重度(Child-Pugh C)肝功能损害患者应避免使用瑞美吉泮。重度肝功能损害受试者的瑞美吉泮血浆浓度(未结合瑞美吉泮的血浆浓度时间曲线下面积[AUC])显著增高。1
- 一项临床研究比较了轻度、中度和重度肝功能损害受试者与各组相匹配的健康对照受试者中瑞美吉泮的药代动力学数据,结果表明与肝功能正常的健康受试者相比,重度肝功能损害受试者接受瑞美吉泮75 mg单次给药后的暴露量(未结合AUC)是健康受试者的3.89倍。1
本品用于偏头痛急性治疗时最常见的不良反应为恶心(1.2%),多数严重程度为轻或中度。接受治疗的患者中超敏反应(包括呼吸困难和严重皮疹)的发生率低于1%。1
下表按系统器官分类列出的不良反应,对每种药物不良反应的发生率进行分类:十分常见(≥1/10);常见(≥1/100 至<1/10);偶见(≥1/1,000 至<1/100);罕见(≥1/10,000 至<1/1,000);十分罕见(<1/10,000)。
表1 不良反应种类和频率1
| 系统器官分类 | 不良反应 | 发生率 |
|---|---|---|
| 免疫系统疾病 | 超敏反应,包括呼吸困难和严重皮疹 | 偶见 |
| 胃肠系统疾病 | 恶心 | 常见 |
在临床研究接受治疗的患者中,超敏反应(包括呼吸困难和皮疹)的发生率低于1%,超敏反应(包括严重超敏反应)可发生在给药后数天,也发生过迟发型严重超敏反应。如果发生超敏反应,应停用瑞美吉泮并给予适当治疗。1
在两项为期1年、开放标签的延伸试验中评估了瑞美吉泮的长期安全性;1662例患者接受了至少6个月的瑞美吉泮治疗,740例患者接受了12个月的瑞美吉泮治疗。1
药物相互作用:1
- 不建议将瑞美吉泮与强效CYP3A4抑制剂(克拉霉素、伊曲康唑、利托那韦)合并使用。
- 不建议与强效CYP3A4诱导剂(苯巴比妥、利福平、圣约翰草 [贯叶连翘])或中效CYP3A4诱导剂(波生坦、依非韦伦、莫达非尼)合并使用。
- 如果与CYP3A4中效抑制剂(地尔硫卓、红霉素、氟康唑)或P-gp 强效抑制剂(环孢素、维拉帕米、奎尼丁)合并使用时,应避免在48小时内再次给予瑞美吉泮。
药物过量性头痛:1
- 过量使用任何类型的药物治疗头痛均可导致其恶化。
- 对于频繁出现或每日发作的头痛,即使已经常规使用了药物治疗急性头痛,或由于常规使用药物导致了头痛,均应考虑药物过量性头痛(MOH)的诊断。
- 如果已出现或怀疑出现这种情况,应立即就医,并停止治疗。
妊娠期:1
- 妊娠妇女服用瑞美吉泮的数据有限。
- 作为预防措施,建议在妊娠期间避免使用本品。
- 动物研究表明,瑞美吉泮没有胚胎致死作用,且在临床相关暴露量下未观察到致畸风险。在妊娠期间给予瑞美吉泮后,仅在与母体毒性相关的暴露水平(约为临床暴露量的200 倍)下观察到对胚胎-胎仔发育的不良影响(大鼠胎仔体重下降和骨骼变异增加)。
- 妊娠大鼠于器官发生期经口给予硫酸瑞美吉泮10、60、300 mg/kg/天,高剂量可导致与母体毒性相关的胎仔体重降低和胎仔骨骼变异发生率增加。大鼠胚胎发育毒性无影响剂量(60 mg/kg)下的血浆暴露量约为人最大推荐剂量(MRHD)暴露量的45倍。妊娠兔于器官发生期经口给予硫酸瑞美吉泮10、25、50 mg/kg/天,未见对兔胚胎发育的不良影响,高剂量(50 mg/kg/天)下兔血浆暴露量约为人MRHD暴露量的10倍。大鼠于妊娠期和哺乳期经口给予硫酸瑞美吉泮10、25、60 mg/kg/天,对大鼠围产期发育未见影响,高剂量(60 mg/kg/天)下大鼠血浆暴露量约为人MRHD暴露量的24倍。
哺乳期:1
- 目前尚没有关于母乳分泌量是否会受到影响的数据,临床使用时应考虑母乳喂养对发育和健康的获益,以及母亲对本品的临床需求,以及瑞美吉泮或母体基础疾病对母乳喂养婴儿的任何潜在不良反应。
- 在一项单中心研究中,12名哺乳期女性接受了瑞美吉泮75 mg单次给药,在她们的乳汁中仅检出极低浓度的瑞美吉泮。相对婴儿剂量(RID)不足1%。
生育能力:1
- 动物研究显示本品对雌性和雄性生育能力无临床相关的影响。
- 雄性和雌性大鼠在交配前和交配期间,雌性大鼠持续给药至妊娠期第7天经口给予硫酸瑞美吉泮30、60、150 mg/kg/天,高剂量可导致生育力降低。降低剂量进行第二项试验,给药剂量为5、15、25 mg/kg/天,未见对生育力和早期胚胎发育的不良影响。大鼠生育力和早期胚胎发育毒性无影响剂量(60 mg/kg/天)下的血浆暴露量约为人最大推荐剂量(MRHD)75 mg/天暴露量的30倍。
活性成分:硫酸瑞美吉泮
辅料:明胶,甘露醇,三氯蔗糖,薄荷香精
48个月
本品是一种降钙素基因相关肽(CGRP)受体拮抗剂。1
表2 关键临床概览
| 研究名称 | 研究设计 | 分组 | 研究终点 |
|---|---|---|---|
| BHV3000-3101,3 | 急性用药 中国和韩国患者;80%为中国患者 | 瑞美吉泮组 安慰剂组 | 主要终点:
|
| BHV3000-3181,4 | 长期安全性研究 中国患者 | 瑞美吉泮组 | 主要终点:
|
| BHV3000-3031,5 | 急性用药 美国患者 | 瑞美吉泮组 安慰剂组 | 主要终点:
|
| 博鳌真实世界研究 18 | 急性用药 中国患者 真实世界研究 | 治疗失败史亚组 极高发作频率亚组 联合单抗亚组 | 有效性终点:
耐受性终点:
|
| 大湾区真实世界研究 19 | 急性用药 中国患者 真实世界研究 | 急性治疗 | 瑞美吉泮治疗偏头痛的效果观察:
探索性终点:
|
MBS:最困扰症状,定义为恶心、畏声或畏光
研究概述:1,3
- 这是一项在中国和韩国开展的、双盲、随机、多中心、评估瑞美吉泮相比安慰剂治疗中度或重度偏头痛的安全性和有效性的研究。
- 受试者被分发一剂试验用药品,即瑞美吉泮75 mg或匹配的安慰剂。
- 研究的总持续时间约为11周。包括3-28天的筛选期、急性治疗期以及在试验用药品给药后7天内的治疗结束(EOT)访视。
- 研究随机入组了1431例受试者。
关键纳入标准:3
- 在入组前3个月内:
- 每月中重度偏头痛发作≥2次
- 每月头痛天数<15天
关键排除标准:3
- 目前有证据表明有未控制、不稳定或最近确诊的心血管疾病
研究终点:1,3
- 主要终点:给药后2小时无痛比例、给药后2小时无最困扰的症状 (MBS) 比例。
- 次要终点:给药后2小时的疼痛缓解率、给药后2小时功能恢复正常的比例、给药后24小时内的补救药物使用情况、给药后2-24小时的持续无疼痛率、给药后2-48小时的持续无疼痛率。
单剂给药后2小时患者无痛比例,瑞美吉泮组显著优于安慰剂组。3
图1 2小时无痛患者比例3
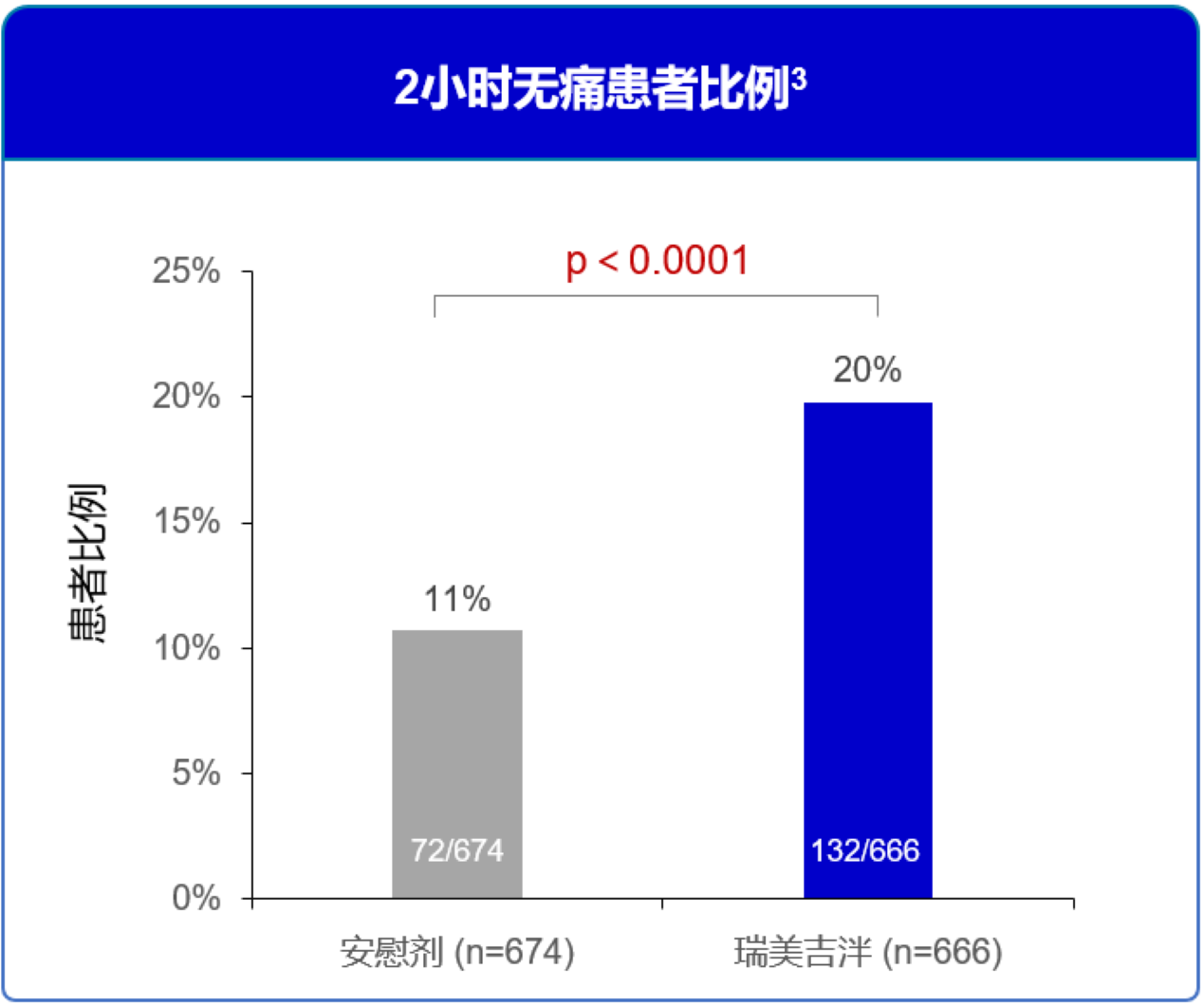
单剂给药后2小时患者无最困扰症状(MBS)比例,瑞美吉泮组显著优于安慰剂组。3
图2 2小时无MBS患者比例3
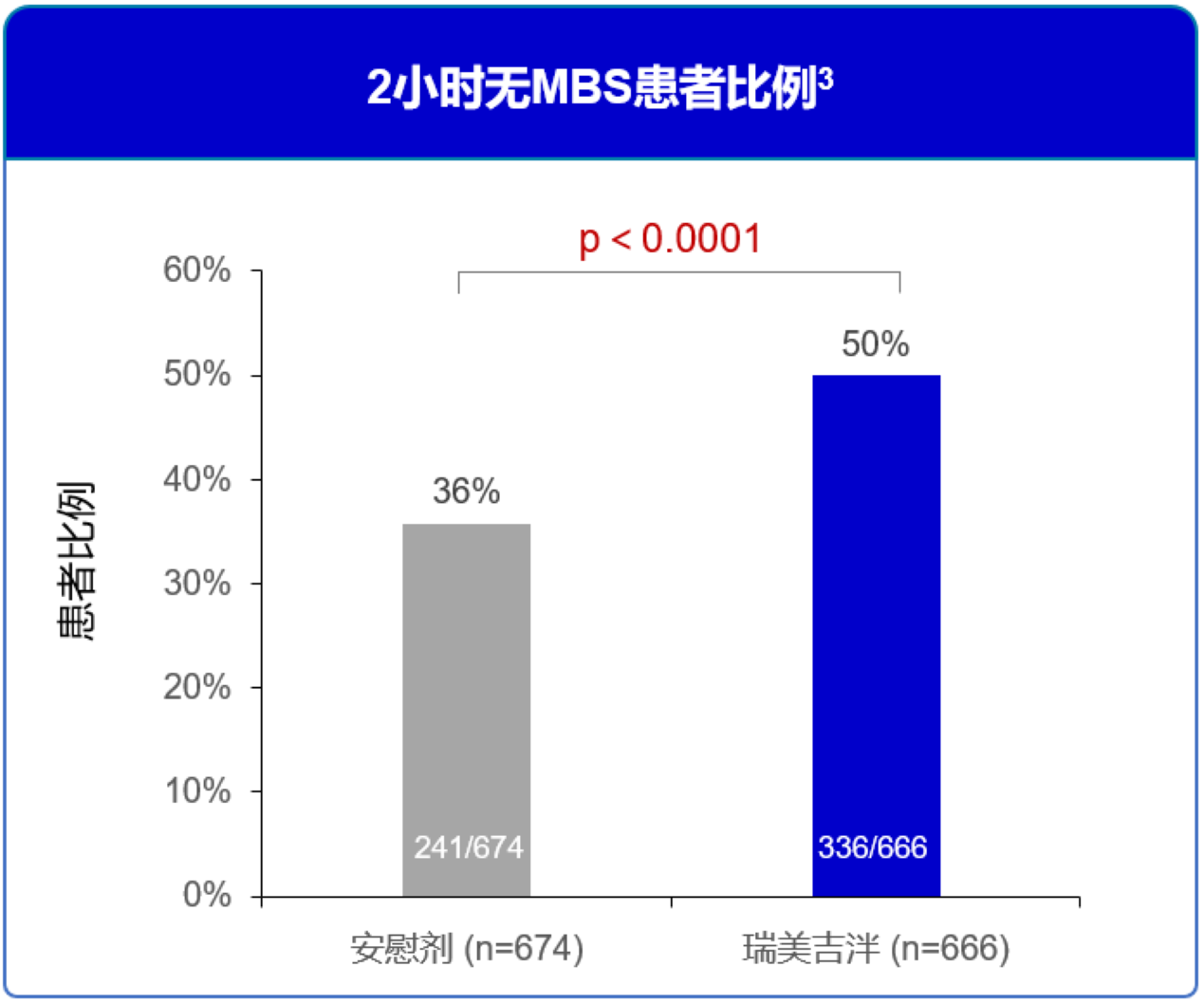
MBS:最困扰症状
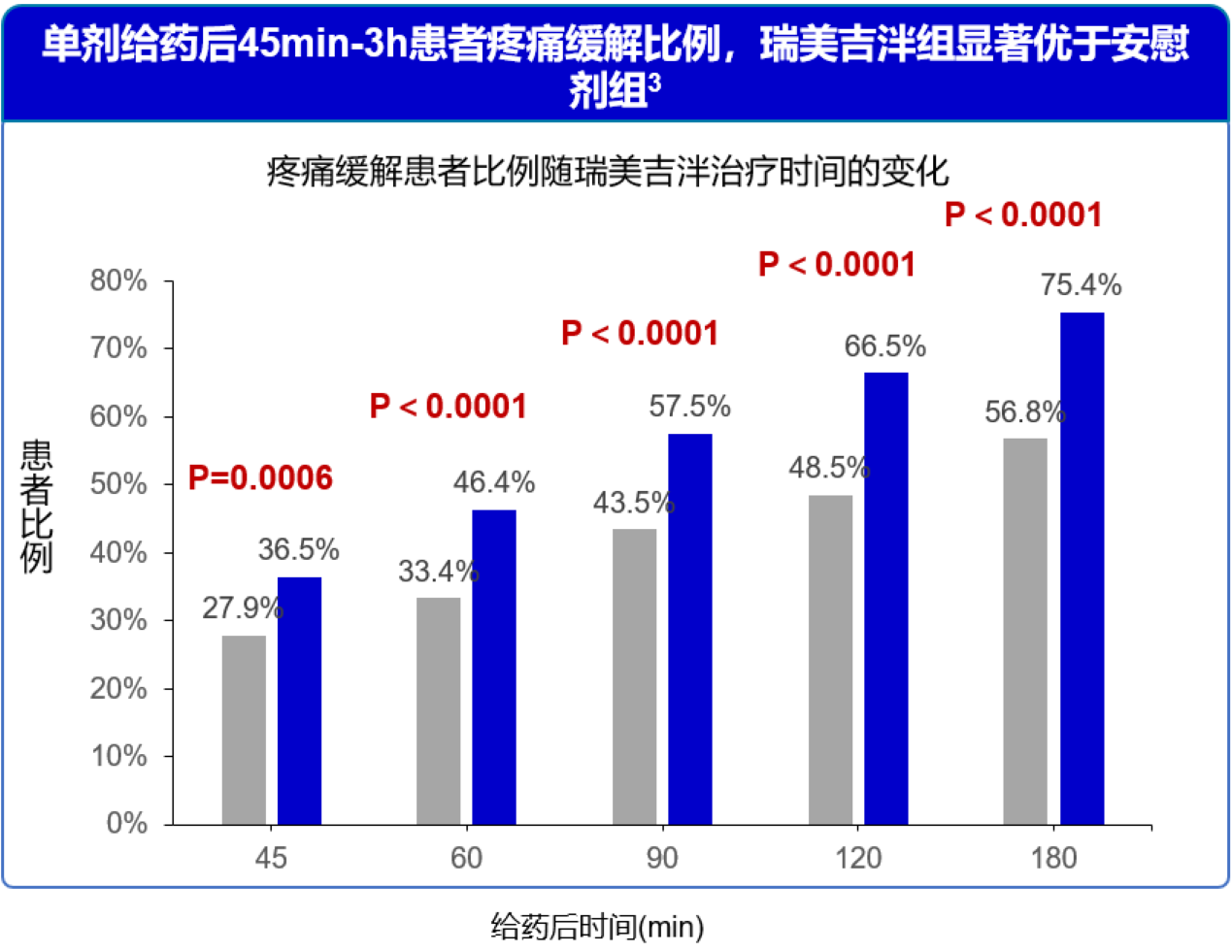
单剂给药后45分钟患者疼痛缓解比例,瑞美吉泮组显著优于安慰剂组,45分钟至3小时患者疼痛缓解比例,瑞美吉泮组持续显著优于安慰剂组。3
图3 单剂给药后45分钟至3小时患者疼痛缓解比例,瑞美吉泮组显著优于安慰剂组。3
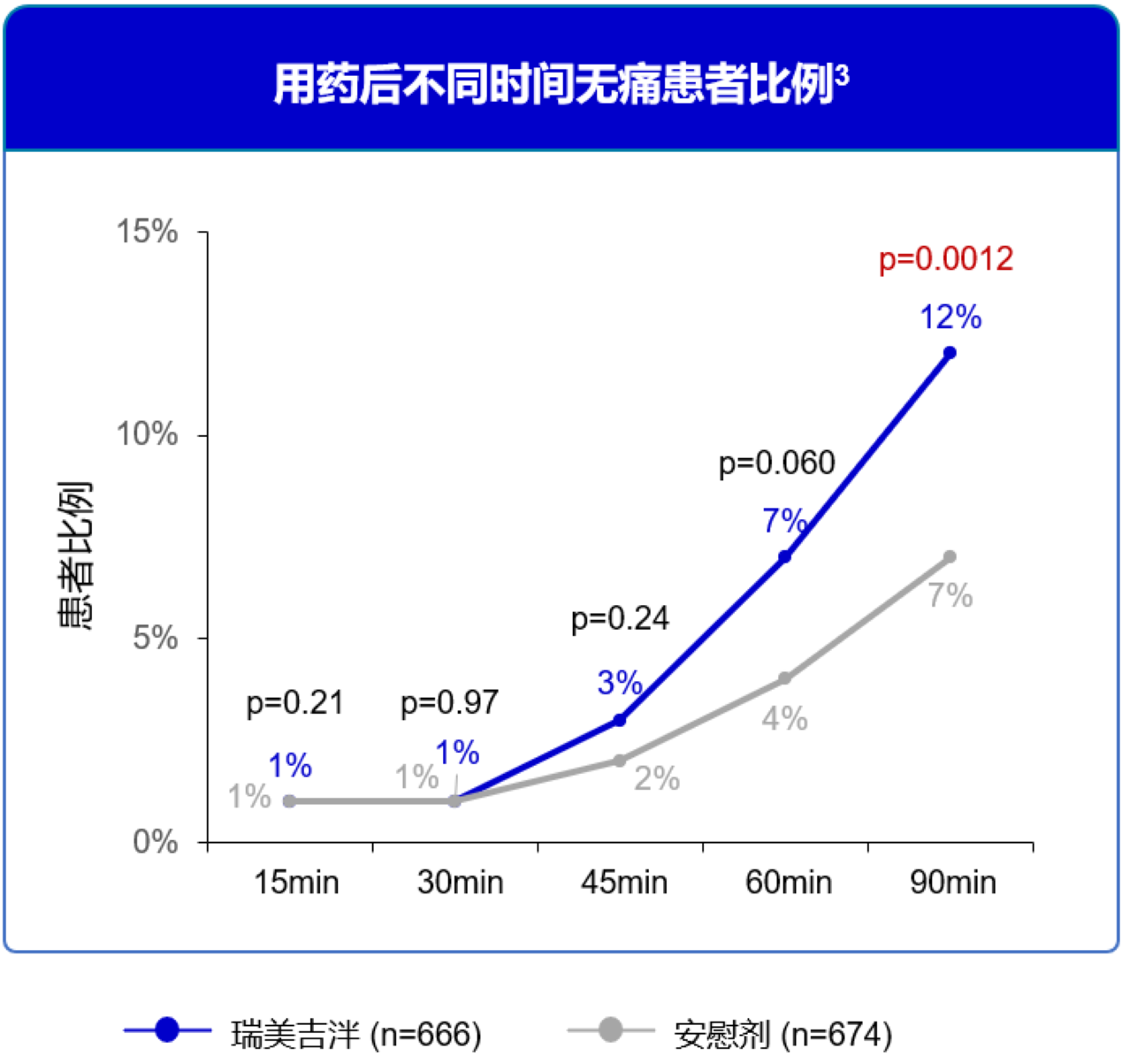
瑞美吉泮组在给药后90分钟的无痛方面的疗效显著优于安慰剂组。3
图4 用药后不同时间无痛患者比例3
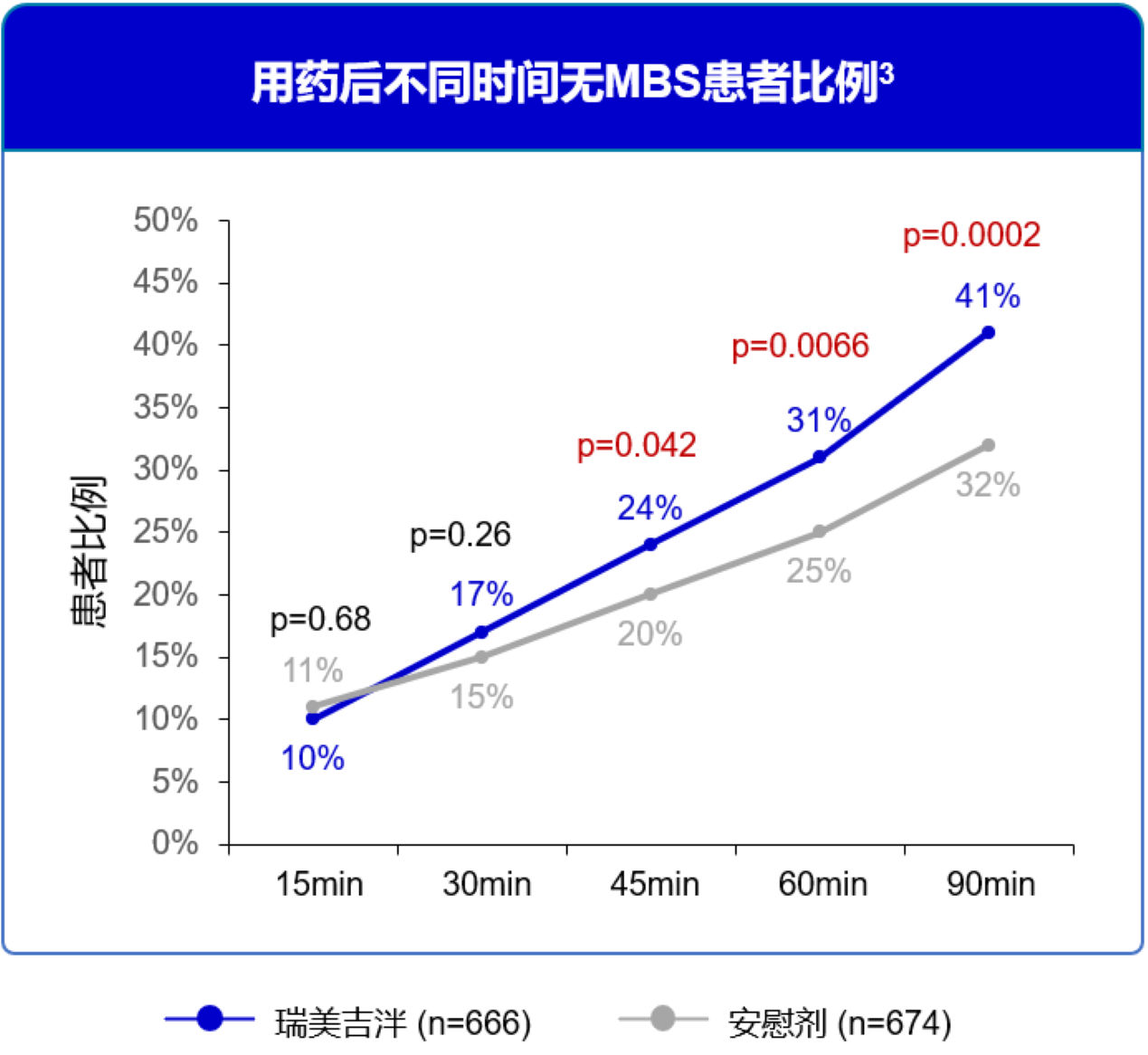
瑞美吉泮组在给药后45分钟的无最困扰症状(MBS)方面的疗效显著优于安慰剂组。3
图5 用药后不同时间无MBS患者比例3
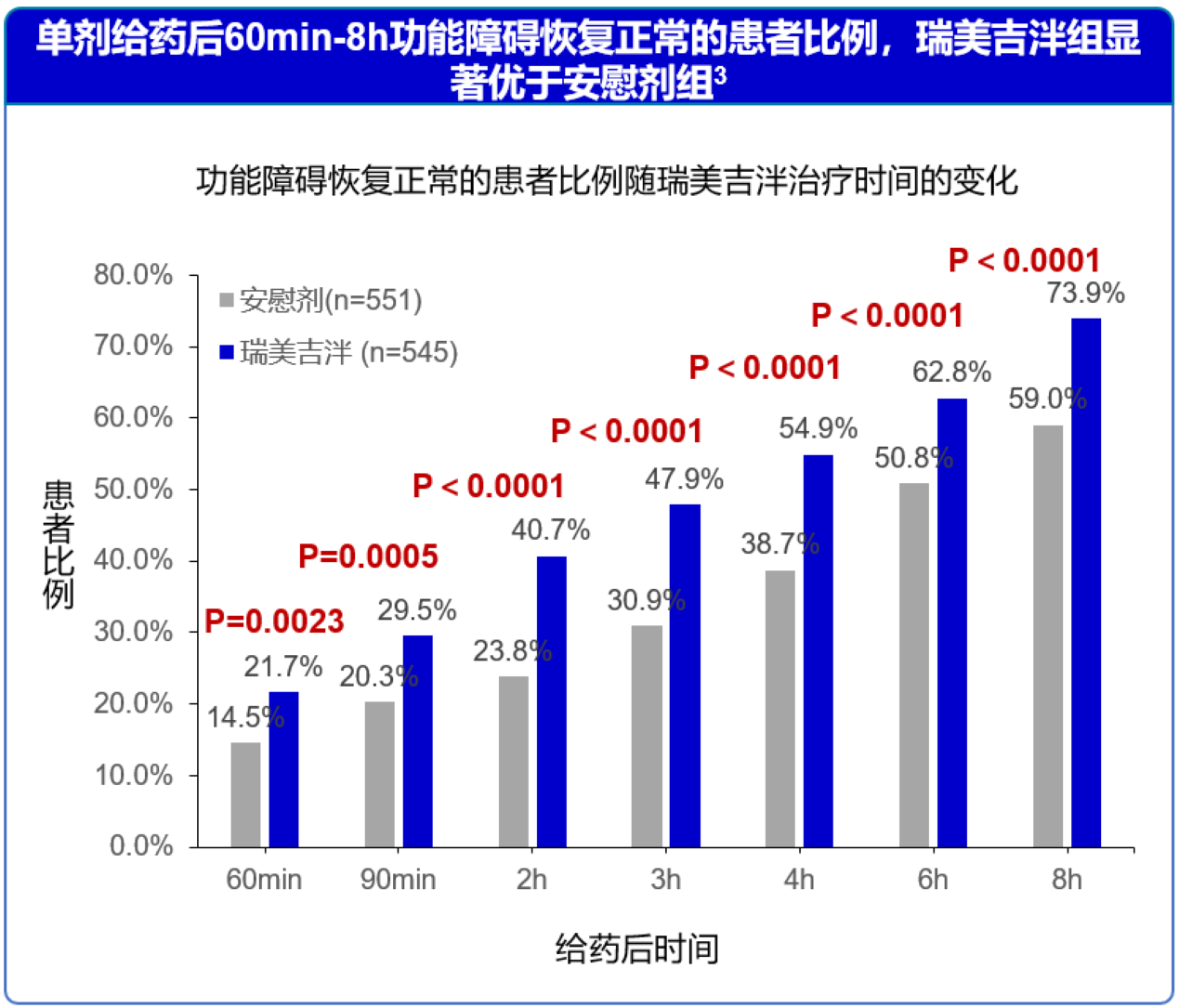
单剂给药后60分钟患者恢复正常功能比例,瑞美吉泮组显著优于安慰剂组,60分钟至8小时患者恢复正常功能比例,瑞美吉泮组持续显著优于安慰剂组。3
图6 单剂给药后60分钟至8小时功能障碍恢复正常的患者比例,瑞美吉泮组显著优于安慰剂组。3
单剂给药后2小时患者疼痛缓解比例,瑞美吉泮组显著优于安慰剂组。3
图7 2小时疼痛缓解3
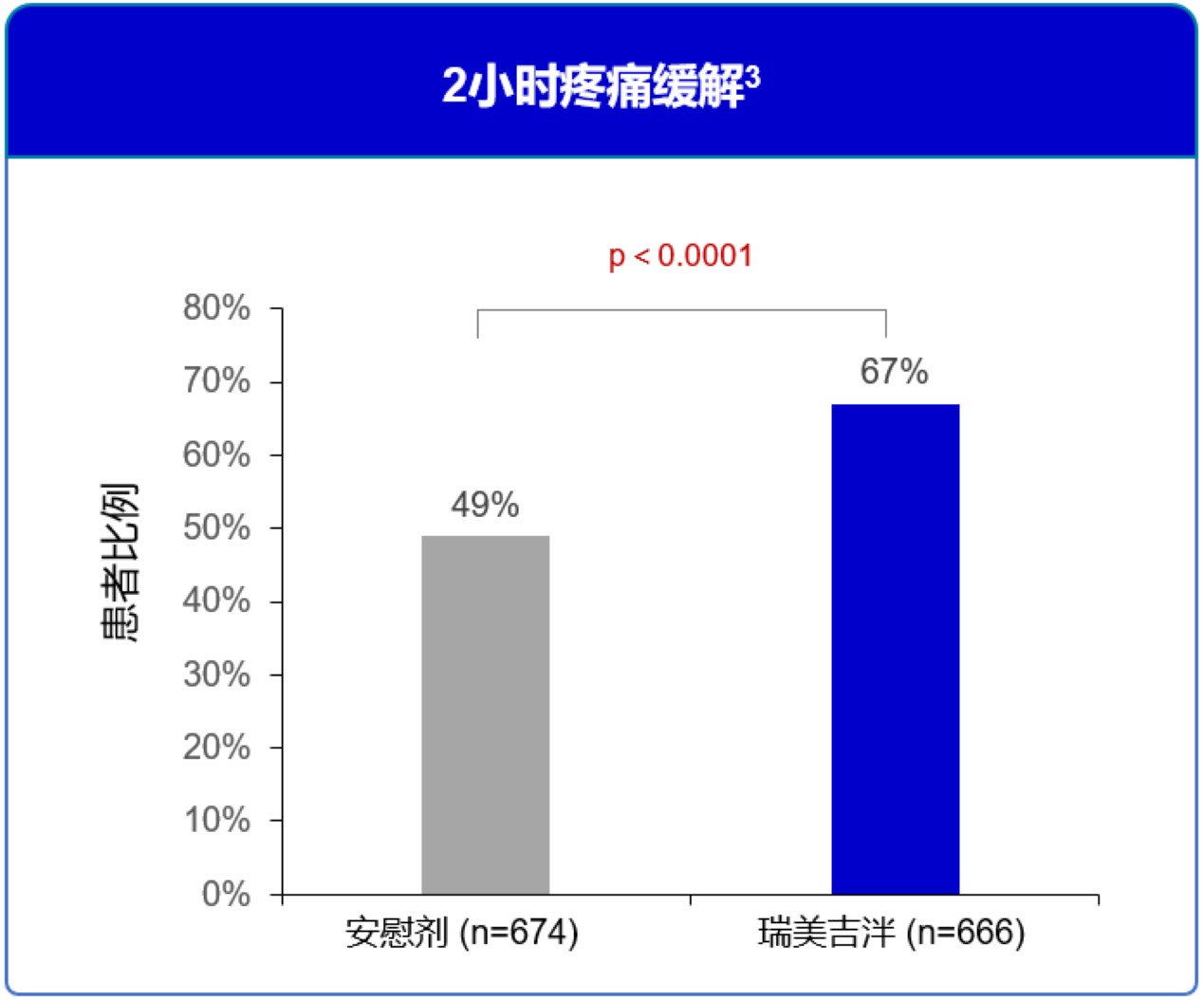
单剂给药后2小时患者功能障碍恢复正常比例,瑞美吉泮组显著优于安慰剂组。3
图8 2小时功能障碍恢复正常3
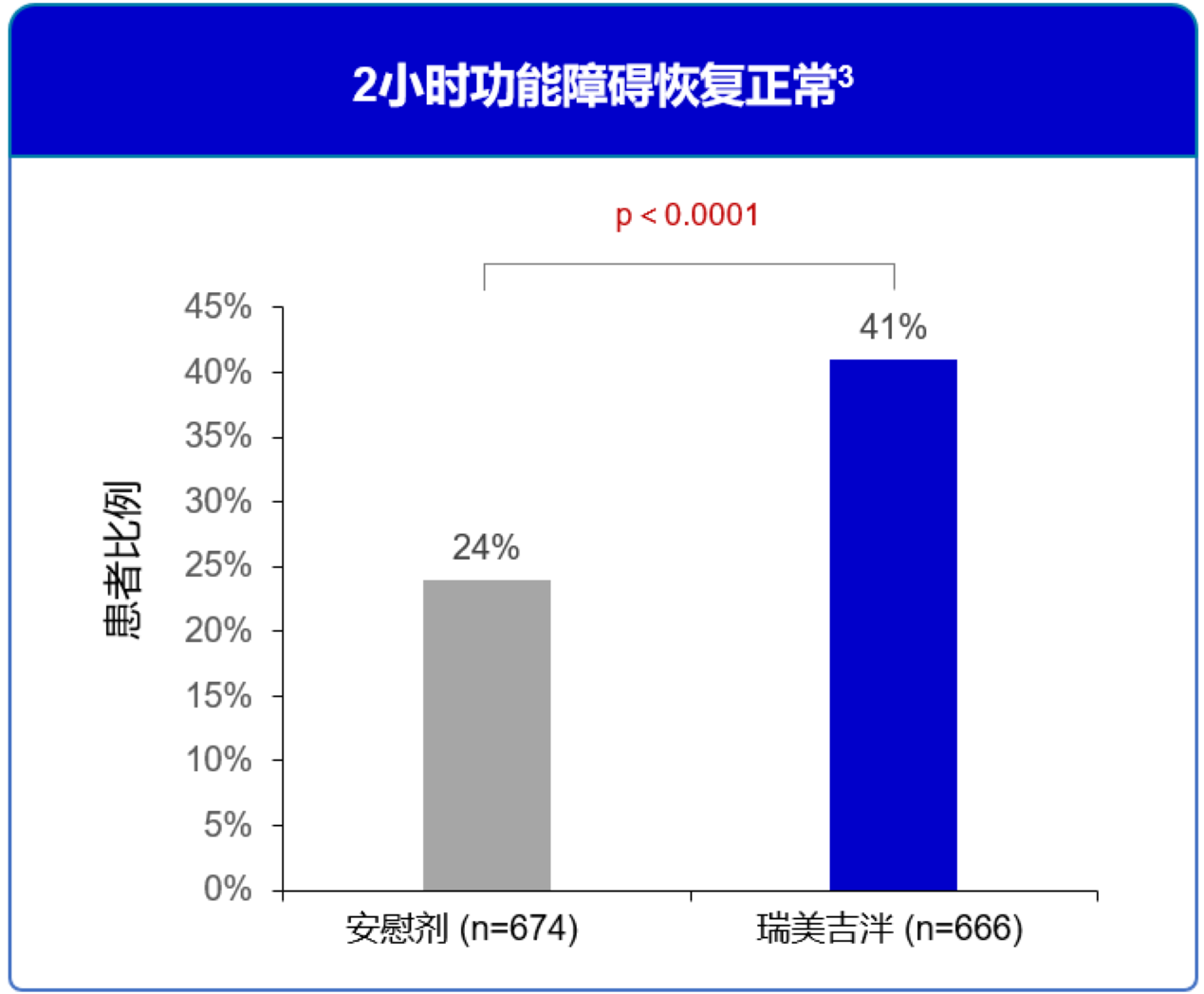
单剂给药后24小时内患者使用补救药物比例,瑞美吉泮组显著优于安慰剂组。3
图9 24小时内使用补救药物3
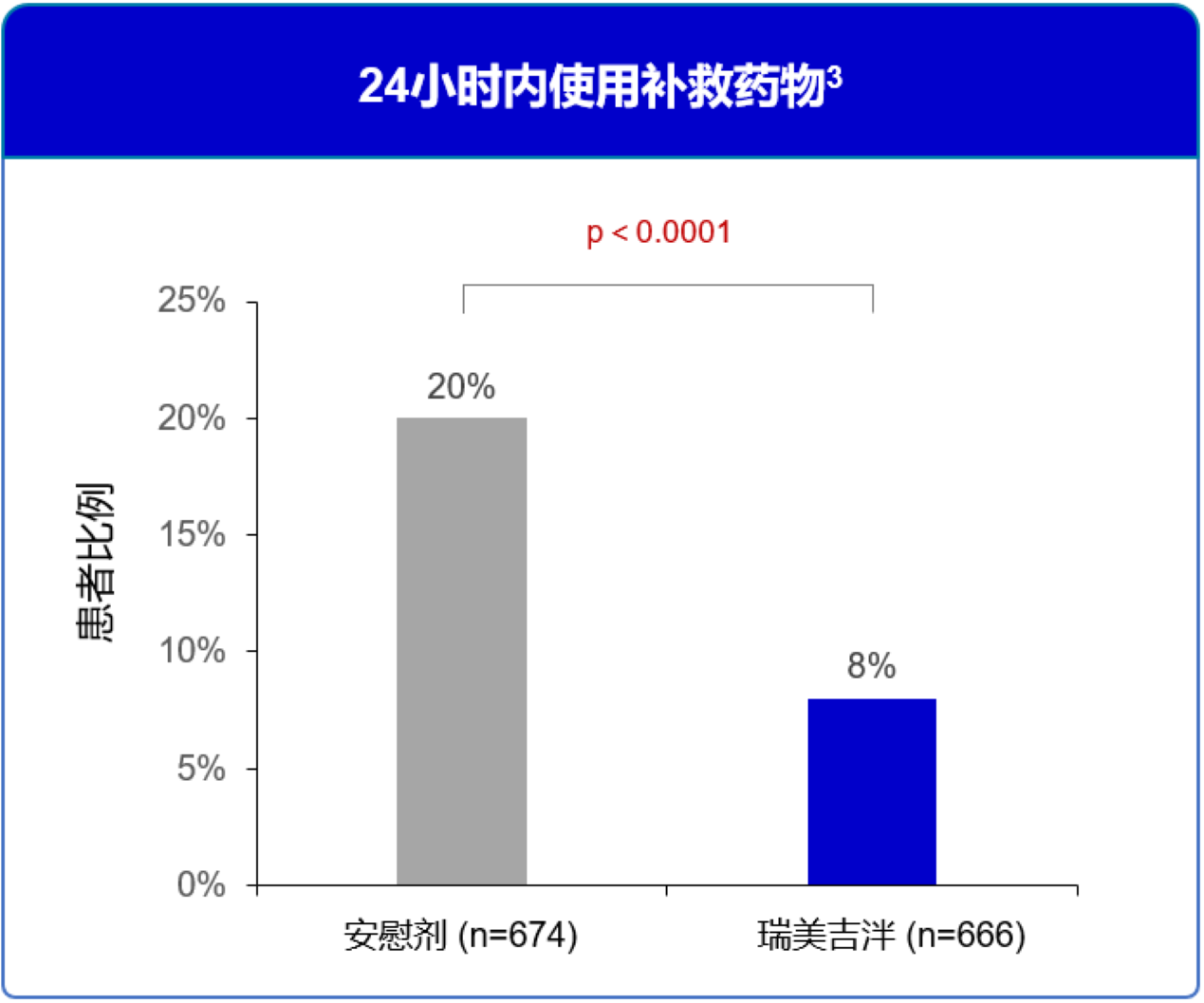
单剂给药后患者2-24小时和2-48小时持续无疼痛率,瑞美吉泮组显著优于安慰剂组。3
图10 2-24小时和2-48小时持续无疼痛率3
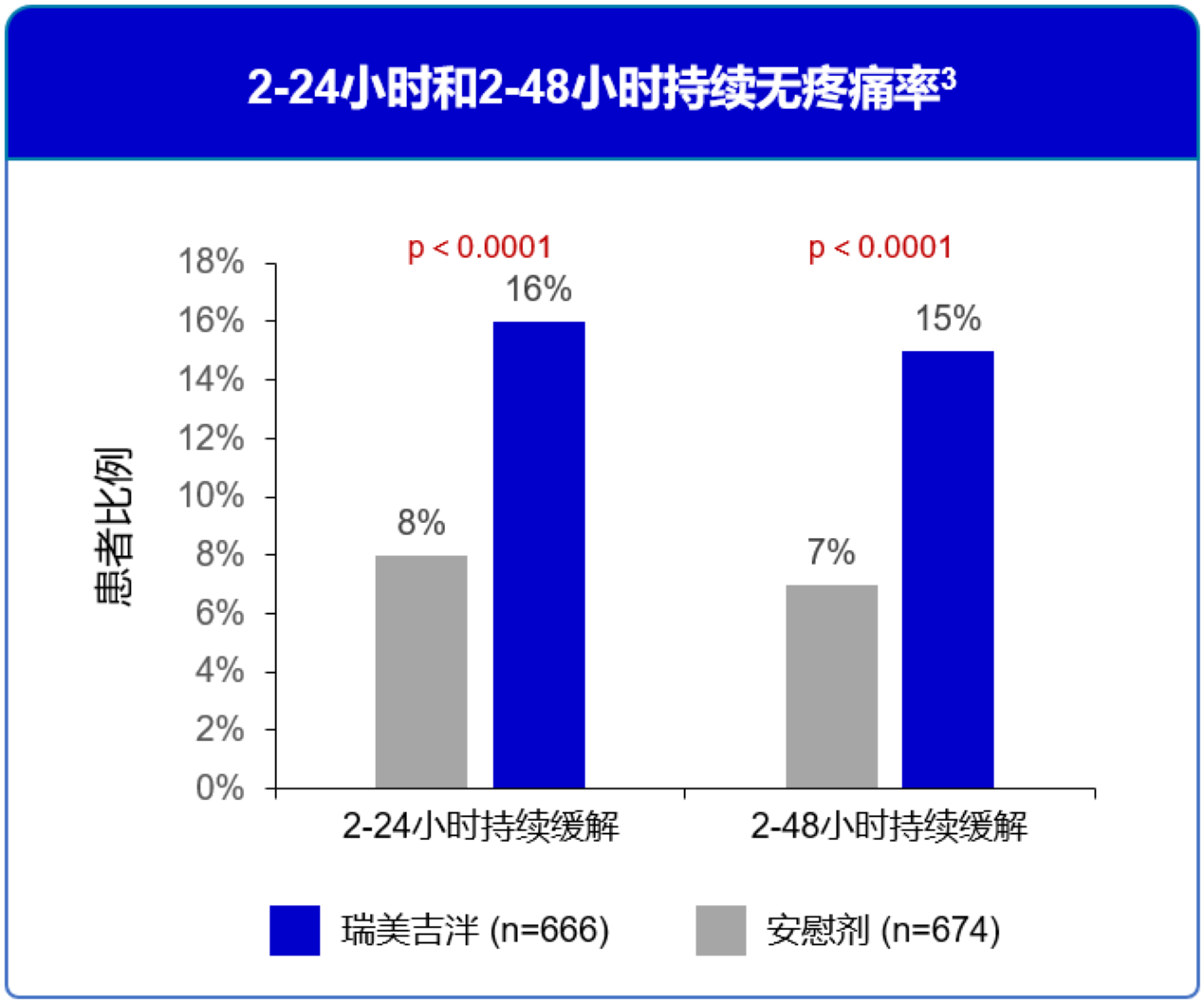
- 中韩3期研究中国患者占比>80%。研究整体的安全性能够体现中国患者服用瑞美吉泮后的安全性。3
- 瑞美吉泮组和安慰剂组不良反应总体发生率相当(16% vs17%),大多数不良事件为轻度或中度,TEAEs、严重TEAEs以及药物相关的严重TEAEs,安慰剂组的发生率均高于或等于瑞美吉泮组,且瑞美吉泮组没有任何患者出现与药物相关的严重不良反应。3
表3 中韩3期研究不良事件概览
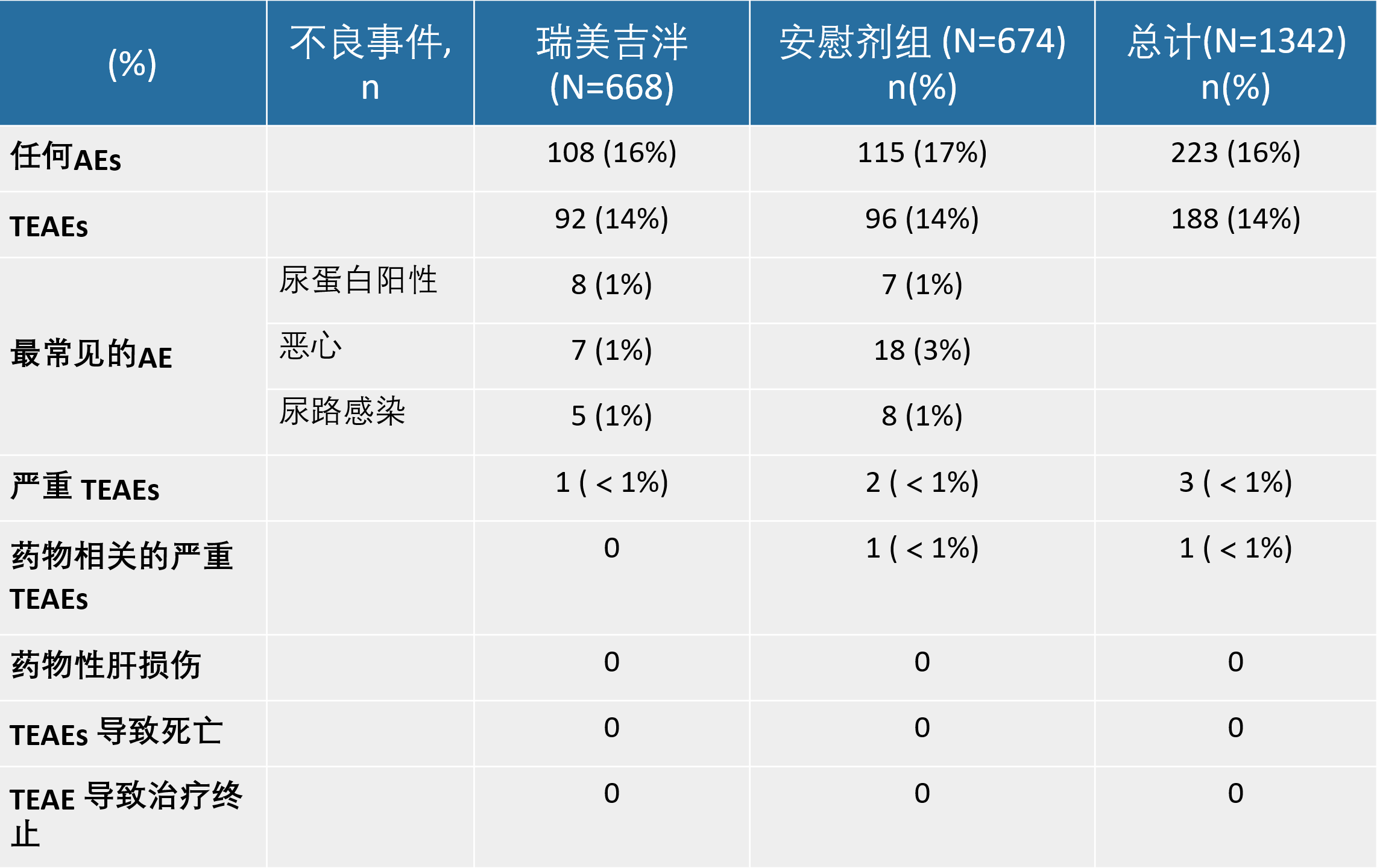
AE=不良事件;TEAE=治疗期间不良事件。
基于瑞美吉泮中韩3期临床试验的研究结果,对1075名中国受试者进行子集分析:6
- 瑞美吉泮75 mg用于中国成人偏头痛的急性治疗有效,具有快速、持续的疗效,安全性和耐受性和安慰剂组相当。
- 这些结果证实了先前研究的发现,并且与总体试验人群的结果相似。单剂给药后患者2小时无痛和无最困扰症状(MBS)比例,瑞美吉泮组显著优于安慰剂。
图11 中国患者亚组分析共同主要终点 瑞美吉泮在改善服药后2小时无疼痛及无MBS患者比例
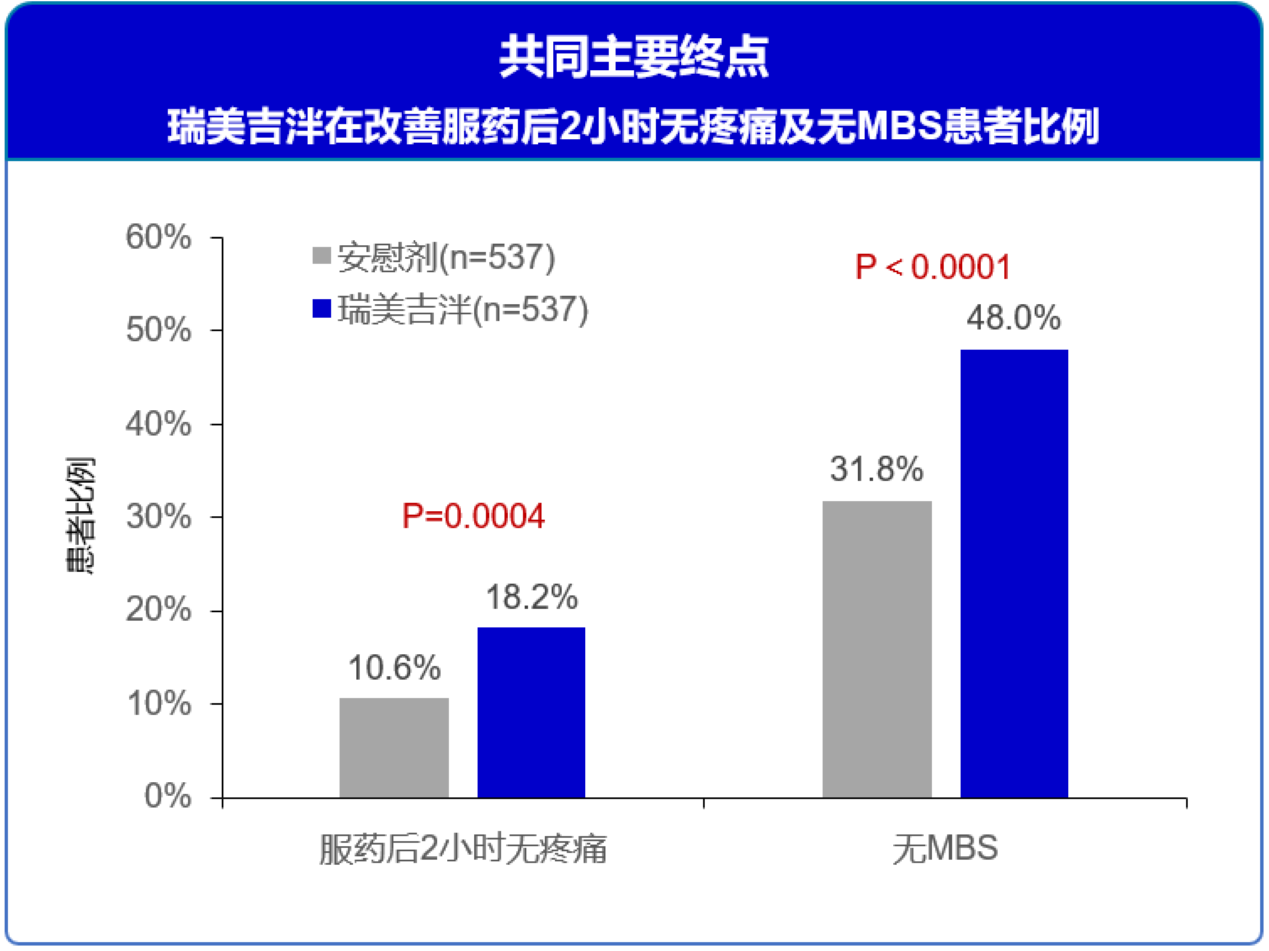
MBS:最困扰症状
图12 中国患者亚组分析关键次要终点 瑞美吉泮所有的关键次要终点改善均显著优于安慰剂6
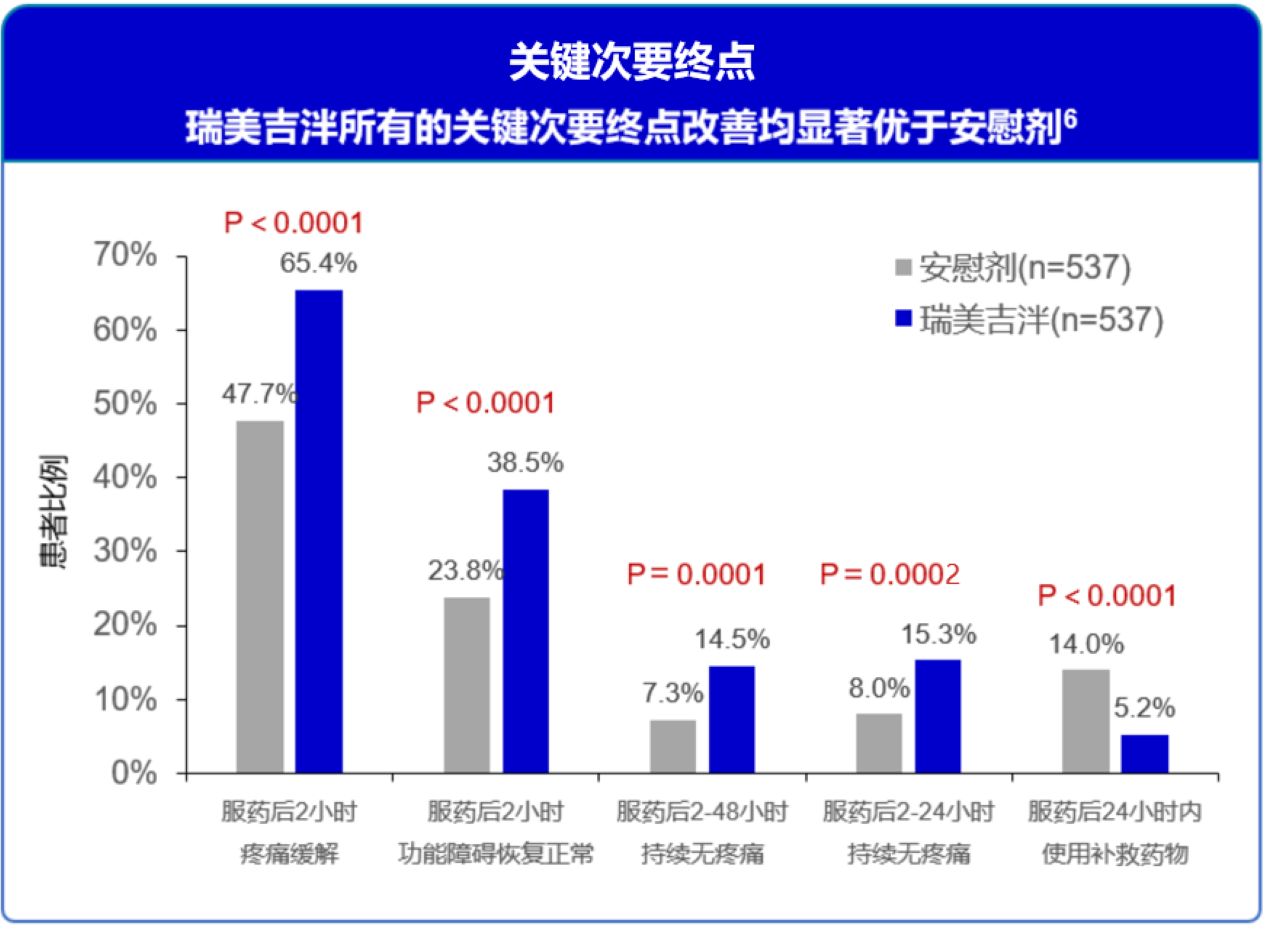
基于瑞美吉泮中韩3期临床试验的研究结果,对1075名中国受试者进行子集分析:6
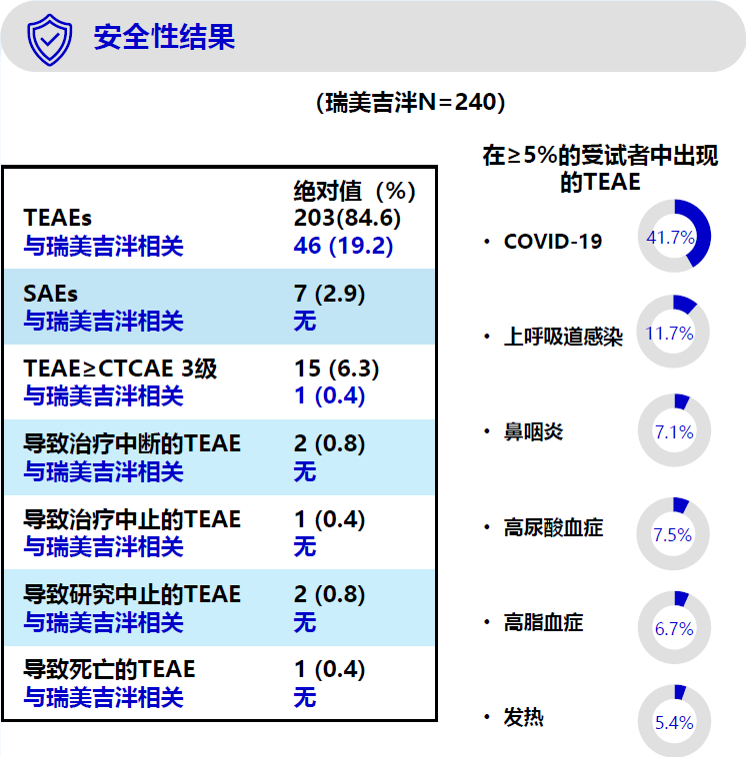
- 瑞美吉泮的总体安全性与安慰剂相当,因此在中国受试者身上观察到的安全性结果也与之前在美国进行的瑞美吉泮试验结果一致。
- 在中国受试者亚组中,瑞美吉泮组未出现与治疗相关的严重TEAE,大多数TEAE的严重程度为轻度或中度,大多数TEAE无需治疗即可缓解,TEAE在瑞美吉泮组和安慰剂组中的发生率相似,未观察到心电图或常规实验室检查有临床意义的变化,也未出现肝毒性信号。
表4 所有接受治疗的中国受试者的治疗期间不良事件概要
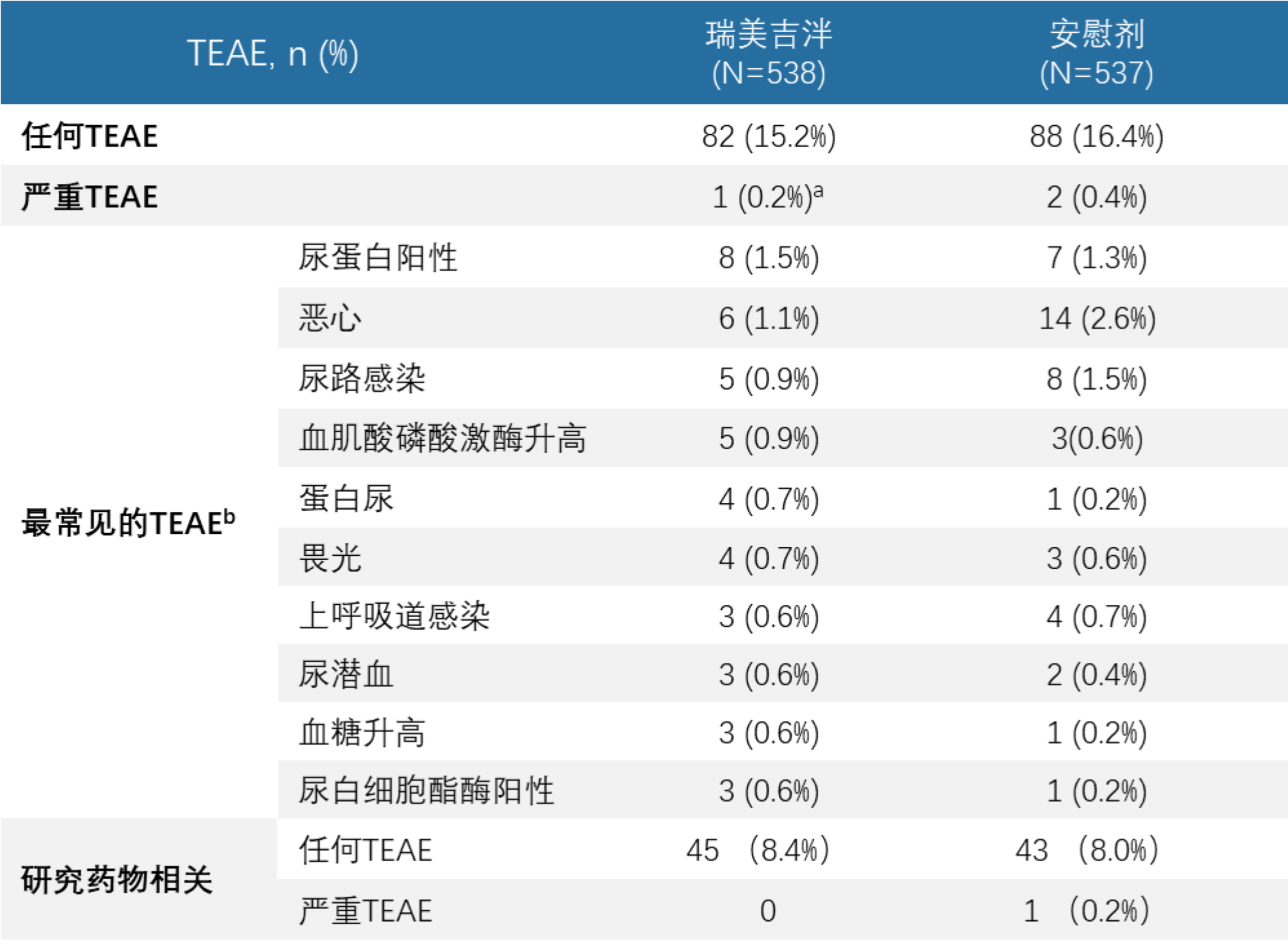
TEAE=治疗期间不良事件
a该严重TEAE使用MedDRA(23.0版)首选术语“感染”进行分类。
b瑞美吉泮口崩片75 mg组有≥0.5%的受试者出现TEAE。
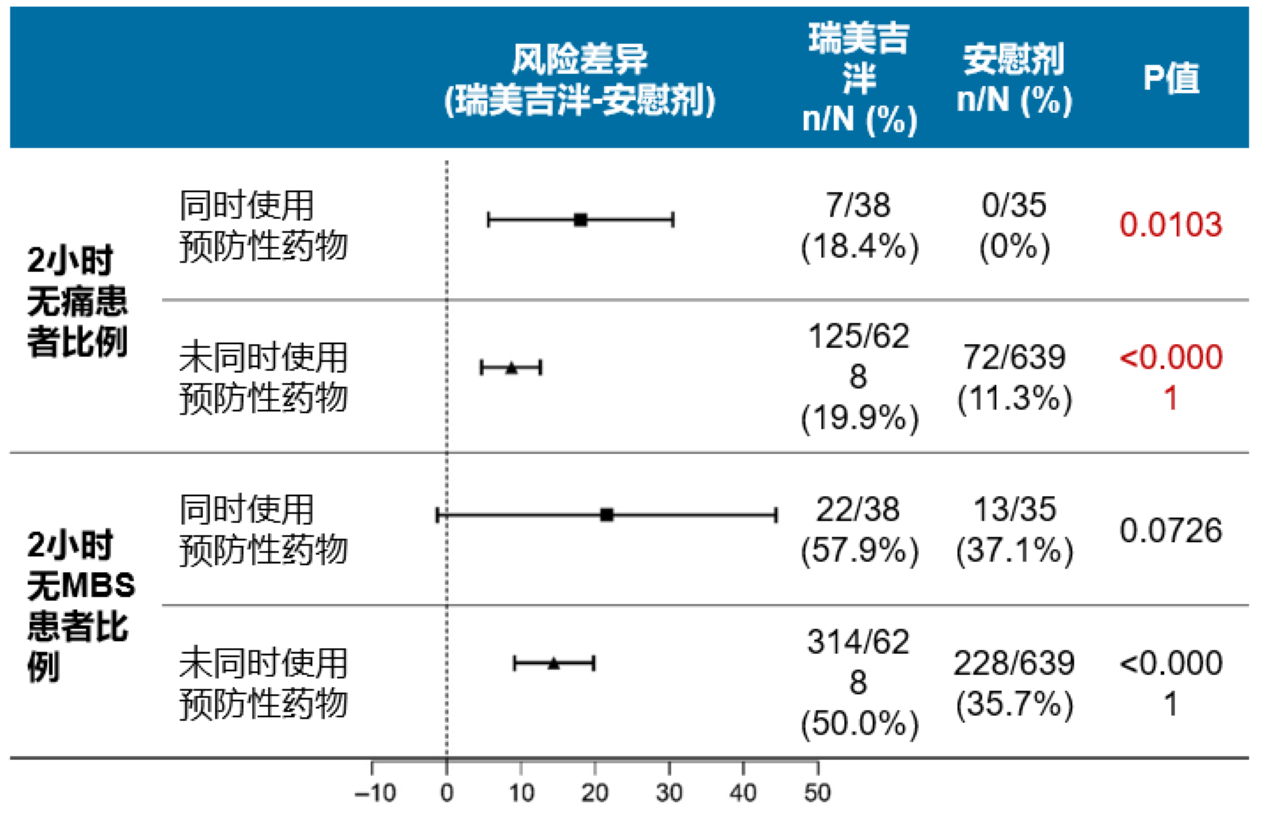
无论患者是否同时使用预防性药物,瑞美吉泮均可显著提高无痛患者比例。
瑞美吉泮中韩3期研究中,98例(7.3%)受试者既往使用过预防性偏头痛药物*,使用最多的前三种预防性药物分别为:氟桂利嗪,阿米替林,托吡酯。7
表5 瑞美吉泮中韩3期亚组分析
风险差异 (95%CI)
*允许使用预防性偏头痛药物的受试者继续接受该治疗,只要这些受试者在筛选访视前接受稳定剂量治疗至少已达3个月,且该剂量预计不会在研究期间改变。
MBS:最困扰症状
本研究证实了中国偏头痛患者使用瑞美吉泮急性治疗1年,其安全性和耐受性良好。
瑞美吉泮75 mg 按需使用治疗偏头痛急性发作,从第一个月起即减少患者每月偏头痛天数(MMDs)和疼痛强度。治疗一个月后,MMDs平均值从11.2天(基线)降低至9.5天。治疗11个月后,MMDs进一步降低至5.5天。
患者每月服用瑞美吉泮的片数逐渐下降。
使用瑞美吉泮按需治疗1年,偏头痛专用生活质量调查问卷(MSQoLQ)问卷评分(限制性角色功能、预防性角色功能,情感功能)均显著改善(52.7→77、62.3→85、63.2→86.2);偏头痛失能评估测试问卷(MIDAS)评分显著改善(55.1→ 17.3)。
本研究证实,瑞美吉泮按需治疗可以持续降低偏头痛发作频率,有效阻止发作性偏头痛向慢性偏头痛的转化。
研究概述:4
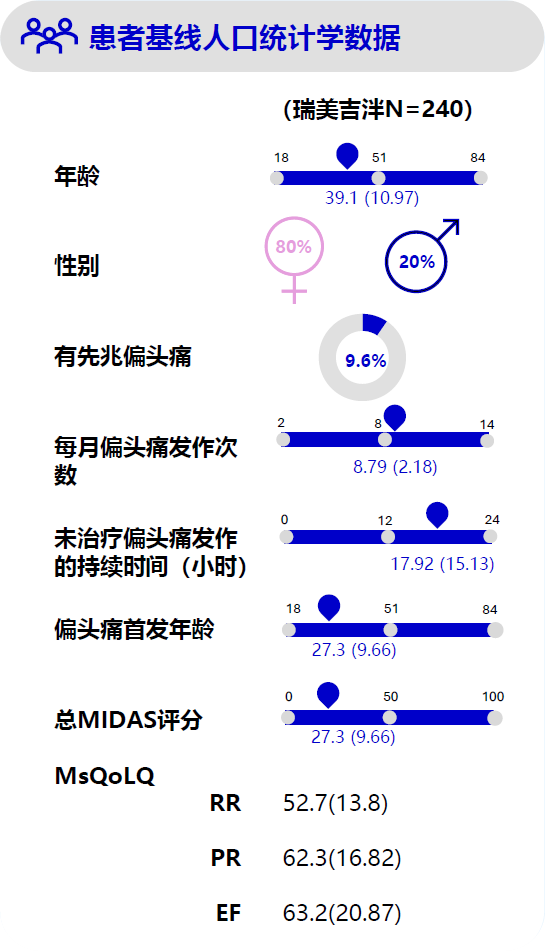
本研究是一项多中心、开放研究,目的是在中国偏头痛受试者中评估瑞美吉泮75 mg长期给药(按需给药,每个日历日最多给药1片)的安全性和耐受性。研究入组240名受试者,观察期为30天,疗程期限为52周±7天,随后进行14±2天的随访。
纳入标准和筛选过程:4
纳入标准包括年龄≥18岁,至少有1年的偏头痛史(根据国际头痛分类第3版[beta版]),首次偏头痛发作年龄小于50岁,偏头痛发作持续时间为4-72小时(如果未接受治疗),以及在30天的观察期内至少有6天的偏头痛发作。此外,筛选前3个月内,每月中重度偏头痛发作次数应在6-18次之间。该研究允许使用预防性偏头痛药物的患者也可入组。
研究终点:4
研究的主要终点包括不良事件的记录,包括常见不良事件(发生率≥5%)、严重不良事件、导致停药的不良事件以及检查数据等。次要终点包括每4周偏头痛发作的天数(与观察期相比)、每4周偏头痛发作的严重程度(与观察期相比)。此外,还设有探索性终点,包括
1.参与者的生活质量(QoL),通过使用偏头痛特异性生活质量问卷(MSQoLQ版本2.1)在基线的变化来衡量,2.偏头痛相关的残疾,通过使用偏头痛残疾评估(MIDAS)在基线的变化来衡量,3.受试者的偏好、满意度和整体治疗反应
头痛发作频率
对于所有严重程度(轻中重度)的偏头痛发作
- 按需服用瑞美吉泮一个月MMDs平均降低1.7天,MMDs由基线11.2天降至9.5天
- 至第11个月MMDs降低5.7天,MMDs降至5.5天
对于中重度的偏头痛
- 按需服用瑞美吉泮一个月即有效降低MMDs1.9天,MMDs由基线9.3天降至7.4天
- 至第11个月MMDs降低5.9天,MMDs降至3.4天
用药片数
患者每月服用瑞美吉泮的片数逐渐下降
- 第2个月(第5–8周)中位数平均瑞美吉泮剂量最高,为每月7片,至第9个月(第33–36周)时下降至每月4片。
- 在长期治疗期内,瑞美吉泮的平均月剂量中位数为4.6片;共有10.8%的患者每月服用少于2片,70.8%服用≥2至<8 片,12.9%服用≥8至<14片,5.4%服用≥14 片。
实验室检查异常
| 瑞美吉泮(N=240) | CTCAE分级 绝对值(%) | ||
|---|---|---|---|
| 1-2级 | 3-4级 | 未报告 | |
| 血红蛋白升高 | 15(6.3) | 0 | 2(0.8) |
| 贫血 | 34(14.2) | 1(0.4) | 2(0.8) |
| 白细胞减少 | 29(12.1) | 1(0.4) | 2(0.8) |
| 中性粒细胞计数减少 | 33(13.8) | 1(0.4) | 2(0.8) |
| 淋巴细胞计数减少 | 36(15.0) | 1(0.4) | 2(0.8) |
| 低钠血症 | 25(10.4) | 0 | 2(0.8) |
| 低钾血症 | 2(0.8) | 1(0.4) | 2(0.8) |
| 肌酐升高 | 13(5.4) | 0 | 2(0.8) |
| 肌酸磷酸激酶(CPK)升高 | 10(4.2) | 4(1.7) | 2(0.8) |
| 天冬氨酸氨基转移酶(AST)升高 | 27(11.3) | 1(0.4) | 2(0.8) |
| 丙氨酸氨基转移酶(ALT)升高 | 36(15.0) | 0 | 2(0.8) |
| 慢性肾病* | 52(21.7) | 0 | 2(0.8) |
| 胆固醇升高 | 55(22.9) | 0 | 11(4.6) |
| 高甘油三酯血症 | 50(20.8) | 2(0.8) | 11(4.6) |
注:CTCAE=不良事件通用术语标准;CPK=肌酸磷酸激酶;AST=天冬氨酸氨基转移酶;ALT=丙氨酸氨基转移酶。
*慢性肾病基于估算的肾小球滤过率(eGFR)。
研究概述:1,5
- 这是一项在美国开展的、双盲、随机、多中心、评估瑞美吉泮相比安慰剂治疗中度或重度偏头痛的安全性和有效性的研究。
- 受试者被分发一剂试验用药品,即瑞美吉泮75mg或匹配的安慰剂。
- 研究的总持续时间约为11周。包括3-28天的筛选期、急性治疗期以及在试验用药品给药后7天内的治疗结束(EOT)访视。
- 研究随机入组了1811例受试者。
关键纳入标准:5
- 在入组前3个月内:
- 每月中重度偏头痛发作2-8次
- 每月头痛天数<15天
关键排除标准:5
- 目前有证据表明有未控制、不稳定或最近确诊的心血管疾病
研究终点:1,5
- 主要终点:给药后2小时无痛比例、给药后2小时无最困扰的症状 (MBS) 比例。
- 次要终点:给药后2小时的疼痛缓解率、给药后2小时功能恢复正常的比例、给药后24小时内的补救药物使用情况、给药后2-24小时的持续无疼痛率、给药后2-48小时的持续无疼痛率。
瑞美吉泮组比安慰剂组在服药后2小时无疼痛及无最困扰症状(MBS)的患者比例更高。5
图18 主要终点:给药后2小时无痛、无MBS患者比例
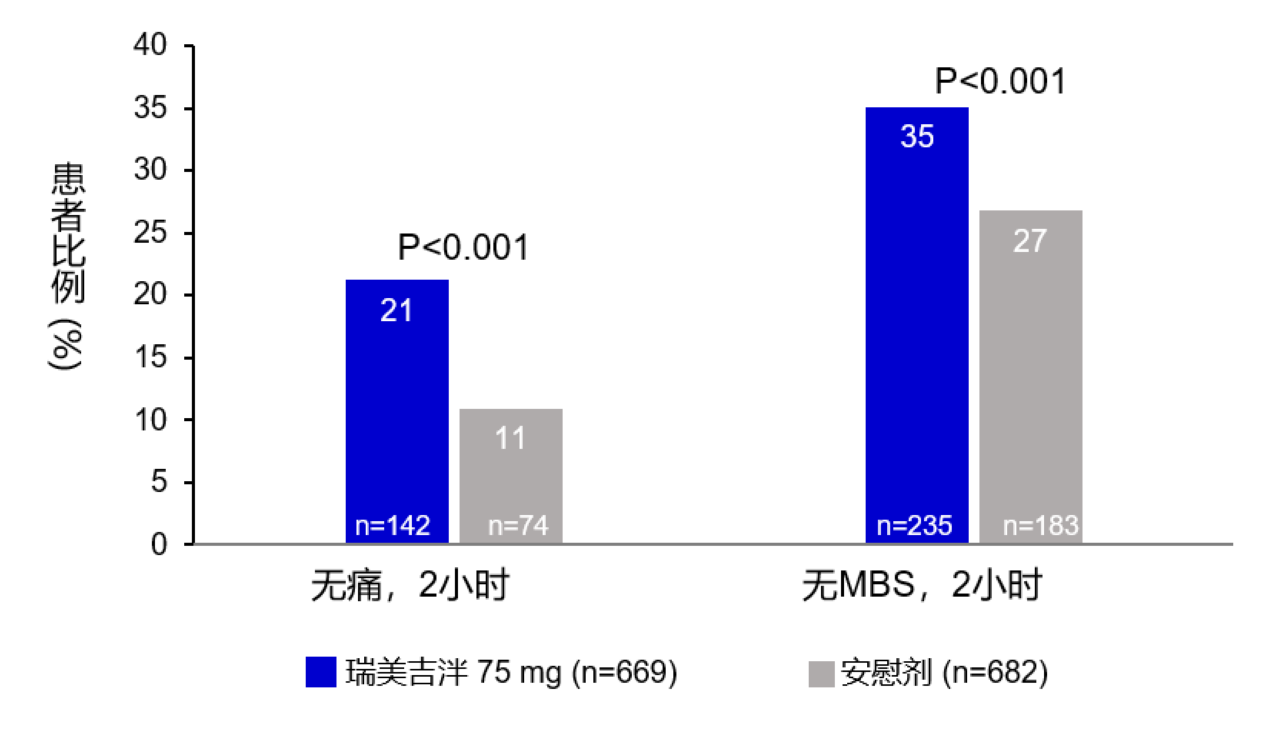
MBS=最困扰症状
瑞美吉泮组和安慰剂组分别有90名(13%)和73名(11%)患者报告不良事件(AE)。最常见的AE为恶心(瑞美吉泮2%,安慰剂1%)和尿路感染(瑞美吉泮1%,安慰剂1%)。两组患者均未报告严重不良事件。5
全球第一篇全文发表的瑞美吉泮急性治疗中国偏头痛患者的真实世界研究证据
主要纳入标准
- 根据《国际头痛疾病分类》第3版(ICHD-3)诊断为偏头痛(有或没有先兆),并由处方医生确定为常规治疗的成年人
主要排除标准
- 无法完成问卷和随访的个人、孕妇和哺乳期女性、高度依赖医疗护理的个人、研究者认为不适合参与研究的个人
有效性重点
- 给药后0.5、1、2、24、48h出现中度至重度疼痛的受试者百分比 在疼痛强度、功能状况、伴随症状方面好转/良好的患者比例#
耐受性终点
- 受试者在治疗期间报告的不良事件
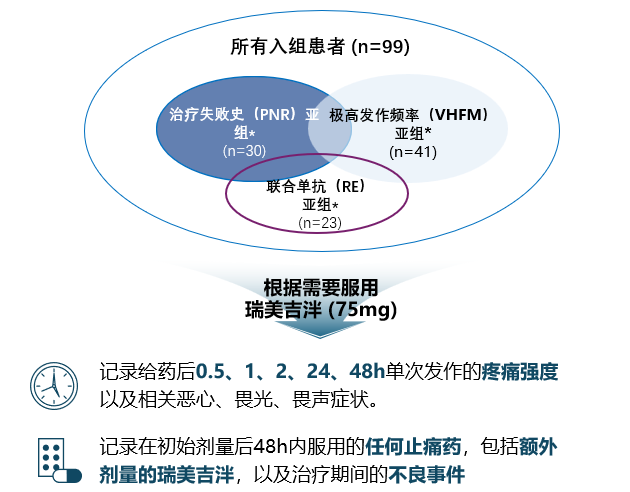
* PNR亚组:入组前1个月对任何急性或预防性偏头痛治疗药物无反应;RE亚组:使用瑞美吉泮治疗偏头痛发作,使用艾普奈珠单抗预防;VHFM亚组:MMDs≥15的患者
#疼痛程度好转/良好:疼痛强度较用药前有任何程度的降低(好转)或仅为轻度疼痛或无痛(良好);功能状况好转/良好:功能状况较用药前有任何程度的改善(好转)或仅为轻度受损或功能正常(良好);伴随症状好转/良好:伴随症状的数量较用药前有任何降低(好转)或无任何伴随症状(良好)
基线特征:研究人群相比一般偏头痛患者的严重程度更高
相比于一般偏头痛患者,本研究纳入患者:病程更长 (21.6 年 vs. 10.2 年) ;月经相关性偏头痛比例更高 (70.8% vs. 9.80%) ;偏头痛发作频率高:≥ 15 MMDs (41.4% vs. 20.9%) ;使用预防治疗的患者比例更高 (35.4% vs. 16.5%)
| 人口学特征 | 全人群(n=99) |
|---|---|
| 年龄,平均值(SD), y | 41.4 (10.4) |
| 女性,n (%) | 72 (72.7) |
| BMI,平均值 (SD), kg/m2 | 22.7 (3.5) |
| 偏头痛发作年龄,平均值(SD), y | 19.8 (9.1) |
| 伴随症状的数量,n (%) | |
| 0 | 2 (2.0) |
| 1 | 7 (7.1) |
| 2 | 13 (13.1) |
| ≥3 | 77 (77.8) |
| 伴随症状,n (%) | |
| 头晕 | 39 (39.4) |
| 恶心 | 79 (79.8) |
| 呕吐 | 65 (65.7) |
| 畏声 | 74 (74.7) |
| 畏光 | 69 (69.7) |
| 其他 | 50 (50.5) |
| 偏头痛家族史,n (%) | 61 (61.6) |
| 月经相关偏头痛,n (%) | 51 (70.8) |
| 原发性偏头痛类型,n (%) | |
| 无先兆偏头痛 | 53 (53.5) |
| 先兆性偏头痛 | 43 (43.4) |
| 不清楚 | 39 (3.0) |
| 过去一个月的 MMD中位数 (IQR)、d | 10.0 (5.0-20.0) |
| MMDs频率,n (%) | |
| 0-3 d | 16/99 (16.2) |
| 4-7 d | 21/99 (21.2) |
| 8-14 d | 21/99 (21.2) |
| ≥15 d | 41/99 (41.4) |
| 过去一个月的药物治疗情况,n (%) | |
| 接受过急性治疗 | 81 (81.8) |
| 接受过预防性治疗 | 35 (35.4) |
| 接受过急性和预防性治疗 | 24 (24.2) |
| 过去一个月发生AE, n (%) | 42 (42.4) |
| 过去一个月药物应答情况, n (%) | |
| 对任一急性治疗无应答 | 20 (20.2) |
| 对任一预防性治疗无应答 | 16 (16.2) |
| 对任一急性或预防性治疗无应答 | 30 (30.3) |
| HIT-6*得分、平均值(SD) | 65.6 (6.7) |
| 严重影响 (60-78),n (%) | 84 (87.5) |
| 重大影响 (56-59),n (%) | 6 (6.2) |
| 一些影响 (50-55),n (%) | 4 (4.2) |
| 轻微或无影响 (36-49),n (%) | 2 (2.1) |
| MSQ#得分,平均值(SD) | |
| 角色限制 | 45.0 (20.5) |
| 角色预防 | 51.1 (22.0) |
| 情绪功能 | 57.5 (26.6) |
瑞美吉泮治疗严重偏头痛患者可有效缓解疼痛
瑞美吉泮治疗后经历中度至重度疼痛的患者比例有 显著下降趋势
从51.5% 下降至2h 24.7% ,48h降至10.1%
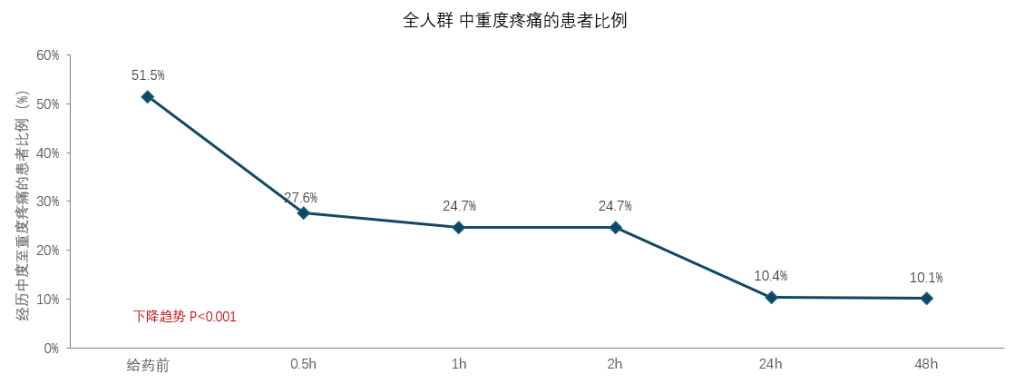
瑞美吉泮急性治疗可以有效改善严重偏头痛患者的头痛强度、功能状况和伴随症状
瑞美吉泮治疗0.5h即有超过60%的患者在疼痛强度、功能状况、伴随症状方面均实现好转/良好
治疗24h升高至90%以上,并维持至48h
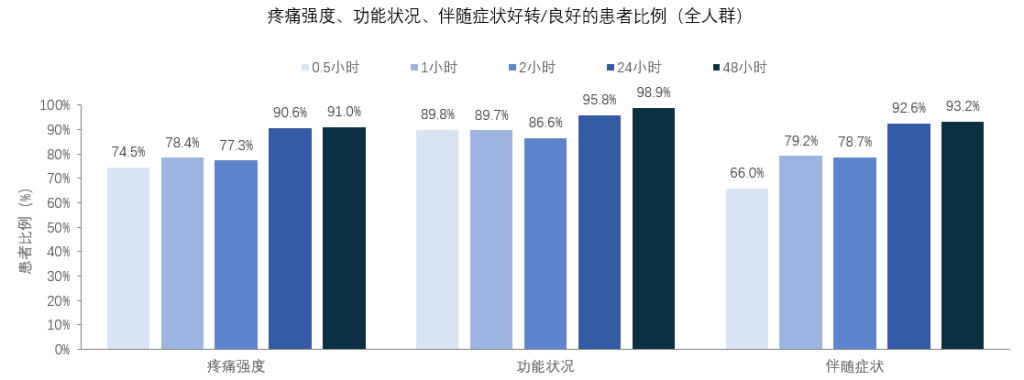
#疼痛程度好转/良好:疼痛强度较用药前有任何程度的降低(好转)或仅为轻度疼痛或无痛(良好);功能状况好转/良好:功能状况较用药前有任何程度的改善(好转)或仅为轻度受损或功能正常(良好);伴随症状好转/良好:伴随症状的数量较用药前有任何降低(好转)或无任何伴随症状(良好)
治疗失败史(PNR)亚组患者伴随症状更重,更多接受预防性治疗
几乎所有PNR患者都有严重的头痛相关残疾
PNR(治疗失败史)组与FP(全人群)相比:伴3种及以上伴随症状患者比例更高 (86.7% vs. 77.8%) ,呕吐患者更多(83.3% vs. 65.7%) ;使用预防治疗的患者比例更多 (63.3% vs. 35.4%) ;HIT-6严重影响的患者比例更高 (96.6% vs. 87.5%)
| 人口学特征 | FP(n=99) | PNR(n=30) |
|---|---|---|
| 年龄,平均值(SD), y | 41.4 (10.4) | 41.5 (9.8) |
| 女性,n (%) | 72 (72.7) | 24 (80.0) |
| BMI,平均值 (SD), kg/m2 | 22.7 (3.5) | 22.9 (3.1) |
| 偏头痛发作年龄,平均值(SD), y | 19.8 (9.1) | 18.9 (8.9) |
| 伴随症状的数量,n (%) | ||
| 0 | 2 (2.0) | 0 (0.0) |
| 1 | 7 (7.1) | 2 (6.7) |
| 2 | 13 (13.1) | 2 (6.7) |
| ≥3 | 77 (77.8) | 26 (86.7) |
| 伴随症状,n (%) | ||
| 头晕 | 39 (39.4) | 13 (43.3) |
| 恶心 | 79 (79.8) | 26 (86.7) |
| 呕吐 | 65 (65.7) | 25 (83.3) |
| 畏声 | 74 (74.7) | 24 (80.0) |
| 畏光 | 69 (69.7) | 20 (66.7) |
| 其他 | 50 (50.5) | 14 (46.7) |
| 偏头痛家族史,n (%) | 61 (61.6) | 17 (56.7) |
| 月经相关偏头痛,n (%) | 51 (70.8) | 14 (58.3) |
| 原发性偏头痛类型,n (%) | ||
| 无先兆偏头痛 | 53 (53.5) | 18 (60.0) |
| 先兆性偏头痛 | 43 (43.4) | 11 (36.7) |
| 不清楚 | 39 (3.0) | 1 (3.3) |
| 过去一个月的 MMD中位数 (IQR)、d | 10.0 (5.0-20.0) | 11.0 (6.5-25.0) |
| MMDs频率,n (%) | ||
| 0-3 d | 16/99 (16.2) | 3/30 (10.0) |
| 4-7 d | 21/99 (21.2) | 5/30 (16.6) |
| 8-14 d | 21/99 (21.2) | 8/30 (26.7) |
| ≥15 d | 41/99 (41.4) | 14/30 (46.7) |
| 过去一个月的药物治疗情况,n (%) | ||
| 接受过急性治疗 | 81 (81.8) | 26 (86.7) |
| 接受过预防性治疗 | 35 (35.4) | 19 (63.3) |
| 接受过急性和预防性治疗 | 24 (24.2) | 15 (50.0) |
| 过去一个月发生AE, n (%) | 42 (42.4) | 16 (53.3) |
| 过去一个月药物应答情况, n (%) | ||
| 对任一急性治疗无应答 | 20 (20.2) | 20 (66.7) |
| 对任一预防性治疗无应答 | 16 (16.2) | 16 (53.3) |
| 对任一急性或预防性治疗无应答 | 30 (30.3) | 30 (100.0) |
| HIT-6*得分、平均值(SD) | 65.6 (6.7) | 68.8 (5.3) |
| 严重影响 (60-78),n (%) | 84 (87.5) | 28 (96.6) |
| 重大影响 (56-59),n (%) | 6 (6.2) | 1 (3.45) |
| 一些影响 (50-55),n (%) | 4 (4.2) | 0 (0.0) |
| 轻微或无影响 (36-49),n (%) | 2 (2.1) | 0 (0.0) |
| MSQ#得分,平均值(SD) | ||
| 角色限制 | 45.0 (20.5) | 35.6 (20.5) |
| 角色预防 | 51.1 (22.0) | 42.0 (22.4) |
| 情绪功能 | 57.5 (26.6) | 43.6 (27.2) |
*HIT-6,头痛影响测评量表-6,用于评估头痛对患者日常生活影响的简短问卷,HIT-6得分越高代表偏头痛越严重,对患者日常生活影响越大
#MSQ,共含有3个维度:角色限制维度,角色妨碍维度和情感功能维度,分别检测偏头痛导致正常功能受限的程度,干扰正常活动的程度以及偏头痛对情绪的作用(0-100分,分越高越好)
AE,不良事件;MMD,每月偏头痛天数;BMI,身体质量指数
瑞美吉泮对既往治疗失败的患者同样有显著效果
PNR亚组*瑞美吉泮治疗后 2h ,经历中度至重度疼痛的患者比例 下降至34.5% , 48h 降至7.4%
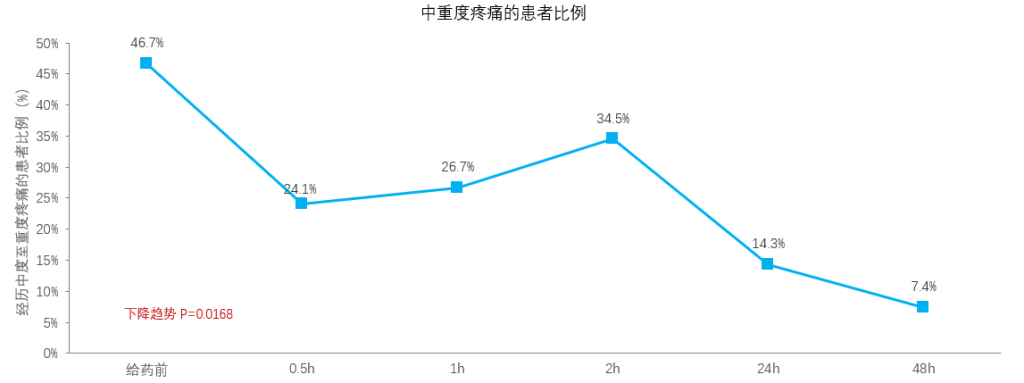
*PNR亚组:入组前1个月对任何急性或预防性偏头痛治疗药物无反应
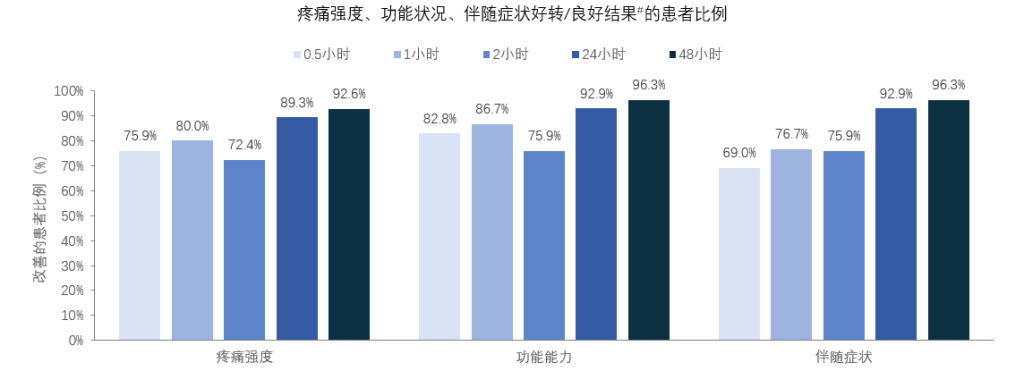
瑞美吉泮急性治疗可以有效改善有治疗失败史(PNR)患者的头痛强度、功能状况和伴随症状
PNR亚组*瑞美吉泮治疗0.5h,约70%的患者在疼痛强度、功能能力、伴随症状方面均达到较好/良好结果
治疗24h升高至约90%,并持续至48h
* PNR亚组:入组前1个月对任何急性或预防性偏头痛治疗药物无反应;
#疼痛程度好转/良好:疼痛强度较用药前有任何程度的降低(好转)或仅为轻度疼痛或无痛(良好);功能状况好转/良好:功能状况较用药前有任何程度的改善(好转)或仅为轻度受损或功能正常(良好);伴随症状好转/良好:伴随症状的数量较用药前有任何降低(好转)或无任何伴随症状(良好)
联合单抗(RE)组表现为更重的伴随症状,偏头痛发作频率更高
RE(联合单抗)组与FP(全人群)相比:伴3种及以上伴随症状患者比例更高 (87.0% vs. 77.8%)、呕吐患者更多 (82.6% vs. 65.7%)、畏声患者更多 (87.0% vs. 74.7%),偏头痛发作频率高:MMDs 15 vs 10,≥ 15 MMDs (60.9% vs. 41.4%) ,使用预防治疗的患者比例更高 (43.5% vs. 35.4%)
| 人口学特征 | FP(n=99) | RE(n=23) |
|---|---|---|
| 年龄,平均值(SD), y | 41.4 (10.4) | 42.2 (10.3) |
| 女性,n (%) | 72 (72.7) | 16 (69.6) |
| BMI,平均值 (SD), kg/m2 | 22.7 (3.5) | 23.5 (3.8) |
| 偏头痛发作年龄,平均值(SD), y | 19.8 (9.1) | 19.7 (9.5) |
| 伴随症状的数量,n (%) | ||
| 0 | 2 (2.0) | 0 (0.0) |
| 1 | 7 (7.1) | 1 (4.4) |
| 2 | 13 (13.1) | 2 (8.7) |
| ≥3 | 77 (77.8) | 20 (87.0) |
| 伴随症状,n (%) | ||
| 头晕 | 39 (39.4) | 11 (47.8) |
| 恶心 | 79 (79.8) | 19 (82.6) |
| 呕吐 | 65 (65.7) | 19 (82.6) |
| 畏声 | 74 (74.7) | 20 (87.0) |
| 畏光 | 69 (69.7) | 16 (69.6) |
| 其他 | 50 (50.5) | 10 (43.5) |
| 偏头痛家族史,n (%) | 61 (61.6) | 14 (60.9) |
| 月经相关偏头痛,n (%) | 51 (70.8) | 12 (75.0) |
| 原发性偏头痛类型,n (%) | ||
| 无先兆偏头痛 | 53 (53.5) | 16 (69.6) |
| 先兆性偏头痛 | 43 (43.4) | 7 (30.4) |
| 不清楚 | 39 (3.0) | 0 (0.0) |
| 过去一个月的 MMD中位数 (IQR)、d | 10.0 (5.0-20.0) | 15.0 (7.5-20.5) |
| MMDs频率,n (%) | ||
| 0-3 d | 16/99 (16.2) | 0/23 (0.0) |
| 4-7 d | 21/99 (21.2) | 6/23 (26.1) |
| 8-14 d | 21/99 (21.2) | 3/23 (13.0) |
| ≥15 d | 41/99 (41.4) | 14/23 (60.9) |
| 过去一个月的药物治疗情况,n (%) | ||
| 接受过急性治疗 | 81 (81.8) | 18 (78.3) |
| 接受过预防性治疗 | 35 (35.4) | 10 (43.5) |
| 接受过急性和预防性治疗 | 24 (24.2) | 7 (30.4) |
| 过去一个月发生AE, n (%) | 42 (42.4) | 13 (56.5) |
| 过去一个月药物应答情况, n (%) | ||
| 对任一急性治疗无应答 | 20 (20.2) | 4 (17.4) |
| 对任一预防性治疗无应答 | 16 (16.2) | 5 (21.7) |
| 对任一急性或预防性治疗无应答 | 30 (30.3) | 7 (30.4) |
| HIT-6*得分、平均值(SD) | 65.6 (6.7) | 65.5 (6.4) |
| 严重影响 (60-78),n (%) | 84 (87.5) | 18 (81.8) |
| 重大影响 (56-59),n (%) | 6 (6.2) | 3 (13.6) |
| 一些影响 (50-55),n (%) | 4 (4.2) | 1 (4.5) |
| 轻微或无影响 (36-49),n (%) | 2 (2.1) | 0 (0.0) |
| MSQ#得分,平均值(SD) | ||
| 角色限制 | 45.0 (20.5) | 44.8 (21.3) |
| 角色预防 | 51.1 (22.0) | 50.4 (22.6) |
| 情绪功能 | 57.5 (26.6) | 58.0 (26.1) |
*HIT-6,头痛影响测评量表-6,用于评估头痛对患者日常生活影响的简短问卷,HIT-6得分越高代表偏头痛越严重,对患者日常生活影响越大
#MSQ,共含有3个维度:角色限制维度,角色妨碍维度和情感功能维度,分别检测偏头痛导致正常功能受限的程度,干扰正常活动的程度以及偏头痛对情绪的作用(0-100分,分越高越好)
AE,不良事件;MMD,每月偏头痛天数;BMI,身体质量指数
瑞美吉泮可有效治疗CGRP单抗治疗期间的突破性偏头痛发作
瑞美吉泮治疗后 2h,RE亚组*经历中度至重度疼痛的患者比例 下降至17.4%,48h降至 8.7%
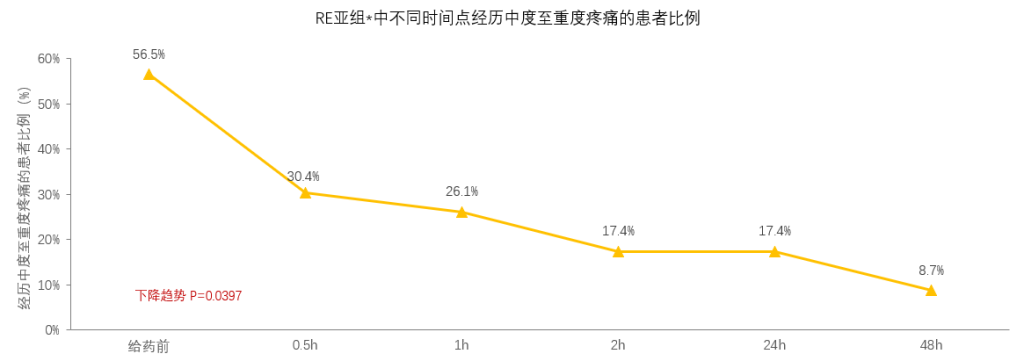
*RE亚组:使用瑞美吉泮治疗偏头痛发作,使用艾普奈珠单抗预防
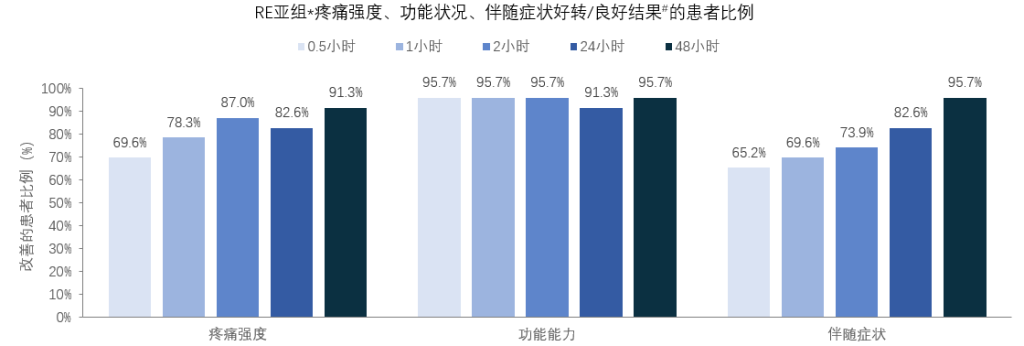
瑞美吉泮急性治疗可以有效改善突破性偏头痛患者的头痛强度、功能状况和伴随症状
RE亚组*瑞美吉泮治疗 0.5h即有 超过60%的患者在疼痛强度、功能状况、伴随症状方面均实现好转/良好,
治疗 24h升高至80%以上,在 48h进一步提高至90%以上
* PNR亚组:入组前1个月对任何急性或预防性偏头痛治疗药物无反应;
#疼痛程度好转/良好:疼痛强度较用药前有任何程度的降低(好转)或仅为轻度疼痛或无痛(良好);功能状况好转/良好:功能状况较用药前有任何程度的改善(好转)或仅为轻度受损或功能正常(良好);伴随症状好转/良好:伴随症状的数量较用药前有任何降低(好转)或无任何伴随症状(良好)
极高发作频率(MMD ≥15)的患者基线特征
VHFM(极高发作频率)组与FP(全人群)相比:偏头痛发作年龄更小(19.8 vs. 10.7岁)、过去一个月的MMD中位数更大(10.0 vs. 21.0天),过去一个月发生的AE更多(42.4% vs. 51.2%),对预防性治疗无应答的比例更高(16.2% vs. 24.4%)
| 人口学特征 | FP(n=99) | VHFM(n=41) |
|---|---|---|
| 年龄,平均值(SD), y | 41.4 (10.4) | 41.0 (11.0) |
| 女性,n (%) | 72 (72.7) | 28 (68.3) |
| BMI,平均值 (SD), kg/m2 | 22.7 (3.5) | 22.8 (3.5) |
| 偏头痛发作年龄,平均值(SD), y | 19.8 (9.1) | 10.7 (9.0) |
| 伴随症状的数量,n (%) | ||
| 0 | 2 (2.0) | 0 (0.0) |
| 1 | 7 (7.1) | 5 (12.2) |
| 2 | 13 (13.1) | 6 (14.6) |
| ≥3 | 77 (77.8) | 30 (73.2) |
| 伴随症状,n (%) | ||
| 头晕 | 39 (39.4) | 16 (39.0) |
| 恶心 | 79 (79.8) | 28 (68.3) |
| 呕吐 | 65 (65.7) | 26 (63.4) |
| 畏声 | 74 (74.7) | 30 (73.2) |
| 畏光 | 69 (69.7) | 25 (61.0) |
| 其他 | 50 (50.5) | 23 (56.1) |
| 偏头痛家族史,n (%) | 61 (61.6) | 24 (58.5) |
| 月经相关偏头痛,n (%) | 51 (70.8) | 16 (57.1) |
| 原发性偏头痛类型,n (%) | ||
| 无先兆偏头痛 | 53 (53.5) | 28 (68.3) |
| 先兆性偏头痛 | 43 (43.4) | 13 (31.7) |
| 不清楚 | 39 (3.0) | 0 (0.0) |
| 过去一个月的 MMD中位数 (IQR)、d | 10.0 (5.0-20.0) | 21.0 (16.0-28.0) |
| MMDs频率,n (%) | ||
| 0-3 d | 16/99 (16.2) | |
| 4-7 d | 21/99 (21.2) | |
| 8-14 d | 21/99 (21.2) | |
| ≥15 d | 41/99 (41.4) | |
| 过去一个月的药物治疗情况,n (%) | ||
| 接受过急性治疗 | 81 (81.8) | 34 (82.9) |
| 接受过预防性治疗 | 35 (35.4) | 16 (39.0) |
| 接受过急性和预防性治疗 | 24 (24.2) | 11 (26.8) |
| 过去一个月发生AE, n (%) | 42 (42.4) | 21 (51.2) |
| 过去一个月药物应答情况, n (%) | ||
| 对任一急性治疗无应答 | 20 (20.2) | 7 (17.1) |
| 对任一预防性治疗无应答 | 16 (16.2) | 10 (24.4) |
| 对任一急性或预防性治疗无应答 | 30 (30.3) | 14 (34.1) |
| HIT-6*得分、平均值(SD) | 65.6 (6.7) | 67.4 (6.1) |
| 严重影响 (60-78),n (%) | 84 (87.5) | 36 (90.0) |
| 重大影响 (56-59),n (%) | 6 (6.2) | 4 (10.0) |
| 一些影响 (50-55),n (%) | 4 (4.2) | 0 (0.0) |
| 轻微或无影响 (36-49),n (%) | 2 (2.1) | 0 (0.0) |
| MSQ#得分,平均值(SD) | ||
| 角色限制 | 45.0 (20.5) | 35.9 (20.3) |
| 角色预防 | 51.1 (22.0) | 43.9 (22.7) |
| 情绪功能 | 57.5 (26.6) | 51.7 (28.0) |
*HIT-6,头痛影响测评量表-6,用于评估头痛对患者日常生活影响的简短问卷,HIT-6得分越高代表偏头痛越严重,对患者日常生活影响越大
#MSQ,共含有3个维度:角色限制维度,角色妨碍维度和情感功能维度,分别检测偏头痛导致正常功能受限的程度,干扰正常活动的程度以及偏头痛对情绪的作用(0-100分,分越高越好)
AE,不良事件;MMD,每月偏头痛天数;BMI,身体质量指数
极高发作频率(MMD ≥15)的患者接受瑞美吉泮急性治疗,中重度患者的比例同样显著降低
VHFM组*的患者,瑞美吉泮治疗后中重度患者比例从治疗前的48.8%降低至48h后的16.2%
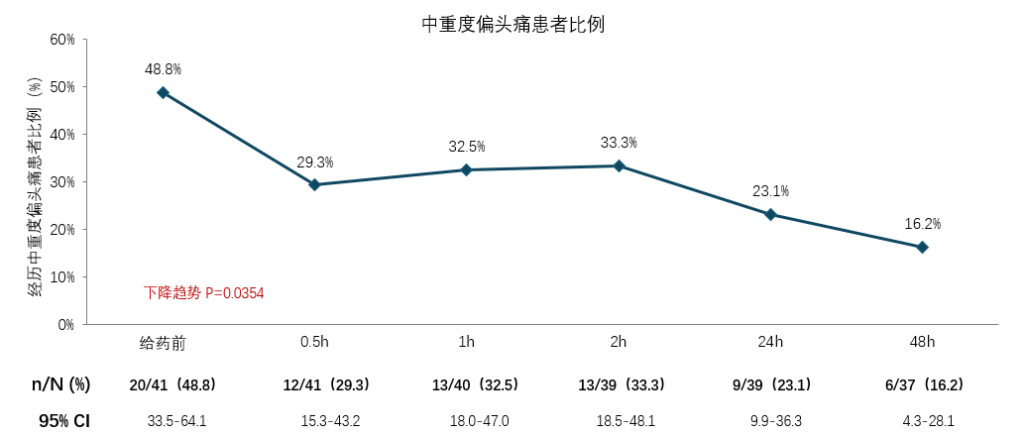
* VHFM亚组:MMDs≥15的患者
MMD,每月偏头痛天数
停用预防用药的情况下瑞美吉泮疗效依然好

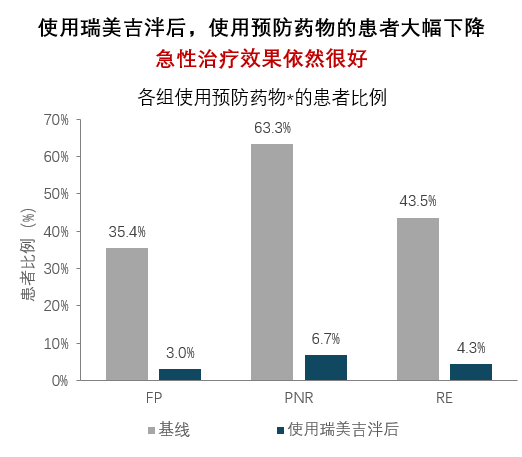
*除艾普奈珠单抗以外的其他预防治疗药物
FP:所有入组患者;PNR亚组:入组前1个月对任何急性或预防性偏头痛治疗药物无反应;RE亚组:使用瑞美吉泮治疗偏头痛发作,使用艾普奈珠单抗预防

真实世界研究样本量小,患者比例容易更高!
真实世界研究中瑞美吉泮的安全性良好
- 全人群(FP)的不良事件发生率为6.1%,治疗失败史(PNR)组为13.3%,联用单抗(RE)组为4.3%
- 所有不良事件均为轻度,最常报告的不良事件是腹部胀气、胃部胀气、胃部不适、恶心、失眠、嗜睡、头晕等
- 没有患者出现“尿路感染”、“尿检异常”等临床医生比较关心的AE
瑞美吉泮治疗常见的不良事件
| 不良事件,n(%) | FP组(n=99) | PNR组(n=30) | RE组(n=23) |
|---|---|---|---|
| 任何不良事件 | 6(6.1) | 4(13.3) | 1(4.3) |
| 最常见的不良事件 | |||
| 腹胀 | 2(2.0) | 2(6.7) | 0 |
| 胃胀 | 2(2.0) | 2(6.7) | 0 |
| 流涎症 | 1(1.0) | 1(3.3) | 1(4.3) |
| 嗜睡 | 1(1.0) | 1(3.3) | 0 |
| 胃部不适 | 1(1.0) | 1(3.3) | 0 |
| 眩晕 | 1(1.0) | 1(3.3) | 0 |
| 恶心 | 1(1.0) | 0 | 0 |
| 失眠 | 1(1.0) | 0 | 0 |
FP:所有入组患者;PNR亚组:入组前1个月对任何急性或预防性偏头痛治疗药物无反应;RE亚组:使用瑞美吉泮治疗偏头痛发作,使用艾普奈珠单抗预防
一、真实世界研究纳入的患者病情重
平均基线MMD高达10天左右,且一半左右的患者可能是慢性偏头痛;
近80%的患者伴随症状数量≥3种;
近90%的患者功能严重受损
二、 对于病情重的患者,瑞美吉泮急性治疗偏头痛疗效依然好
瑞美吉泮急性治疗偏头痛可以显著降低中重度患者的比例
- 起效快:服药后半小时,中重度头痛比例较基线下降约50%
- 疗效持久:服药后48小时,中重度头痛患者比例降到10%或以下
瑞美吉泮急性治疗偏头痛可以明显改善患者的疼痛程度、功能状况和伴随症状
- 起效快:服药后半小时,好转/良好的患者比例高(疼痛:70%及以上;功能:80%以上;伴随症状:65%以上)
- 疗效持久:服药后48小时,好转/良好的患者比例均在90%之上
瑞美吉泮急性治疗既往治疗失败(急性/预防)的患者有效
瑞美吉泮急性治疗正在使用CGRP单抗的突破性偏头痛有效
瑞美吉泮急性治疗极高频率偏头痛(MMD≥15天)患者有效
三、 瑞美吉泮急性治疗偏头痛耐受性好,AE发生率低于III期,均为轻度AE,未出现“尿路感染、尿检异常”AE
NCT06221267:本研究是一项前瞻性、单臂、多中心、观察性研究(非干预性)
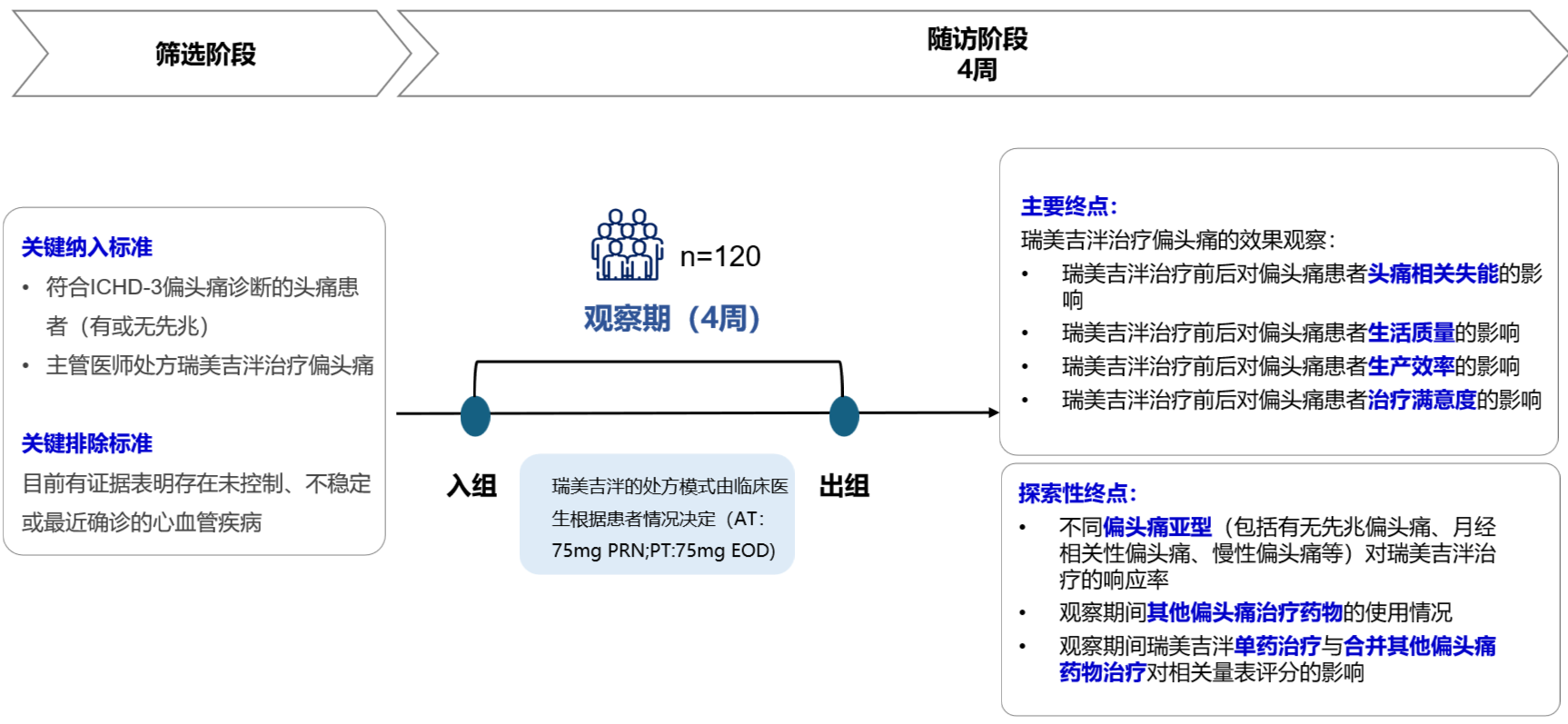
ICHD-3=《国际头痛疾病分类》第3版;PRN=按需;EOD=隔日一次;
基线特征
- 共有108例实际使用了瑞美吉泮用于偏头痛治疗的偏头痛患者纳入分析
- 受试者年龄中位数为37.0岁,其中83.3%为女性,在这些女性患者中,67.8%的患者报告了偏头痛发作与月经周期相关。
- 基线的平均MMD在急性治疗组(AT)为8.1(7.9)
- 最常见的偏头痛类型在AT组是无先兆偏头痛(78.7%)
- 最常见的伴随症状是恶心(84.3%),畏光(60.2%)、畏声(59.3%)和颈部僵硬/疼痛(54.6%)
- 最常见的共病是失眠(29.6%)、焦虑(17.6%)和抑郁(8.3%)
- 47.2%的患者有偏头痛家族史
| 总体 (N=108) | 急性治疗 (N=89) | P值 | |
|---|---|---|---|
| 年龄 (岁), 中位数 (Q1, Q3) | 37.0 (31.5,46.0) | 37.0 (32.0,45.0) | 0.6025 |
| 年龄分组, 例数 (%) | 0.4254 | ||
| 18-30岁 | 24 (22.2) | 18 (20.2) | |
| 31-45岁 | 56 (51.9) | 49 (55.1) | |
| 46-60岁 | 21 (19.4) | 16 (18.0) | |
| ≥ 61岁 | 7 (6.5) | 6 (6.7) | |
| 女性, 例数 (%) | 90 (83.3) | 75 (84.3) | 0.5177 |
| 月经相关性偏头痛a, 例数 (%) | 61/90 (67.8) | 53/75 (70.7) | 0.2227 |
| 偏头痛发病年龄 (岁), 中位数 (Q1, Q3) | 22.0 (17.0,28.0) | 23.0 (17.0,28.5) | 0.2044 |
| MMD, 中位数 (SD) | 9.4 (8.7) | 8.1 (7.9) | 0.0026 |
| MMD分组, 例数 (%) | 0.0142 | ||
| ≤3 | 29 (26.9) | 26 (29.2) | |
| [4,14] | 55 (50.9) | 48 (53.9) | |
| ≥15 | 24 (22.2) | 15 (16.9) | |
| 偏头痛类型, 例数 (%) | <.0001 | ||
| 无先兆偏头痛 | 76 (70.4) | 70 (78.7) | |
| 有先兆偏头痛 | 12 (11.1) | 10 (11.2) | |
| 慢性偏头痛 | 19 (17.6) | 8 (9.0) | |
| 其他 | 1 (0.9) | 1 (1.1) | |
| 伴随症状, 例数 (%) | |||
| 恶心 | 91 (84.3) | 76 (85.4) | 0.4946 |
| 呕吐 | 55 (50.9) | 44 (49.4) | 0.5033 |
| 畏光 | 65 (60.2) | 53 (59.6) | 0.7706 |
| 畏声 | 64 (59.3) | 52 (58.4) | 0.7032 |
| 颈部僵硬/疼痛 | 59 (54.6) | 45 (50.6) | 0.0661 |
| 合并疾病, 例数 (%) | |||
| 已控制的心血管疾病 | 7 (6.5) | 5 (5.6) | 0.6040 |
| 糖尿病 | 3 (2.8) | 2 (2.2) | 0.4437 |
| 抑郁 | 9 (8.3) | 3 (3.3) | 0.0008 |
| 焦虑 | 19 (17.6) | 12 (13.5) | 0.0403 |
| 失眠 | 32 (29.6) | 25 (28.1) | 0.4482 |
| 偏头痛家族史, 例数 (%) | 51 (47.2) | 40 (44.9) | 0.3047 |
| 父母 | 47 (43.5) | 38 (42.7) | |
| 祖父母 | 8 (7.4) | 6 (6.7) | |
| 兄弟姐妹 | 7 (6.5) | 3 (3.4) |
a 经期相关偏头痛的患病率是基于女性患者的自我报告数据进行评估的。
急性治疗显著改善患者失能、生活质量、工作效率以及治疗满意度
急性治疗 (N=88) | ||
|---|---|---|
| 平均变化 (95%CI) | p值 | |
| TSQMa | ||
| 有效性 | 20.6 (14.3, 26.8) | <0.0001 |
| 不良反应 | 12.6 (6.8, 18.5) | <0.0001 |
| 便利性 | 4.3 (0.4, 8.2) | 0.058 |
| 总体满意度 | 16.2 (10.8, 21.5) | <0.0001 |
| EQ-5D-5L | ||
| VAS | 3.6 (1.0, 6.2) | 0.019 |
| 效用值 | 0.01 (-0.01, 0.03) | 0.22 |
| WPAI-GH | ||
| 缺勤(错过工作时间)b | -4.2 (-8.1, -0.3) | 0.054 |
| 出勤(工作障碍/工作效率降低)c | -10.6 (-18.7, -2.5) | 0.018 |
| 总体工作损失c | -11.3 (-19.8, -2.9) | 0.021 |
| 工作生产力损失 | -12.3 (-18.6, -6.0) | 0.0003 |
TSQM:药物治疗满意度量表;EQ-5D-L:欧洲五维健康量表;WPAI-GH:工作生产力与活动障碍问卷
观察期间合并用药情况
- 瑞美吉泮治疗4周后,AT组 观察到急性用药的显著减少 ,包括NSAIDs、曲普坦类药物、对乙酰氨基酚以及含咖啡因的复方制剂等
- 治疗期间其他急性药物使用比例的减少, 不仅预示着瑞美吉泮的疗效,还可能预示着瑞美吉泮减少MOH的潜在疗效。
急性治疗 (N=88) | |||
|---|---|---|---|
| 基线 | 为期4周的治疗期间 | P值 | |
| 曲普坦, 例数 (%) | 21(23.9) | 6(6.8) | 0.0017 |
| 佐米曲普坦 | 19(21.6) | 5(5.7) | 0.0021 |
| 利扎曲普坦 | 9(10.2) | 1(1.1) | 0.0092 |
| NSAIDs, 例数 (%) | 59(67.0) | 14(15.9) | < 0.0001 |
| 布洛芬 | 49(55.7) | 11(12.5) | < 0.0001 |
| 阿司匹林 | 16(18.2) | 3(3.4) | 0.0016 |
| 氟桂利嗪, No. (%) | 15(17.0) | 7(8.0) | 0.068 |
| 对乙酰氨基酚,例数 (%) | 28(31.8) | 13(14.8) | 0.0075 |
| 含咖啡因的复方制剂, 例数 (%) | 16(18.2) | 3(3.4) | 0.0016 |
NSAIDs:非甾体抗炎药
单药组和联合治疗组的事后分析
- 同时对瑞美吉泮单药组和瑞美吉泮合和其他偏头痛药物的联合治疗组进行事后分析,发现瑞美吉泮单药组与联合治疗组的各量表的改善趋势一致,并且单药治疗效果与联合治疗相当 (大多数P值没有显著差异)
急性治疗 (N=88) | |||
|---|---|---|---|
| 单药治疗 | 联合治疗 | P值 | |
平均变化 (95% CI) | |||
| TSQMa | |||
| 有效性 | 29.3(21.7,36.8) | 9.4(-0.4,19.1) | 0.0009 |
| 不良反应 | 9.7(2.5,16.9) | 16.4(6.4,26.5) | 0.2804 |
| 便利性 | 7.5(3.1,11.9) | 0.1(-6.7,7.0) | 0.0414 |
| 总体满意度 | 23.9(17.5,30.3) | 6.2(-2.1,14.5) | 0.0002 |
| EQ-5D-5L | |||
| VAS | 3.5(0.7,6.4) | 3.6(-1.2,8.5) | 0.4216 |
| 效用值 | 0.02(-0.01,0.04) | 0.00(-0.04,0.05) | 0.5621 |
| WPAI-GH | |||
| 缺勤(错过工作时间)b | -4.6(-9.8,0.7) | -3.6(-9.9,2.7) | 0.8955 |
| 出勤(工作障碍/工作效率降低)c | -12.4(-24.9,0.0) | -7.7(-16.8,1.3) | 0.7870 |
| 总体工作损失 | -13.5(-26.4, -0.6) | -8.0(-17.6,1.7) | 0.8026 |
| 工作生产力损失 | -15.1(-24.7, -5.5) | -8.7(-16.7, -0.7) | 0.4239 |
TSQM:药物治疗满意度量表;EQ-5D-L:欧洲五维健康量表;WPAI-GH:工作生产力与活动障碍问卷
无先兆偏头痛诊断标准(ICHD-3)
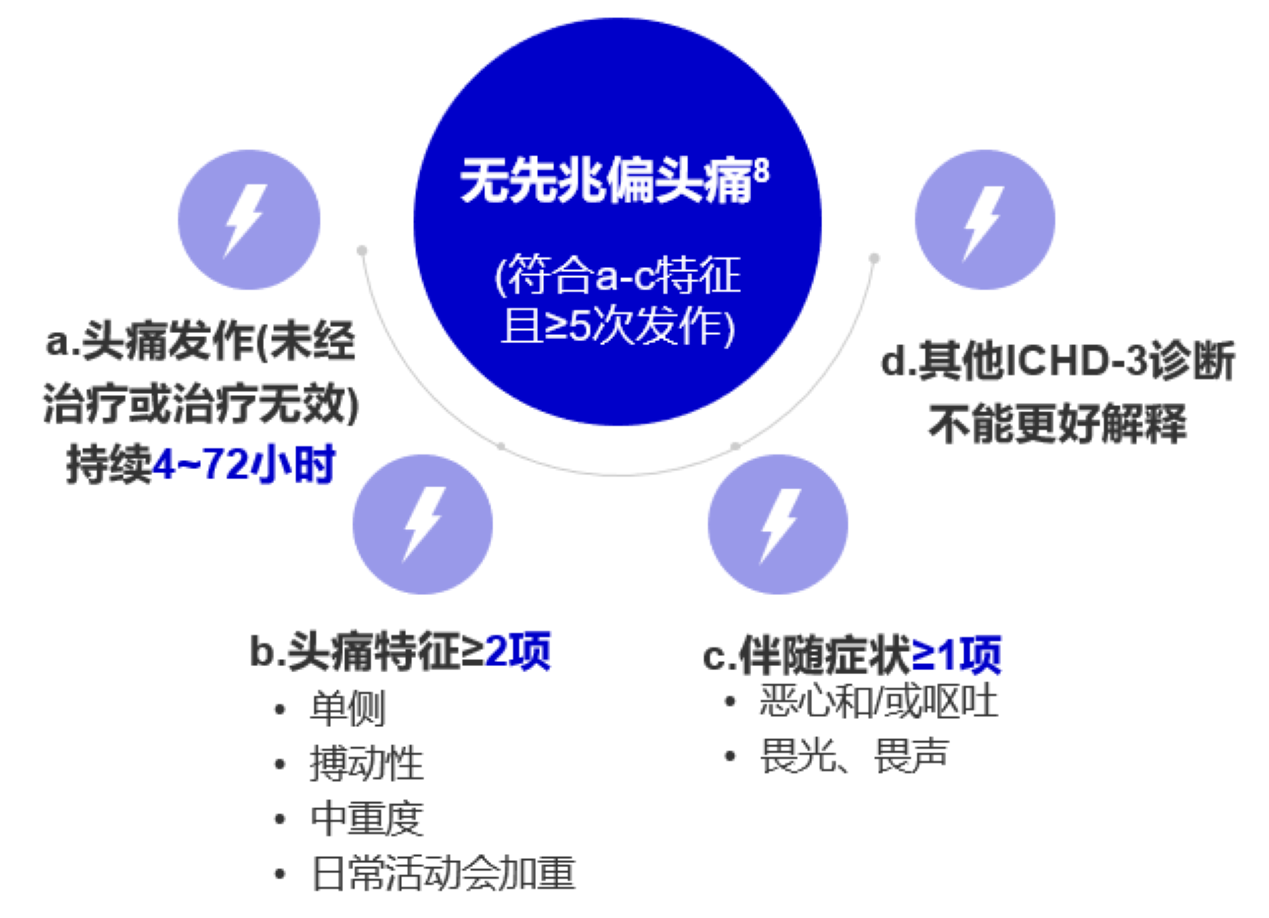
国际头痛疾病分类(ICHD),由国际头痛协会(IHS)发布,目前为2018年出版的第三版ICHD-38
有先兆偏头痛诊断标准(ICHD-3)
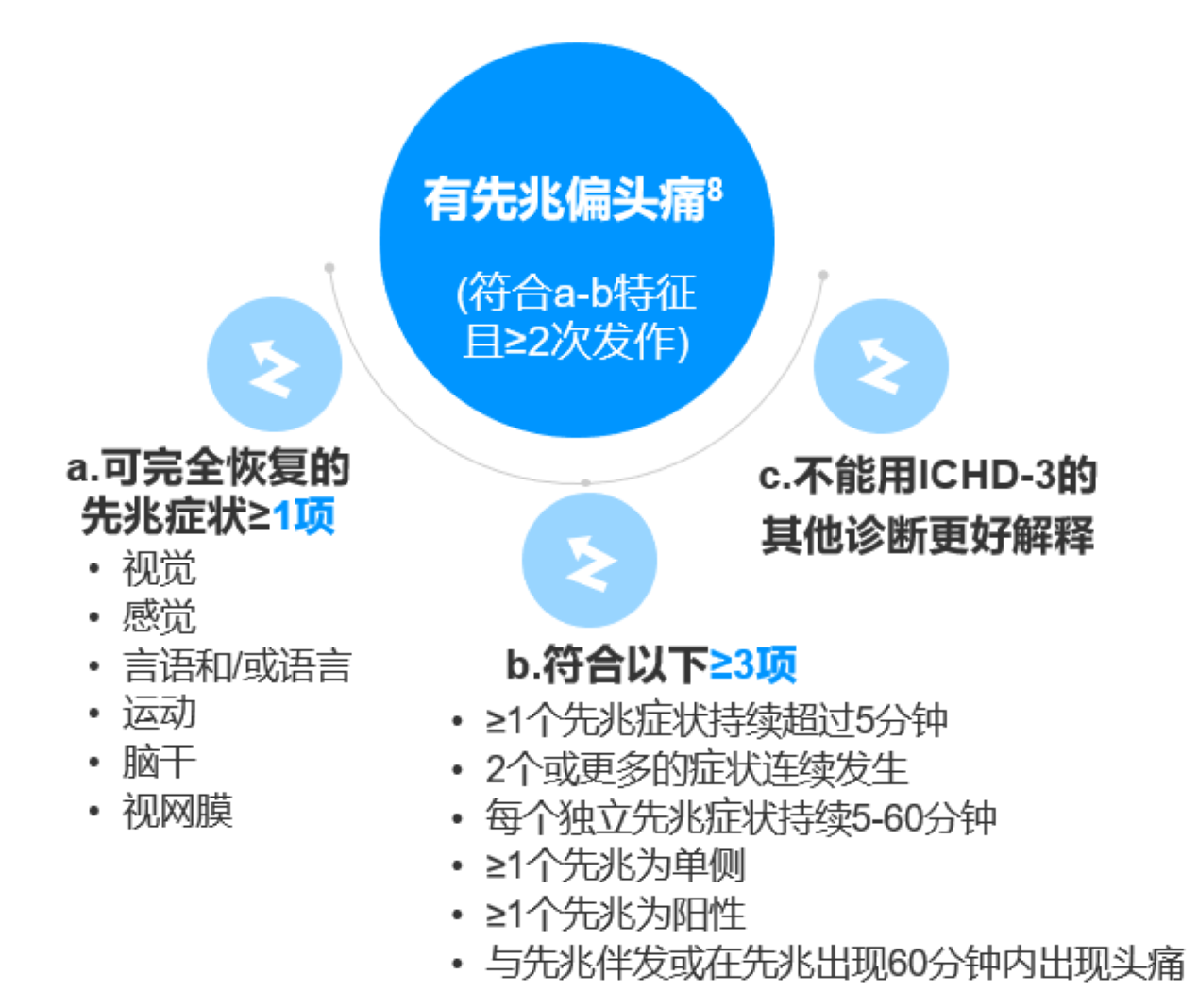
国际头痛疾病分类(ICHD),由国际头痛协会(IHS)发布,目前为2018年出版的第三版ICHD-38
发作性偏头痛和慢性偏头痛诊断标准(ICHD-3)
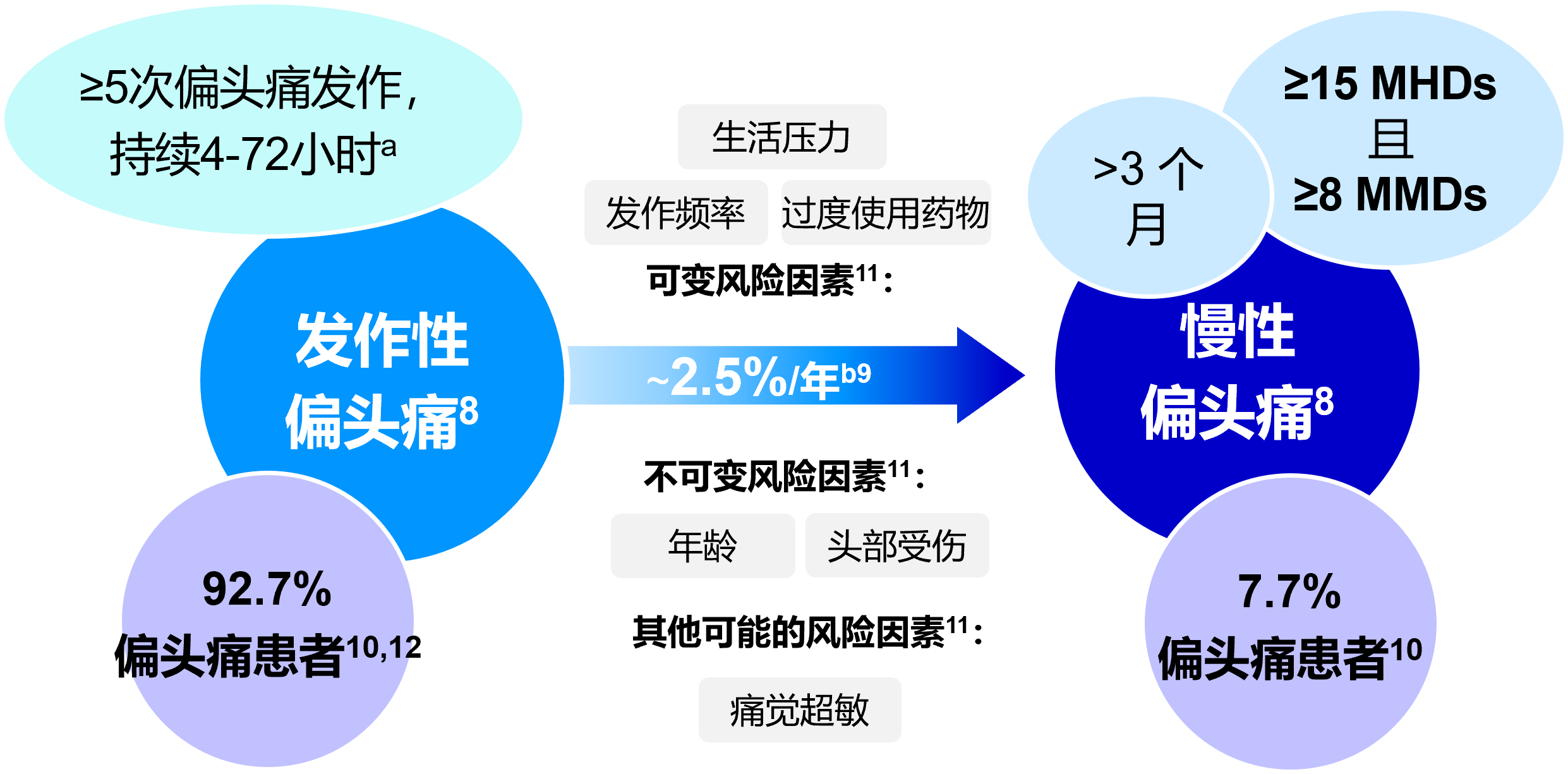
a 不符合慢性偏头痛标准的人
b 每年有2.5%的发作偏头痛患者发展为慢性偏头痛
ICHD-3:国际头痛疾病分类,第3版;MHD:每月头痛天数;MMD:每月偏头痛天数




- 偏头痛医疗质量控制指标中国专家共识(第一版)
- 头痛问诊要领中国专家建议(2025版)
- 药物过度使用性头痛诊断与治疗中国专家共识2025(中华医学会神经病学分会第一版)
- 中国前庭性偏头痛诊治指南(2026)
- 月经性偏头痛诊断和治疗中国专家共识(2025版)
- 美国内科医师学会(ACP)临床指南:门诊环境下发作性偏头痛的急性治疗(Pharmacologic treatments of acute episodic migraine headache in outpatient settings: A clinical guideline from the American College of Physicians)
- 意大利头痛研究学会(SISC)/国际头痛协会(IHS)循证指南:偏头痛的药物治疗(Evidence-based guidelines for the pharmacological treatment of migraine)
- SISC/IHS循证指南:偏头痛的药物治疗(简版)(Evidence-based guidelines for the pharmacological treatment of migraine, summary version)
- 通过德尔菲法达成对难治性偏头痛定义的国际共识(Reaching international consensus on the definition of refractory migraine using the Delphi method)
- 中国药物过度使用性头痛诊治指南(第一版)
- 法国头痛学会对偏头痛治疗的立场文件(Migraine treatment: Position paper of the French Headache Society)
- 月经性偏头痛诊断与治疗中国专家共识
- 成人原发性头痛的规范化管理:泛长三角头痛诊疗专家建议(2024)
- 中国偏头痛急性期治疗指南(第一版)
- 2024 IHS全球实践建议:偏头痛的急性药物治疗(International Headache Society global practice recommendations for the acute pharmacological treatment of migraine)
请注意:我们不建议超出国家药品监督管理局批准的药品说明书的应用或未在中国(不含港澳台)上市药品的应用。如我们所提供的文献信息及指南共识涉及该等内容,系出于传递科学知识的需要,不应视为对未在中国(不含港澳台)上市药品或已在中国上市但超出国家药品监督管理局批准的药品说明书的药品适应症/用法的推广。
- 乐泰可(硫酸瑞美吉泮口崩片)说明书
- Vydura (rimegepant) Package Insert. Pfizer Europe Inc.
- Yu S, Kim BK, Guo A, et al. Safety and efficacy of rimegepant orally disintegrating tablet for the acute treatment of migraine in China and South Korea: a phase 3, double-blind, randomised, placebo-controlled trial. Lancet Neurol. 2023 Jun;22(6):476-484.
Zhang M, Guo A, Wu J, et al. Rimegepant for the acute treatment of migraine: A phase 3, multicenter, open-label, long-term safety and effectiveness study in adults from China. Cephalalgia. 2025 Oct;45(10):3331024251371686
- Croop R, Goadsby PJ, Stock DA, et al. Efficacy, safety, and tolerability of rimegepant orally disintegrating tablet for the acute treatment of migraine: a randomised, phase 3, double-blind, placebo-controlled trial. Lancet. 2019 Aug;31;394(10200):737-745.
- Yu S, Guo A, Wang Z, et al. Rimegepant orally disintegrating tablet 75 mg for acute treatment of migraine in adults from China: a subgroup analysis of a double-blind, randomized, placebo-controlled, phase 3 clinical trial. J Headache Pain. 2024 Apr 16;25(1):57
- Yu S, Lu Z, Liu Y, et al. Efficacy of rimegepant for the acute treatment of migraine in Chinese and Korean adults receiving concurrent preventive medication. Poster session presented at: Inernational Headache Congress; 2023 Sept 14-17; Seoul, South Korea.
- Headache Classification Committee of the International Headache Society (IHS) The International Classification of Headache Disorders, 3rd edition. Cephalalgia. 2018;38(1):1-211.
- Katsarava Z, Buse DC, Manack AN, et al. Defining the differences between episodic migraine and chronic migraine. Curr Pain Headache Rep. 2012 Feb;16(1):86-92.
- Buse DC, Manack AN, Fanning KM, et al. Chronic migraine prevalence, disability, and sociodemographic factors: results from the American Migraine Prevalence and Prevention Study. Headache. 2012 Nov-Dec;52(10):1456-70.
- Bigal ME, Lipton RB. Modifiable risk factors for migraine progression. Headache. 2006 Oct;46(9):1334-43.
- Dodick DW, Loder EW, Manack Adams A, et al. Assessing barriers to chronic migraine consultation, diagnosis, and treatment: results from the chronic migraine epidemiology and outcomes (CaMEO) study. Headache. 2016 May;56(5):821-834.
- 郭政, 等. 疼痛诊疗学第4版. 人民卫生出版社. 2016.
- 冷希圣,韦军民,刘连新, 等. 普通外科围手术期疼痛处理专家共识[J]. 中华普通外科杂志, 2015,30(2):166-173.
- Eigenbrodt AK, Ashina H, Khan S, et al. Diagnosis and management of migraine in ten steps. Nat Rev Neurol. 2021 Aug;17(8):501-514.
- Rapoport AM, Bigal ME. ID-migraine. Neurol Sci. 2004 Oct;25 Suppl 3:S258-60.
- Láinez MJ, Domínguez M, Rejas J, et al. Development and validation of the Migraine Screen Questionnaire (MS-Q). Headache. 2005 Nov-Dec;45(10):1328-38.
- Yang Z, Wang X, Niu M, et al. First real-world study on the effectiveness and tolerability of rimegepant for acute migraine therapy in Chinese patients. J Headache Pain. 2024 Sep 27;25(1):160
- Wang J, Jiang J, Peng S, et al. Patient-reported outcomes of rimegepant for acute and preventive treatment of migraine in China: a prospective, multicenter, real-world study. J Headache Pain. 2025 Nov 7;26(1):242



