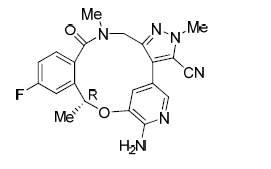
请仔细阅读说明书并在医师指导下使用
本品单药适用于间变性淋巴瘤激酶(ALK)阳性的局部晚期或转移性非小细胞肺癌患者的治疗。
(1)25 mg;(2)100 mg
患者选择
经验证的检测方法证实为ALK阳性的局部晚期或转移性NSCLC患者方可使用本品(见【适应症】)和【临床试验】)。
推荐剂量
本品的推荐剂量为每日一次口服 100 mg(与食物同服或不同服),直至疾病进展或出现不可耐受的毒性(见【药代动力学】)。
应整片吞服,不要咀嚼、掰碎或分割药片。若药片出现破损、裂纹或其他不完整的情况,请勿服用。
每天在大致相同的时间服用本品。如果错过了某次剂量,可以补服漏服的剂量,除非距下次给药时间在 4 小时以内。不要一次服用两次剂量药物以补服漏服的剂量。
如果在服用本品后发生了呕吐,不要服用追加剂量,应在下一次给药时间继续服用推荐剂量。
针对不良反应的剂量调整
推荐的剂量降低方法如下:
- 第一次降低剂量:每日一次口服75 mg
- 第二次降低剂量:每日一次口服50 mg
对于不能耐受每日一次口服 50 mg 的患者,则永久停用本品。
表 1 提供了针对本品不良反应的剂量调整。
表 1 针对本品不良反应的剂量调整建议
| 不良反应a | 剂量调整 |
|---|---|
| 中枢神经系统影响(见【注意事项】) | |
| 1 级 | 按相同剂量水平继续用药或暂停用药直到恢复至基线。以相同剂量或降低一个剂量水平继续服用本品。 |
| 2 级 或 3 级 | 暂停服用本品,直到恢复至 0 或 1 级。降低一个剂量水平继续服用本品。 |
| 4 级 | 永久停用本品。 |
| 高脂血症(见【注意事项】) | |
| 4 级高胆固醇血症 或 4 级高甘油三酯血症 | 暂停服用本品,直到高胆固醇血症和/或高甘油三酯血症恢复至 2 级或以下。以相同剂量继续服用本品。 如果重度高胆固醇血症和/或高甘油三酯血症复发,则降低一个剂量水平继续服用本品。 |
| 房室 (AV) 传导阻滞(见【注意事项】) | |
| 二度房室传导阻滞 | 暂停服用本品,直到 PR 间期小于 200 ms。降低一个剂量水平继续服用本品。 |
| 首次出现完全性房室传导阻滞 | 暂停服用本品,直到
|
| 再次出现完全性房室传导阻滞 | 植入起搏器或永久停用本品。 |
| 间质性肺病 (ILD)/非感染性肺炎(见【注意事项】) | |
| 任何级别的与治疗相关的 ILD/非感染性肺炎 | 永久停用本品。 |
| 高血压(见【注意事项】) | |
| 3 级(收缩压大于或等于 160 mmHg 或舒张压大于或等于 100 mmHg;需要进行医疗干预;需要使用一种以上的降压药物,或需要进行比以前更加强化的治疗) | 暂停服用本品直到高血压恢复至 1 级或以下(收缩压小于 140 mmHg 和舒张压小于 90 mmHg),然后以相同剂量继续服用本品。 如果 3 级高血压复发,则暂停服用本品直到高血压恢复至 1 级或以下,并降低一个剂量水平继续服用本品。 如果不能通过最佳的医疗措施有效控制高血压,则永久停用本品。 |
| 4 级(危及生命,需要紧急干预) | 暂停服用本品直到高血压恢复至 1 级或以下,并降低一个剂量水平继续服用本品或永久停用本品。 如果 4 级高血压复发,则永久停用本品。 |
| 高血糖(见【注意事项】) | |
| 3 级(尽管进行了最佳的降糖治疗,但仍大于 250 mg/dL)或 4 级。 | 暂停服用本品直到高血糖得到充分控制,然后降低一个剂量水平继续服用本品。 如果不能通过最佳的医疗措施有效控制高血糖,则永久停用本品。 |
| 其他不良反应 | |
| 1 级 或 2 级 | 以相同剂量或降低一个剂量水平继续服用本品。 |
| 3 级 或 4 级 | 暂停服用本品,直到症状缓解至≤ 2 级或基线。然后降低一个剂量水平继续服用本品。 |
a 根据美国国家癌症研究所 (NCI) 不良事件通用术语标准 (CTCAE) 4.03 版进行分级。
合用强效CYP3A 诱导剂
本品禁用于正在服用强效 CYP3A 诱导剂的患者。停用强效 CYP3A 诱导剂的3个血浆半衰期后,开始服用本品(见【禁忌】、【注意事项】、【药物相互作用】和【药代动力学】)。
合用中效 CYP3A 诱导剂
避免本品与中效 CYP3A 诱导剂合用。如果不能避免与中效 CYP3A 诱导剂合用,则应将本品剂量增加至 125 mg 每日一次(见【药物相互作用】和【药代动力学】)。
针对强效 CYP3A 抑制剂的剂量调整
避免本品与强效 CYP3A 抑制剂合用。如果不能避免与强效 CYP3A 抑制剂合用,则应将本品的起始剂量从每日一次口服 100 mg 减至每日一次口服 75 mg。
如患者因不良反应而将每日口服剂量减至 75 mg,并开始服用强效 CYP3A 抑制剂,则应将本品剂量减至每日一次口服 50 mg。
如果停止合用强效 CYP3A 抑制剂,则应将本品剂量(在停用强效 CYP3A 抑制剂的 3 个血浆半衰期后)增至开始使用强效CYP3A抑制剂之前的剂量(见【药物相互作用】和【药代动力学】)。
针对氟康唑的剂量调整
避免本品与氟康唑合用(见【药代动力学】)。如果不能避免合用,则应将本品的起始剂量从每日一次口服 100 mg 减至每日一次口服 75 mg(见【药物相互作用】和【药代动力学】)。
肝损害
对于轻度肝损害的患者,不建议进行剂量调整(总胆红素 ≤ 正常值上限 [ULN] 伴 AST > ULN,或者总胆红素 > 1 至 1.5 × ULN 伴任何 AST)。尚未确定本品对于中度(总胆红素 ≥ 1.5 至 3.0 × ULN 伴任何 AST)或重度(总胆红素 > 3.0 × ULN 伴任何 AST)肝损害患者的推荐剂量(见【药代动力学】)。
肾损害
对重度(采用 Cockcroft-Gault 公式估算的肌酐清除率 [CLcr] 为 15 至 <30 mL/min)肾损害患者给予本品时应将本品的起始剂量从每日一次口服 100 mg 减至每日一次口服 75 mg。(见【药代动力学】)。
对于轻度或中度肾损害(采用 Cockcroft-Gault 公式估算的CLcr 为 30 至 89 mL/min)的患者,不建议进行剂量调整(见【药代动力学】)。
以下不良反应在说明书的其他部分进行描述:
- 合用强效 CYP3A 诱导剂的严重肝脏毒性风险(见【注意事项】)
- 中枢神经系统影响(见【注意事项】)
- 高脂血症(见【注意事项】)
- 房室传导阻滞(见【注意事项】)
- 间质性肺病/非感染性肺炎(见【注意事项】)
- 高血压(见【注意事项】)
- 高血糖(见【注意事项】)
临床试验经验
由于不同的临床试验在不同的条件下完成,在一种药物的临床试验中观察到的不良反应率不能直接和其他药物的临床试验中的不良反应率相比较,且未必反映实际临床应用中的不良反应率。
【注意事项】项下提供了在研究 B7461001 (N=327) 和研究 B7461006 (N=149) 中接受本品100 mg 每日一次给药的 476 名患者的数据。在 476 名接受本品的患者中,75% 的患者暴露时间为 6 个月或更长,61% 的患者暴露时间超过 1 年。在该合并安全性人群中,476 名接受本品的患者中最常见的不良反应(≥ 20%)为水肿 (56%)、周围神经病 (44%)、体重增加 (31%)、认知影响 (28%)、疲乏 (27%)、呼吸困难 (27%)、关节痛 (24%)、腹泻 (23%)、情绪影响 (21%) 和咳嗽 (21%)。476 名接受本品的患者中最常见的 3-4 级实验室检查值异常(≥ 20%)为高胆固醇血症 (21%) 和高甘油三酯血症 (21%)。
既往未接受过治疗的 ALK 阳性转移性 NSCLC(CROWN 研究)
在一项治疗既往未针对晚期疾病进行系统性治疗的 ALK 阳性、局部晚期或转移性 NSCLC 患者的随机、开放、阳性对照试验中,在 149名ALK阳性NSCLC患者中评估了本品的安全性(见【临床试验】)。本品的中位暴露持续时间为 16.7 个月(4 天至 34.3 个月),76% 的患者接受了至少 12 个月的本品治疗。
接受本品治疗的患者中,有 34% 出现了严重不良反应;最常见的严重不良反应为肺炎 (4.7%)、呼吸困难 (2.7%)、呼吸衰竭 (2.7%)、认知影响 (2.0%) 和发热 (2.0%)。在接受本品治疗的患者中,有 3.4% 出现了致死性不良反应,包括肺炎 (0.7%)、呼吸衰竭 (0.7%)、急性心力衰竭 (0.7%)、肺栓塞 (0.7%)和突然死亡(0.7%)。
6.7% 的患者因不良反应而永久停用本品。导致永久停用本品的最常见不良反应为认知影响 (1.3%)。在接受本品治疗的患者中,有 49% 因不良反应导致中断给药。导致本品中断给药的最常见不良反应为高甘油三酯血症 (7%)、水肿 (5%)、肺炎 (4.7%)、认知影响 (4.0%)、情绪影响 (4.0%)和高胆固醇血症 (3.4%)。在接受本品治疗的患者中,有 21% 因不良反应导致降低剂量。导致降低剂量的最常见不良反应为水肿 (5%)、高甘油三酯血症 (4.0%) 和周围神经病 (3.4%)。
表 2 和表 3 分别汇总了在研究 B7461006 中接受本品治疗的患者的最常见不良反应和实验室检查异常。
表 2 研究 B7461006 中接受本品治疗的患者发生的不良反应(所有 NCI CTCAE 等级 ≥10% 或 3-4 级 ≥2%)*
| 不良反应 | 本品 N=149 | 克唑替尼 N=142 | ||
|---|---|---|---|---|
| 所有等级 (%) | 3 或 4 级 (%) | 所有等级 (%) | 3 或 4 级 (%) | |
| 精神病类 | ||||
| 情绪影响a | 16 | 2 | 5 | 0 |
| 神经系统 | ||||
| 周围神经病b | 34 | 2 | 15 | 0.7 |
| 认知影响c | 21 | 2 | 6 | 0 |
| 头痛 | 17 | 0 | 18 | 0.7 |
| 头晕 | 11 | 0 | 14 | 0 |
| 睡眠影响d | 11 | 1.3 | 10 | 0 |
| 呼吸系统 | ||||
| 呼吸困难 | 20 | 2.7 | 16 | 2.1 |
| 咳嗽 | 16 | 0 | 18 | 0 |
| 呼吸衰竭 | 2.7 | 2 | 0 | 0 |
| 血管性疾病 | ||||
| 高血压 | 18 | 10 | 2.1 | 0 |
| 视觉 | ||||
| 视觉异常e | 18 | 0 | 39 | 0.7 |
| 胃肠道 | ||||
| 腹泻 | 21 | 1.3 | 52 | 0.7 |
| 恶心 | 15 | 0.7 | 52 | 2.1 |
| 便秘 | 17 | 0 | 30 | 0.7 |
| 呕吐 | 13 | 0.7 | 39 | 1.4 |
| 肌肉骨骼和结缔组织 | ||||
| 关节痛 | 19 | 0.7 | 11 | 0 |
| 肌痛f | 15 | 0.7 | 7 | 0 |
| 背痛 | 15 | 0.7 | 11 | 0 |
| 四肢痛 | 17 | 0 | 8 | 0 |
| 一般情况 | ||||
| 水肿g | 56 | 4 | 40 | 1.4 |
| 体重增加 | 38 | 17 | 13 | 2.1 |
| 疲乏h | 19 | 1.3 | 32 | 2.8 |
| 发热 | 17 | 1.3 | 13 | 1.4 |
| 胸痛 | 11 | 1.3 | 14 | 0.7 |
| 感染 | ||||
| 上呼吸道感染i | 11 | 0.7 | 7.7 | 1.4 |
| 肺炎 | 7.4 | 2 | 8.5 | 3.5 |
| 支气管炎 | 6.7 | 2 | 2.1 | 0 |
| 皮肤 | ||||
| 皮疹j | 11 | 0 | 8.5 | 0 |
* 使用 NCI CTCAE 4.03 版对不良反应进行分级。
缩略词:NCI CTCAE=美国国立癌症研究所不良事件通用术语标准;SOC=系统器官分类。
a 情绪影响(包括情感障碍、情感易变、激越、愤怒、焦虑、双相 I 型障碍、抑郁情绪、抑郁、抑郁症状、欣快感、故意自残、易激惹、情绪改变、情绪波动、压力)。
b 周围神经病(包括感觉迟钝、步态障碍、感觉减退、运动功能障碍、肌无力、神经痛、周围神经病、感觉异常、外周运动神经病变、外周感觉神经元病变)。
c 认知影响(包括 SOC 神经系统疾病中的事件:失忆症、认知障碍、注意力障碍、记忆受损、精神损害;还包括 SOC 精神疾病中的事件:意识模糊状态、谵妄、定向障碍)。
d 睡眠影响(包括失眠、梦魇、睡眠障碍、梦游症)
e 视觉异常(包括复视、畏光、闪光幻觉、视物模糊、视觉敏感度减退、视力损害、飞蚊症)。
f 肌痛(包括骨骼肌疼痛、肌痛)。
g 水肿(包括水肿、外周水肿、眼睑水肿、面部水肿、全身水肿、局部水肿、眶周水肿、外周肿胀、肿胀)。
h 疲乏(包括乏力、疲乏)。
i 上呼吸道感染(包括上呼吸道感染)。
j 皮疹(包括痤疮样皮炎、斑丘疹、皮疹)。
发生率在 1% 至 10% 之间的其他具有临床意义的不良反应为语言影响 (6.7%) 和精神影响 (3.4%)。
表 3 研究 B7461006 中在 ≥20% 的患者中较基线发生恶化的实验室检查值异常*
| 实验室检查异常 | 本品 N=149 | 克唑替尼 N=142 | ||
|---|---|---|---|---|
| 所有等级 (%) | 3 或 4 级 (%) | 所有等级 (%) | 3 或 4 级 (%) | |
| 生化检查 | ||||
| 高甘油三酯血症a,A | 95 | 22 | 27 | 0 |
| 高胆固醇血症a,A | 91 | 19 | 12 | 0 |
| 肌酐升高a,A | 81 | 0.7 | 99 | 2.1 |
| GGT 升高a,A | 52 | 6 | 41 | 6 |
| AST 升高a,A | 48 | 2 | 75 | 3.5 |
| 高血糖a,A | 48 | 7 | 27 | 2.1 |
| ALT 升高a,A | 44 | 2.7 | 75 | 4.3 |
| CPK 升高a,A | 39 | 2 | 64 | 5 |
| 低白蛋白血症a,A | 36 | 0.7 | 61 | 6 |
| 脂肪酶升高a,A | 28 | 7 | 34 | 5 |
| 碱性磷酸酶升高a,A | 23 | 0 | 50 | 0.7 |
| 高钾血症a,A | 21 | 1.3 | 27 | 2.1 |
| 淀粉酶升高b,A | 20 | 1.4 | 32 | 1.4 |
| 血液学 | ||||
| 贫血a,A | 48 | 2 | 38 | 2.8 |
| 活化 PTTc,B | 25 | 0 | 14 | 0 |
| 淋巴细胞减少症a,A | 23 | 2.7 | 43 | 6 |
| 血小板减少症a,A | 23 | 0 | 7 | 0.7 |
| * 根据 NCI CTCAE 4.03 版分级。 缩略词:ALT=丙氨酸氨基转移酶;AST=天冬氨酸氨基转移酶;CPK=肌酸磷酸激酶;GGT=γ 谷氨酰转移酶;NCI CTCAE=美国国立癌症研究所不良事件通用术语标准;PTT = 部分凝血活酶时间。 N=研究中至少接受过 1 次关注参数评估的患者例数。 a N=149 (本品)。 A N=141(克唑替尼)。 b N=148 (本品)。 B N=135(克唑替尼)。 c N=138 (本品)。 | ||||
既往接受过治疗的 ALK 阳性转移性 NSCLC
下述数据反映了研究 B7461001(一项多队列、非比较性试验)中 295 名接受本品100 mg每日一次口服治疗的 ALK 阳性或 ROS1 阳性转移性 NSCLC 患者的暴露情况(见【临床试验】)。本品的中位暴露持续时间为 12.5 个月(1 天至 35 个月),52% 的患者接受了本品 ≥ 12 个月的治疗。患者特征如下:中位年龄 53 岁(19 至 85 岁),年龄 ≥ 65 岁 (18%),女性 (58%),白人 (49%),亚裔 (37%),美国东部肿瘤协作组 (ECOG) 体力状态 0 或 1 (96%)。
最常见 (≥20%) 的不良反应为水肿、周围神经病、认知影响、呼吸困难、疲乏、体重增加、关节疼痛、情绪影响和腹泻;在 ≥20% 的患者中出现的实验室检查值异常中,最常见的为高胆固醇血症、高甘油三酯血症、贫血、高血糖、AST 升高、低白蛋白血症、ALT 升高、脂肪酶升高和碱性磷酸酶升高。
在这 295 名患者中,32% 发生了严重不良反应;最常见的严重不良反应为肺炎 (3.4%)、呼吸困难 (2.7%)、发热 (2%)、精神状态改变 (1.4%) 和呼吸衰竭 (1.4%)。2.7% 的患者发生致命的不良反应,包括肺炎 (0.7%)、心肌梗死 (0.7%)、急性肺水肿 (0.3%)、栓塞 (0.3%)、外周动脉闭塞 (0.3%) 和呼吸窘迫 (0.3%)。8% 的患者因不良反应而永久停用本品。
导致永久停药的最常见不良反应为呼吸衰竭 (1.4%)、呼吸困难 (0.7%)、心肌梗死 (0.7%)、认知影响 (0.7%) 和情绪影响 (0.7%)。约 48% 的患者需要中断给药。导致中断给药的最常见不良反应为水肿 (7%)、高甘油三酯血症 (6%)、周围神经病 (5%)、认知影响 (4.4%)、脂肪酶升高 (3.7%)、高胆固醇血症 (3.4%)、情绪影响 (3.1%)、呼吸困难 (2.7%)、肺炎 (2.7%) 和高血压 (2.0%)。约 24% 的患者因不良反应而至少需要降低一次剂量。导致降低剂量的最常见不良反应为水肿 (6%)、周围神经病 (4.7%)、认知影响 (4.1%) 和情绪影响 (3.1%)。
表 4 和表 5 分别汇总了研究 B7461001 中接受本品治疗的患者的最常见不良反应和实验室检查异常。
表 4 研究 B7461001 中在 ≥10% 的患者中发生的不良反应*
| 不良反应 | 本品 (N=295) | |
|---|---|---|
| 所有等级 (%) | 3 或 4 级 (%) | |
| 精神病类 | ||
| 情绪影响a | 23 | 1.7 |
| 神经系统 | ||
| 周围神经病b | 47 | 2.7 |
| 认知影响c | 27 | 2 |
| 头痛 | 18 | 0.7 |
| 头晕 | 16 | 0.7 |
| 语言影响d | 12 | 0.3 |
| 睡眠影响e | 10 | 0 |
| 呼吸系统 | ||
| 呼吸困难 | 27 | 5 |
| 咳嗽 | 18 | 0 |
| 视觉 | ||
| 视觉异常f | 15 | 0.3 |
| 胃肠道 | ||
| 腹泻 | 22 | 0.7 |
| 恶心 | 18 | 0.7 |
| 便秘 | 15 | 0 |
| 呕吐 | 12 | 1 |
| 肌肉骨骼和结缔组织 | ||
| 关节痛 | 23 | 0.7 |
| 肌痛g | 17 | 0 |
| 背痛 | 13 | 0.7 |
| 四肢痛 | 13 | 0.3 |
| 一般情况 | ||
| 水肿h | 57 | 3.1 |
| 疲乏i | 26 | 0.3 |
| 体重增加 | 24 | 4.4 |
| 发热 | 12 | 0.7 |
| 感染 | ||
| 上呼吸道感染j | 12 | 0 |
| 皮肤 | ||
| 皮疹k | 14 | 0.3 |
* 使用 NCI CTCAE 第 4.03 版对不良反应进行分级。
缩略词:NCI CTCAE=美国国立癌症研究所不良事件通用术语标准;SOC=系统器官分类。
a 情绪影响(包括情感障碍、情感易变、攻击性、激越、焦虑、抑郁情绪、抑郁、欣快感、易激惹、躁狂、情绪变化、情绪波动、人格改变、应激、自杀想法)。
b 周围神经病(包括烧灼感、腕管综合征、感觉迟钝、蚊行感、步态障碍、感觉减退、肌无力、神经痛、周围神经病、神经毒性、感觉异常、外周感觉神经病变、感觉障碍)。
c 认知影响(包括 SOC 神经系统疾病中的事件:失忆症、认知障碍、痴呆、注意力障碍、记忆损害、精神损害;还包括 SOC 精神疾病中的事件:注意力缺陷/多动症、意识模糊状态、谵妄、定向障碍、阅读障碍)。
d 言语影响(包括失语、构音障碍、言语迟缓、言语障碍)
e 睡眠影响(包括睡梦异常、失眠、梦魇、睡眠障碍、呓语、梦游症)
f 视觉异常(包括失明、复视、畏光、闪光幻觉、视物模糊、视觉敏感度减退、视力损害、飞蚊症)。
g 肌痛(包括骨骼肌疼痛、肌痛)。
h 水肿(包括水肿、外周水肿、眼睑水肿、面部水肿、全身水肿、局部水肿、眶周水肿、外周肿胀、肿胀)。
i 疲乏(包括乏力、疲乏)。
j 上呼吸道感染(包括上呼吸道真菌感染、上呼吸道感染和上呼吸道病毒感染)。
k 皮疹(包括痤疮样皮炎、斑丘疹、皮疹瘙痒、皮疹)。
发生率在 1% 至 10% 之间的其他具有临床意义的不良反应为精神影响 (7%)。
表 5 研究 B7461001 中在 ≥20% 的患者中发生的实验室检查值异常*
| 实验室检查异常 | 本品 | |
|---|---|---|
| 所有等级 (%) | 3 或 4 级 (%) | |
| 生化检查 | ||
| 高胆固醇血症a | 96 | 18 |
| 高甘油三酯血症a | 90 | 18 |
| 高血糖b | 52 | 5 |
| AST 升高a | 37 | 2.1 |
| 低白蛋白血症c | 33 | 1 |
| ALT 升高a | 28 | 2.1 |
| 脂肪酶升高d | 24 | 10 |
| 碱性磷酸酶升高a | 24 | 1 |
| 淀粉酶升高e | 22 | 3.9 |
| 低磷血症a | 21 | 4.8 |
| 高钾血症b | 21 | 1 |
| 高镁血症a | 21 | 0 |
| 血液学 | ||
| 贫血b | 52 | 4.8 |
| 血小板减少症b | 23 | 0.3 |
| 淋巴细胞减少症a | 22 | 3.4 |
* 根据 NCI CTCAE 4.03 版分级。
缩略词:ALT=丙氨酸氨基转移酶;AST=天冬氨酸氨基转移酶;NCI CTCAE=美国国立癌症研究所不良事件通用术语标准。
N=研究中至少接受过 1 次关注参数评估的患者例数。
a N=292。
b N=293。
c N=291。
d N=290。
e N=284。
本品禁用于正在服用强效 CYP3A 诱导剂的患者,因为可能发生严重肝脏毒性(见【注意事项】)。
合用强效 CYP3A 诱导剂的严重肝脏毒性风险
接受本品单次给药和利福平(一种强效 CYP3A 诱导剂)多次每日给药的 12 名健康受试者中有 10 名出现了严重肝脏毒性。50% 的受试者出现 4 级丙氨酸氨基转移酶 (ALT) 或天冬氨酸氨基转移酶 (AST) 升高,33% 的受试者出现 3 级 ALT 或 AST 升高,8% 的受试者出现 2 级 ALT 或 AST 升高。ALT 或 AST 升高发生在 3 天内并在中位时间 15 天后(7 至 34 天)恢复到正常范围内;3 或 4 级 ALT 或 AST 升高的受试者中位恢复时间为 18 天,2 级 ALT 或 AST 升高的受试者中位恢复时间为 7 天(见【药物相互作用】)。
本品禁用于正在服用强效 CYP3A 诱导剂的患者。停用强效 CYP3A 诱导剂的3个血浆半衰期后,开始服用本品(见【禁忌】和【药物相互作用】)。
中枢神经系统影响
服用本品的患者可能会发生广泛的中枢神经系统 (CNS) 影响。这些影响包括癫痫发作、精神影响和认知功能、情绪(包括自杀想法)、言语、精神状态和睡眠改变。总体而言,在临床研究中接受本品100 mg 每日一次的476名患者中,有 52% 发生了中枢神经系统影响(见【不良反应】)。有 28% 发生了认知影响;这些事件中有 2.9% 为重度影响(3 或 4 级)。有 21% 的患者出现了情绪影响;这些事件中有 1.7% 为重度影响。有 11% 的患者出现了言语影响;这些事件中有 0.6% 为重度影响。有 7% 的患者出现了精神影响;这些事件中有 0.6% 为重度影响。有 1.3% 的患者出现了精神状态改变;这些事件中有 1.1% 为重度影响。有 1.9% 的患者出现癫痫发作,有时与其他神经系统疾病相关。有 12% 的患者出现睡眠影响。任何 CNS 影响首次出现的中位时间为 1.4个月(1 天至 3.4 年)。总体而言,2.1% 的患者因 CNS 影响需要永久停用本品;10% 的患者需要暂时停用,8% 的患者需要降低剂量。
根据严重程度暂停用药并以相同剂量或降低一个剂量水平恢复给药,或者永久停用本品(见【用法用量】)。
高脂血症
在接受本品给药的患者中可能出现血清胆固醇和甘油三酯升高的情况(见【不良反应】)。在 476 名接受本品100 mg 每日一次给药的患者中,有 18% 发生了 3 或 4 级总胆固醇升高,有 19% 发生了 3 或 4 级甘油三酯升高。高胆固醇血症和高甘油三酯血症的中位发生时间为 15 天。在研究 B7461001 和研究 B7461006 中的胆固醇和甘油三酯升高的患者中,约 4% 和 7% 的患者需要暂时停用本品,1% 和 3% 的患者需要降低剂量。有 83% 的患者需要开始服用降脂药物,开始服用这类药物的中位时间为 17 天。
在高脂血症患者中开始使用或增加降脂剂的剂量。在开始服用本品之前,以及在开始服用本品之后第1 和第2 个月时监测血清胆固醇和甘油三酯,并在此后定期监测。对第一次出现的情况,暂停并以相同剂量恢复给药;根据严重程度,对复发的情况,以相同剂量或降低一个剂量水平继续给药(见【用法用量】)。
房室传导阻滞
在接受本品给药的患者中可能会发生 PR 间期延长和房室 (AV) 传导阻滞(见【不良反应】和【药代动力学】)。在接受本品100 mg 每日一次给药并且具有基线心电图 (ECG) 的 476 名患者中,有 1.9% 出现房室传导阻滞,且 0.2% 发生了 3 级房室传导阻滞并接受了起搏器植入。
在开始服用本品之前监测 ECG,并在此后定期监测。对于接受起搏器植入的患者,应暂停用药并以降低一个剂量水平或相同的剂量恢复给药。对于没有起搏器的患者,如果复发,应永久停用本品(见【用法用量】)。
间质性肺病/非感染性肺炎
本品给药可能会引起重度或危及生命的肺部不良反应,即间质性肺病 (ILD)/非感染性肺炎。在接受本品100 mg 每日一次给药的患者中,有 1.9% 发生了 ILD/非感染性肺炎,其中 0.6% 的患者发生了 3 或 4 级 ILD/非感染性肺炎。4名患者 (0.8%) 因 ILD/非感染性肺炎而停止服用本品。
对任何呼吸系统症状恶化且可能预示 ILD/非感染性肺炎(例如呼吸困难、咳嗽和发热)的患者,立即诊断是否为 ILD/非感染性肺炎。如果怀疑患有 ILD/非感染性肺炎,应立即停用本品。对于与本品治疗相关的任何程度的 ILD/非感染性肺炎,应永久停用本品(见【用法用量】)。
高血压
接受本品治疗的患者可能出现高血压(见【不良反应】)。在接受本品100 mg 每日一次治疗的患者中,有 13% 出现了高血压,其中 6% 的患者出现了 3 或 4 级事件。至高血压发作的中位时间为 6.4 个月(1 天至 2.8 年),2.3% 的患者因高血压而暂停服用本品。
应在开始本品治疗之前控制血压,服药2 周后监测血压,之后在本品治疗期间至少每月监测一次。根据高血压的严重程度暂停用药并降低一个剂量水平恢复给药,或者永久停用本品(见【用法用量】)。
高血糖
接受本品治疗的患者可能出现高血糖(见【不良反应】)。在接受本品100 mg 每日一次治疗的患者中,有 9% 出现了高血糖,其中 3.2% 的患者出现了 3 或 4 级事件。至高血糖发作的中位时间为 4.8 个月(1 天至 2.9 年),0.8% 的患者因高血糖而暂停服用本品。
在开始本品治疗之前评估空腹血糖并在此后定期评估。根据高血糖的严重程度暂停用药并降低一个剂量水平恢复给药,或者永久停用本品(见【用法用量】)。
胚胎-胎儿毒性
基于动物研究的发现及本品的作用机制,妊娠女性服用本品可能会对胎儿造成伤害。在器官形成期间向妊娠大鼠和兔灌胃给药,母体暴露量等于或低于推荐剂量每日一次 100 mg 下的人体暴露量(基于曲线下面积 (AUC))的洛拉替尼时,导致畸形、胎盘植入后丢失率增加和流产。
应告知妊娠女性本品对胎儿的潜在风险。建议有生育能力的女性使用有效的非激素避孕法,因为本品在治疗期间和末次剂量后至少 6 个月可使激素避孕药失效。对于女性伴侣具有生育能力的男性患者,建议在接受本品治疗期间及末次给药后 3 个月内使用有效的避孕措施(见【药物相互作用】、【孕妇及哺乳期妇女用药】和【药理毒理】)。
妊娠
风险总结
基于动物研究的发现及本品的作用机制(见【药理毒理】),妊娠女性服用本品可能会造成胚胎-胎儿伤害。目前尚无本品在妊娠女性中使用的数据。在器官形成期间向妊娠大鼠和兔灌胃给药,母体暴露量等于或低于推荐剂量每日一次 100 mg 下的人体暴露量(基于 AUC)的洛拉替尼时,导致畸形、胎盘植入后丢失率增加和流产(见数据)。应告知妊娠女性对胎儿的潜在风险。
在美国一般人群中,估计主要出生缺陷和流产在临床识别妊娠中的背景风险分别为 2% - 4% 和 15% - 20%。
数据
动物数据
在大鼠和兔中进行了初步胚胎-胎仔发育研究,旨在研究器官形成期间给与洛拉替尼的影响。在兔中,剂量为 15 mg/kg(约为推荐剂量 100 mg 下人体暴露量的 3 倍)或更高时,洛拉替尼给药导致流产和妊娠完全丢失。剂量为 4 mg/kg(约为推荐剂量 100 mg 下人体暴露量的 0.6 倍)时,毒性包括着床后丢失率增加和畸形(包括四肢旋转、肾脏畸形、半球形头、高弓形上颚和脑室扩张)。在大鼠中,剂量为 4 mg/kg(约为推荐剂量 100 mg 下人体暴露量的 5 倍)或更高时,洛拉替尼给药导致妊娠完全丢失。剂量为 1 mg/kg(约等于推荐剂量 100 mg 下的人体暴露量)时,出现着床后丢失率增加、胎仔体重减轻和畸形(包括腹裂、四肢旋转、多指/趾和血管异常)。
哺乳期
风险总结
尚无有关人或动物乳汁中含有洛拉替尼或其代谢物以及对哺乳婴儿或产奶的影响的数据。由于哺乳婴儿存在发生严重不良反应的潜在可能性,因此应告知女性在接受本品治疗期间以及末次给药后至少 7 天内不要哺乳。
具有生育潜能的女性和男性
妊娠检查
对于具有生育能力的女性,在开始本品给药之前检查妊娠状态。
避孕
妊娠女性使用本品可能会引起胚胎-胎儿伤害。
女性
应告知具有生育能力的女性患者在接受本品治疗期间及末次给药后至少 6 个月内使用有效的非激素避孕措施。建议具有生育能力的女性使用非激素避孕措施,因为本品可能使激素类避孕药失效(见【药物相互作用】)。
男性
基于遗传毒性的研究结果,对于女性伴侣具有生育能力的男性,应告知在接受本品治疗期间及末次给药后至少 3 个月内使用有效的避孕措施(见【药理毒理】)。
不孕
男性
基于动物研究的研究结果,本品可能会短暂损伤男性生育力(见【药理毒理】)。
儿童患者使用本品的安全性和有效性尚未确定。
对于在研究 B7461001 (N=295) 和研究 B7461006 (N=149) 中接受 100 mg本品每日一次口服给药的患者中,分别有 18% 和 40% 的患者的年龄为 65 岁或更高。65 岁或更高年龄的患者与较年轻患者之间未观察到安全性或疗效出现具有临床意义的差异。
其他药物对本品的影响
强效CYP3A 诱导剂
本品与强效 CYP3A 诱导剂合用可使洛拉替尼血浆浓度降低,从而可能降低本品的疗效(见【药代动力学】)。
接受本品与利福平(一种强效 CYP3A 诱导剂)同时给药的健康受试者曾发生严重肝脏毒性。在 12 名接受 100 mg本品单次给药和利福平多次每日给药的健康受试者中,83% 受试者发生 3 或 4 级 ALT 或 AST 升高,8% 受试者发生 2 级 ALT 或 AST 升高。一种可能的机制是本品和利福平(两者都是 PXR 激动剂)对孕烷 X 受体的激活作用。
本品禁用于正在服用强效 CYP3A 诱导剂的患者(见【禁忌】)。停用强效 CYP3A 诱导剂的3个血浆半衰期后,开始服用本品(见【用法用量】)。
中效 CYP3A 诱导剂
本品与中效 CYP3A 诱导剂合用可使洛拉替尼血浆浓度降低,从而可能降低本品的疗效(见【药代动力学】)。避免本品与中效 CYP3A 诱导剂合用。如果不能避免合用,则应增加本品剂量(见【用法用量】)。
强效 CYP3A 抑制剂
与强效 CYP3A 抑制剂合用可使洛拉替尼血浆浓度升高(见【药代动力学】),从而可能增加本品不良反应的发生率和严重程度。避免本品与强效 CYP3A 抑制剂合用。如果不能避免合用,则应降低本品剂量(见【用法用量】)。
氟康唑
本品与氟康唑合用可使洛拉替尼血浆浓度升高(见【药代动力学】),从而可能增加本品不良反应的发生率和严重程度。避免本品与氟康唑合用。如果不能避免合用,则应降低本品剂量(见【用法用量】)。
本品对其他药物的影响
某些CYP3A 底物
本品是一种中效 CYP3A 诱导剂。与本品合用会降低 CYP3A 底物的浓度(见【药代动力学】),这可能会降低这些底物的疗效。避免本品与某些CYP3A 底物合用,因为底物浓度的极小改变可能会导致严重的治疗失败。如果合用无法避免,则根据批准的产品说明书增加 CYP3A 底物的剂量。
某些P-糖蛋白 (P-gp) 底物
本品是一种中效 P-gp 诱导剂,与本品合用会降低 P-gp 底物的浓度(见【药代动力学】),这可能会降低这些底物的疗效。避免本品与某些P-gp 底物合用,因为底物浓度的极小改变可能会导致严重的治疗失败。如果合用无法避免,则根据批准的产品说明书增加 P-gp 底物的剂量。
药物过量的治疗包括一般性支持措施。考虑到对PR间期的剂量依赖性效应,建议进行心电图监测。本品没有解毒剂。
既往未接受过治疗的 ALK 阳性转移性 NSCLC(CROWN 研究)
在一项开放、随机、阳性对照、多中心研究(研究 B7461006;NCT03052608)中,确定了本品用于治疗既往未接受过针对转移性疾病的系统性治疗的 ALK 阳性 NSCLC 患者的疗效。要求患者的 ECOG 体力状态为 0 至 2,并且经 VENTANA ALK (D5F3) CDx 检测确定为 ALK 阳性 NSCLC。同时纳入了存在接受过或未接受过治疗的无症状中枢神经系统 (CNS) 转移(包括软脑膜转移)、达到神经系统稳定的患者。要求患者在随机分组前至少 2 周(对于立体定向放射或部分放射)或 4 周(对于全脑放射)完成放射治疗。将患有严重的急性或慢性精神病(包括近期 [过去一年内] 或目前有自杀想法或行为)的患者排除在外。
患者按 1:1 的比例随机分组,以本品100 mg 每日一次口服给药或克唑替尼 250 mg 每天两次口服给药。按人种(亚洲人与非亚洲人)和基线时是否存在 CNS 转移进行随机化分层。两组的治疗均持续到出现疾病进展或不可接受的毒性。主要的疗效结果指标是由盲态独立中心审查 (BICR) 根据实体瘤疗效评价标准 (RECIST) 1.1 版 (v1.1) 确定的无进展生存期 (PFS)。其他的疗效结果指标包括总生存期 (OS) 和由 BICR确定的肿瘤评估相关数据,包括总体缓解率 (ORR)和缓解持续时间 (DOR)。在基线时存在可测量的 CNS 转移的患者中,结果指标还包括由BICR确定的颅内总体缓解率 (IC-ORR) 和颅内缓解持续时间 (IC-DOR)。
共 296 名患者被随机分配接受本品(n=149) 或克唑替尼 (n=147) 治疗。总体研究人群的基线特征为:中位年龄 59 岁(范围:26 至 90 岁),年龄 ≥65 岁 (35%),女性 59%,白人 49%,亚裔 44%,黑人 0.3%。96% 的患者基线时的 ECOG 体力状态评分为 0 或 1。大多数患者患有腺癌 (95%),并且从不吸烟 (59%)。26% (n=78) 的患者存在 CNS 转移:其中 30 例患者具有可测量的 CNS 病变。
表 6 和图 1 汇总了研究 B7461006 中经 BICR 评定的疗效结果。结果表明,洛拉替尼组的 PFS 较克唑替尼组有显著改善。在数据截止点时,OS数据尚不成熟。
表 6 研究 B7461006 (CROWN) 的疗效结果
| 疗效指标 | 本品 N=149 | 克唑替尼 N=147 |
|---|---|---|
| 无进展生存期 | ||
| 事件数,n (%) | 41 (28%) | 86 (59%) |
| 疾病进展,n (%) | 32 (22%) | 82 (56%) |
| 死亡,n (%) | 9 (6%) | 4 (3%) |
| 中位数(月数)(95% CI)a | NE(NE,NE) | 9.3 (7.6, 11.1) |
| 风险比 (95% CI)b | 0.28 (0.19, 0.41) | |
| p 值* | <0.0001 | |
| 总体缓解率 | ||
| 总体缓解率 (95% CI)c | 76% (68, 83) | 58% (49, 66) |
| 完全缓解 | 3% | 0% |
| 部分缓解 | 73% | 58% |
| 缓解持续时间 | ||
| 缓解人数,n | 113 | 85 |
| 中位数,月(范围) | NE (0.9, 31.3) | 11 (1.1, 27.5) |
| 缓解持续时间 ≥6 个月,n (%) | 101 (89%) | 53 (62%) |
| 缓解持续时间 ≥12 个月,n (%) | 79 (70%) | 23 (27% ) |
| 缓解持续时间 ≥18 个月,n (%) | 34 (30%) | 9 (11%) |
缩略词:CI=置信区间;N=患者例数;NE=不可估计;PFS=无进展生存期。
* p 值基于单侧分层对数秩检验。
a 基于 Brookmeyer 和 Crowley 方法。
b 风险比基于 Cox 比例风险模型。
c 使用基于二项分布的精确方法。
图 1:研究 B7461006 (CROWN) 中经BICR评定的无进展生存期的 Kaplan-Meier 图
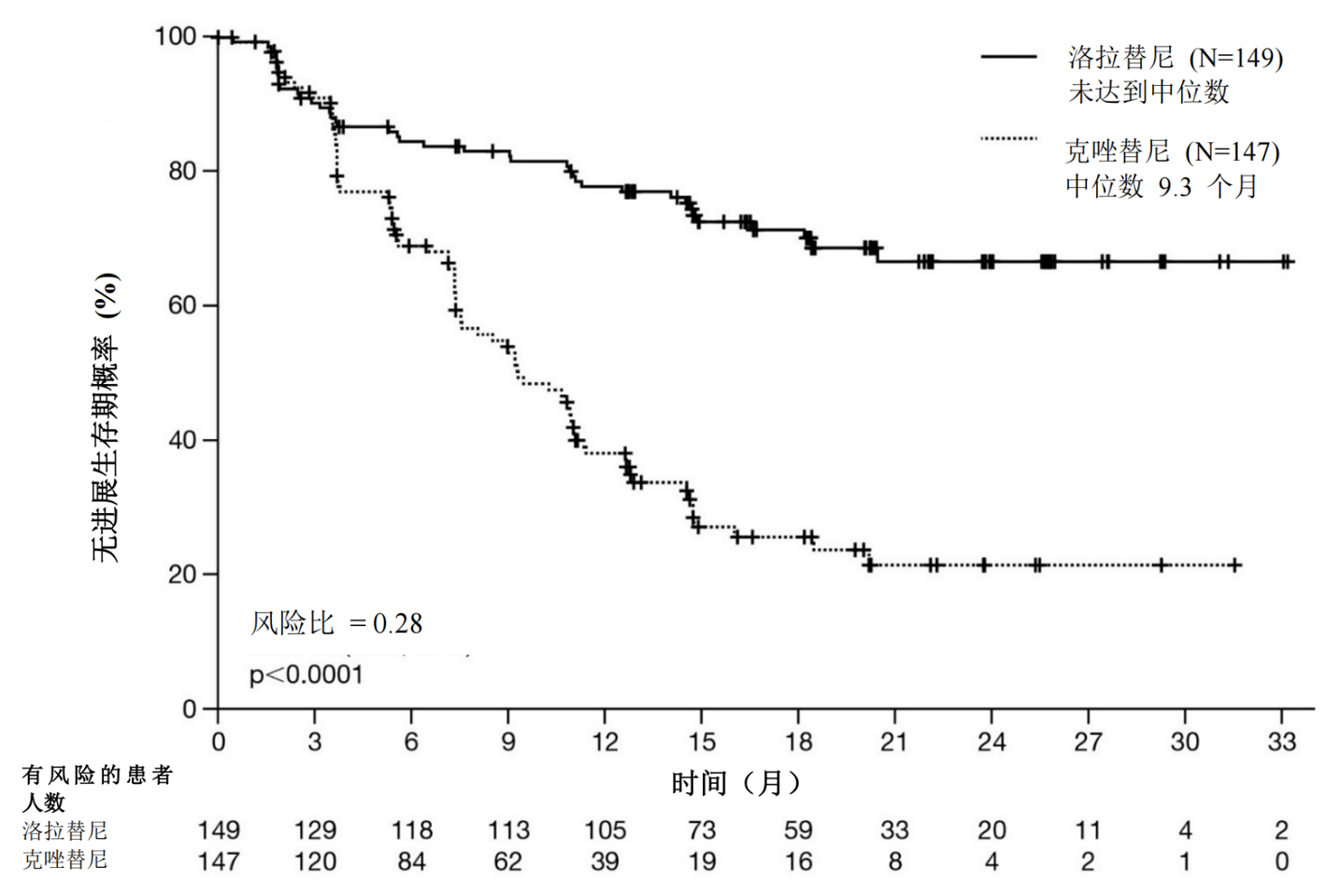
表 7 总结了对基线时具有经 BICR 评定的可测量 CNS 病变的30 例患者的颅内缓解率进行的预设的探索性分析结果。
表 7 CROWN 研究中具有可测量颅内病变的患者的颅内缓解率
| 颅内肿瘤缓解评价 | 本品 N=17 | 克唑替尼 N=13 |
|---|---|---|
| 颅内缓解率 (95% CI)a | 82% (57, 96) | 23% (5, 54) |
| 完全缓解 | 71% | 8% |
| 缓解持续时间 | ||
| 缓解人数,n | 14 | 3 |
| 缓解持续时间 ≥12 个月,n (%) | 11 (79%) | 0 |
缩略词:CI=置信区间;N/n=患者例数。
a 使用基于二项分布的精确方法。
曾接受过 ALK 激酶抑制剂治疗的 ALK 阳性转移性 NSCLC
在一项非随机、剂量范围与活性评估、多队列、多中心的研究(研究 B7461001;NCT01970865)中,在曾接受一种或多种 ALK 激酶抑制剂治疗的 ALK 阳性转移性NSCLC 患者亚组中证实了本品的疗效。按照要求,该研究中包括的患者根据 RECIST v1.1 确定具有至少 1 处可测量靶病灶的转移性疾病,ECOG 体力状态为 0 至 2,并且有根据荧光原位杂交 (FISH) 试验或通过免疫组织化学 (IHC) 检测确定的肿瘤组织 ALK 重排记录,接受本品100 mg 每日一次口服给药。同时纳入了存在无症状 CNS 转移的患者(包括进入研究前的 2 周内使用稳定或降低剂量的激素的患者)。将患有严重、急性或慢性精神病(包括有自杀想法或行为)的患者排除在外。此外,对于 ALK 阳性转移性 NSCLC 患者,规定了每个单独队列先前治疗的程度和类型(见表 8)。主要疗效指标为ORR 和颅内 ORR,由独立中心审查 (ICR) 委员会根据 RECIST v1.1进行评估。对表 8 列出的各亚组数据进行汇总。其他疗效指标包括DOR 和颅内 DOR。
研究中各亚组共计入组了 215 名患者(见表 8)。表 8 提供了按既往治疗的类型和程度列出的患者分布。215 名患者的基线特征为:女性 59%,白人 51%,亚裔 34%,中位年龄 53 岁(29 至 85 岁),其中 18% 的患者 ≥ 65 岁。96% 的患者的基线时 ECOG 体力状态为 0 或 1。所有患者均存在转移性疾病,95% 的患者为腺癌。69% 的患者通过 ICR 确定发生脑转移;其中 60% 先前曾接受过脑部放疗,而有 60% (n=89) 的患者经 ICR 判定有可测量疾病。
表 8 研究 B7461001 中曾接受治疗的 ALK 阳性转移性 NSCLC 患者亚组中的既往治疗情况
| 既往治疗情况 | 患者人数 |
|---|---|
| 曾接受克唑替尼治疗且未曾接受过化 疗a | 29 |
| 曾接受克唑替尼治疗和 1 - 2 线化 疗a | 35 |
| 曾接受 ALK 抑制剂(非克唑替尼)且伴或不伴化 疗a | 28 |
| 曾接受两种 ALK 抑制剂且伴或不伴化 疗a | 75 |
| 曾接受三种 ALK 抑制剂且伴或不伴化 疗a | 48 |
| 总计 | 215 |
缩略词:ALK=间变性淋巴瘤激酶;NSCLC=非小细胞肺癌。
a 化疗在转移性病变中使用。
研究 B7461001 的疗效结果总结见表 9 和表 10。
表 9 研究 B7461001 的疗效结果
| 疗效指标 | 总体 N=215 |
|---|---|
| 总体缓解率a (95% CI)b | 48% (42,55) |
| 完全缓解 | 4% |
| 部分缓解 | 44% |
| 缓解持续时间 | |
| 中位数(月数)c (95% CI) | 12.5 (8.4,23.7) |
缩略词:CI=置信区间;N=患者人数。
a 依据独立中心评估结果。
b 采用基于二项分布的精确方法。
c 采用 Kaplan Meier 方法进行估算。
在研究 B7461001 中,根据 RECIST v1.1 对基线时具有 CNS 可测量病变的 89 例患者亚组进行 CNS 转移瘤的颅内 ORR 评估和缓解持续时间评估,总结见表 10。在这些患者中,有 56 位 (63%) 先前曾接受过脑部放疗,其中有 42 位患者 (47%) 在开始接受本品治疗至少6个月前已完成脑部放疗。
表 10 研究 B7461001 中有可测量颅内病变患者的颅内缓解率
| 疗效指标 | 颅内 N=89 |
|---|---|
| 颅内缓解率a (95% CI)b | 60% (49, 70) |
| 完全缓解 | 21% |
| 部分缓解 | 38% |
| 缓解持续时间 | |
| 中位数(月数)c (95% CI) | 19.5(12.4,NR) |
缩略词:CI=置信区间;N=患者人数;NR=未达到。
a 依据独立中心评估结果。
b 采用基于二项分布的精确方法。
c 采用 Kaplan-Meier 方法进行估算。
在对规定了先前治疗方式的亚组的探究性分析中,本品的缓解率为:
- 曾接受克唑替尼和至少一种其他 ALK 抑制剂且伴或不伴化疗的 119 名患者,ORR=39%(95% CI:30,48)
- 曾接受阿来替尼作为唯一一种 ALK 抑制剂且伴或不伴化疗的 13 名患者,ORR=31%(95% CI:9,61)
- 曾接受塞瑞替尼作为唯一一种 ALK 抑制剂且伴或不伴化疗的 13 名患者,ORR=46%(95% CI:19,75)
药理作用
洛拉替尼为ALK、ROS1激酶抑制剂,对TYK1、FER、FPS、TRKA、TRKB、TRKC、FAK、FAK2、ACK激酶也具有体外抑制活性。洛拉替尼对ALK激酶的多种突变形式具有体外抑制活性,包括疾病进展(克唑替尼和其它ALK抑制剂治疗)时肿瘤中所检测到的一些突变。
在EML4与ALK变体1或ALK突变体(包括在ALK抑制剂治疗后进展的肿瘤中检测到的G1202R和I1171T突变)融合的小鼠皮下移植瘤模型中,可见洛拉替尼抗肿瘤活性。洛拉替尼在EML4-ALK颅内移植瘤模型小鼠中也可见抗肿瘤活性,并可延长小鼠生存期。洛拉替尼在体内模型中的整体抗肿瘤活性呈剂量依赖性,并与抑制ALK的磷酸化相关。
毒理研究
遗传毒性:
洛拉替尼Ames试验结果为阴性,人淋巴母细胞TK6细胞的体外染色体畸变试验和大鼠骨髓体内微核试验结果阳性。
生殖毒性:
洛拉替尼未进行专门的生育力试验。在重复给药毒性试验中,大鼠和犬分别给予洛拉替尼15mg/kg/天和 7mg/kg/天(以AUC计,约为临床推荐剂量100mg时人暴露量的8倍、2 倍),雄性生殖系统可见睾丸、附睾和前列腺重量下降,睾丸小管变性/萎缩,前列腺萎缩、附睾炎症等。上述雄性生殖器官改变可恢复。
在大鼠和兔中,开展了洛拉替尼在器官形成期给药的初步的胚胎-胎仔发育毒性试验。兔给予洛拉替尼15mg/kg(约为临床推荐剂量100mg时人暴露量的3倍)及以上剂量时,可导致流产和妊娠完全丢失;给予4mg/kg(约为临床推荐剂量100mg时人暴露量的0.6倍)剂量时,毒性包括着床后丢失率增加和畸形(包括前/后肢掌外/内翻、肾畸形、脑膜膨出、高颚穹和脑室扩张)。大鼠给予洛拉替尼4mg/kg(约为临床推荐剂量100mg时人暴露量的5倍)及以上剂量时,可导致妊娠完全丢失;给予1mg/kg(约相当于临床推荐剂量100mg的人暴露量)剂量时,可见着床后丢失率增加、胎仔体重减轻和畸形(包括腹裂、前/后肢掌外/内翻、多指/趾和血管异常)。
致癌性:
洛拉替尼尚未开展致癌性研究。
其它毒性:
大鼠和犬分别给予洛拉替尼15mg/kg/天和2mg/kg/天(以AUC计,分别约为临床推荐剂量100mg时人暴露量的8倍和0.5倍),可见动物腹部肿胀、皮疹、胆固醇和甘油三酯升高,伴随肝脏中胆管增生、扩张以及胰腺腺泡萎缩。上述毒性作用恢复期内可恢复。
在每日一次口服给药 10 mg 至 200 mg 剂量范围内(推荐剂量的 0.1 至 2 倍),稳态洛拉替尼最大血浆浓度 (Cmax) 按比例增加并且 AUC 的增加略低于药物增加比例。在推荐剂量下,癌症患者的平均[变异系数 (CV) %] Cmax 为 577 ng/mL (42%),AUC0-24h 为 5650 ng·h/mL (39%)。与单次给药相比,洛拉替尼口服清除率在稳态下有所增加,表明存在自身诱导。
吸收
100 mg 单次口服给药和 100 mg每日一次口服给药后稳态下洛拉替尼的Tmax 中位数分别为 1.2 小时(0.5 至 4 小时)和 2 小时(0.5 至 23 小时)。
与静脉给药相比,口服给药后平均绝对生物利用度为 81%(90% CI 75.7%,86.2%)。
食物的影响
随高脂肪、高热量餐(大约 1000 卡路里,其中 150 卡路里来自蛋白质,250 卡路里来自碳水化合物及 500 至 600 卡路里来自脂肪)给予本品对洛拉替尼的药代动力学没有临床意义的影响。
分布
在体外,洛拉替尼的浓度为2.4 μM时与血浆蛋白质结合率为 66%。血液-血浆比为 0.99。在单次静脉给药后,平均 (CV%) 稳态分布容积 (Vss) 为 305 L (28%)。
消除
在单次口服 100 mg 剂量本品后的平均血浆半衰期 (t½) 为 24 小时 (40%)。100 mg 单次口服给药后的平均口服清除率 (CL/F) 为 11 L/h (35%),稳态时增加到 18 L/h (39%),表明存在自身诱导。
代谢
在体外,洛拉替尼主要通过 CYP3A4 和 UGT1A4 代谢,一小部分通过 CYP2C8、CYP2C19、CYP3A5 和 UGT1A3 代谢。
在血浆中,通过洛拉替尼的酰胺和芳香醚键的氧化裂解产生的洛拉替尼苯甲酸代谢物 (M8) 占循环放射性的 21%。氧化裂解代谢物 M8 为药理学非活性产物。
排泄
单次口服100 mg 放射性标记的洛拉替尼后,48% 的放射性在尿中回收(无变化形式 < 1%),41% 在粪便中回收(无变化形式约 9%)。
特殊人群
根据年龄(19 至 85 岁)、性别、人种/种族、体重、轻度至中度肾损害(采用 Cockcroft-Gault 公式估算的CLcr 为30 至 89 mL/min)、轻度肝损害(总胆红素 ≤ ULN 和 AST > ULN 或总胆红素 > 1-1.5 × ULN 和任何 AST)、或 CYP3A5 和 CYP2C19 的代谢物表现型,未观察到洛拉替尼药代动力学出现显著的临床变化。中度至重度肝损害(总胆红素 ≥ 1.5 × ULN 伴任何 AST)对洛拉替尼的药代动力学的影响尚不清楚。
重度肾损害患者
单次口服 100 mg 剂量的本品后,相比肾功能正常(采用 Cockcroft-Gault 公式估算的CLcr ≥ 90 mL/min)的受试者,重度肾损害(采用 Cockcroft-Gault 公式估算的CLcr 为 15 至 < 30 mL/min)受试者的洛拉替尼AUCinf 增加了 42%。尚未在需要血液透析的终末期肾病患者中进行洛拉替尼的药代动力学研究。
药物相互作用研究
临床研究和基于模型的方法
强效CYP3A 诱导剂对洛拉替尼的影响:接受8天利福平(一种强效 CYP3A 诱导剂,还可激活 PXR)600 mg 每日一次给药(第 1 至 8 天)并在第 8 天接受本品100 mg 单次口服给药,使洛拉替尼 AUCinf 平均值下降 85%,Cmax 下降 76%。在 3 天内出现 ALT 或 AST 2 至 4 级升高。50% 的受试者出现 4 级 ALT 或 AST 升高,33% 的受试者出现 3 级 ALT 或 AST 升高,8% 的受试者出现 2 级 ALT 或 AST 升高。7 至 34 天(中位数为 15 天)内 ALT 和 AST 恢复至正常限度范围内(见【药物相互作用】)。
中效 CYP3A 诱导剂对洛拉替尼的影响:莫达非尼(一种中效 CYP3A 诱导剂)使单次口服 100 mg剂量本品的 AUCinf 下降了 23%,Cmax 下降了 22%(见【药物相互作用】)。
强效 CYP3A 抑制剂对洛拉替尼的影响:伊曲康唑是一种强效 CYP3A 抑制剂,可使单次口服 100 mg 剂量本品的AUCinf 升高 42%,Cmax 升高 24%(见【药物相互作用】)。
氟康唑对洛拉替尼的影响:同时口服本品(每日一次100 mg)与氟康唑(每日一次200 mg)后,氟康唑预计可使洛拉替尼的稳态 AUCtau 和 Cmax 分别升高 59% 和 28%(见【药物相互作用】)。
中效 CYP3A 抑制剂对洛拉替尼的影响:与维拉帕米或红霉素合用时,预计不会对稳态洛拉替尼药代动力学产生显著的临床影响。
洛拉替尼对 CYP3A 底物的影响:本品150 mg 每日一次口服给药15 天,可使咪达唑仑(一种敏感的 CYP3A 底物)2 mg 单次口服给药的 AUCinf 下降 64%,Cmax 下降 50%(见【药物相互作用】)。
洛拉替尼对 CYP2B6 底物的影响:本品100 mg 每日一次口服给药15 天,可使安非他酮(一种敏感的 CYP2B6 底物)100 mg 单次口服给药的 AUCinf 下降 25%,Cmax 下降 27%。
洛拉替尼对 CYP2C9 底物的影响:本品100 mg 每日一次口服给药15 天,可使甲苯磺丁脲(一种敏感的 CYP2C9 底物)100 mg 单次口服给药的 AUCinf 下降 43%,Cmax 下降 15%。
洛拉替尼对 UGT1A 底物的影响:本品100 mg 每日一次口服给药15 天,可使对乙酰氨基酚(一种 UGT1A 底物)100 mg 单次口服给药的 AUCinf 下降 45%,Cmax 下降 28%。
洛拉替尼对 P-gp 底物的影响:本品100 mg 每日一次口服给药15 天,可使非索非那定(一种 P-gp 底物)60 mg 单次口服给药的 AUCinf 下降 67%,Cmax 下降 63%(见【药物相互作用】)。
抑酸剂对洛拉替尼的影响:合用质子泵抑制剂雷贝拉唑对洛拉替尼的药代动力学未产生显著的临床影响。
体外研究
洛拉替尼对 CYP 酶的影响:洛拉替尼是 CYP3A 的一种时间依赖性抑制剂,也是诱导剂,且它可以激活 PXR,体内净效应是诱导。洛拉替尼诱导 CYP2B6 并激活人组成型雄甾烷受体 (CAR)。洛拉替尼和主要的循环代谢物 M8 不抑制 CYP1A2、CYP2B6、CYP2C8、CYP2C9、CYP2C19 或 CYP2D6。M8 不抑制 CYP3A。
M8 不诱导 CYP1A2、CYP2B6 或 CYP3A。
洛拉替尼对尿苷二磷酸葡糖醛酸 (UGT) 的影响:洛拉替尼和 M8 不抑制 UGT1A1、UGT1A4、UGT1A6、UGT1A9、UGT2B7 或 UGT2B15。
洛拉替尼对转运蛋白系统的影响:洛拉替尼是一种 P-gp 抑制剂,并且可以激活 PXR(可能诱导 P-gp),体内净效应是诱导。洛拉替尼可抑制有机阳离子转运蛋白 (OCT)1、有机阴离子转运蛋白 (OAT)3、多药物和毒素挤出物 (MATE)1 和肠乳腺癌耐药蛋白 (BCRP)。洛拉替尼不抑制有机阴离子转运多肽 (OATP)1B1、OATP1B3、OAT1、OCT2、MATE2K 或全身性 BCRP。M8 不抑制 P-gp、BCRP、OATP1B1、OATP1B3、OAT1、OAT3、OCT1、OCT2、MATE1 或 MATE2K。
药效动力学
在推荐剂量下洛拉替尼达到的稳态暴露量下,观察到 3 或 4 级高胆固醇血症和任何 3 或 4 级不良反应具有暴露-反应关系,在洛拉替尼暴露量升高时发生不良反应的可能性更高。
心脏电生理学
在研究 B7461001 中295 名接受 100 mg 每日一次推荐剂量的洛拉替尼并进行 ECG 测量的患者中,PR 间期相对于基线的最大平均变化为 16.4 ms(双侧 90% 置信区间上限 [CI] 为 19.4 ms)。在284 名基线 PR 间期 < 200 ms 的患者中,14% 的患者在开始洛拉替尼给药后的 PR 间期延长 ≥ 200 ms。PR 间期延长为浓度依赖性。1% 的患者出现房室传导阻滞。
在研究 B7461001 的活性评估阶段接受推荐剂量的洛拉替尼的 275 名患者中,未检测到 QTcF 间期出现相对于基线的较大平均增幅(即,> 20 ms)。
30℃以下保存。
25mg:
聚酰胺/铝/聚氯乙烯冷冲压成型固体药用复合硬片,药用铝箔。90片/盒,120片/盒。
100mg:
聚酰胺/铝/聚氯乙烯冷冲压成型固体药用复合硬片,药用铝箔。30片/盒。
36个月。
JX20220048。
25mg:国药准字HJ20220040
100mg:国药准字HJ20220041
名 称:Pfizer Europe MA EEIG
注册地址:Boulevard de la Plaine 17, 1050 Bruxelles, Belgium
企业名称:Pfizer Manufacturing Deutschland GmbH
生产地址:Mooswaldallee 1, 79108 Freiburg Im Breisgau, Germany
名 称:辉瑞投资有限公司
地 址:上海市南京西路1168号中信泰富广场36层
联系方式:400 910 0055
2022年4月27日
2025年6月4日