请仔细阅读说明书并在医师或药师指导下使用
本品为粉色椭圆形薄膜衣缓释片,除去包衣后显白色。
类风湿关节炎
托法替布缓释片适用于一种或多种TNF阻滞剂疗效不足或对其无法耐受的中度至重度活动性类风湿关节炎(RA)成人患者。
使用限制:不建议将托法替布缓释片与生物DMARD类药物或强效免疫抑制剂(如硫唑嘌呤和环孢霉素)联用。
银屑病关节炎
托法替布缓释片适用于对一种或多种改善病情抗风湿药(DMARD)应答不佳或不耐受的活动性银屑病关节炎(PsA)成人患者。本品可与甲氨蝶呤(MTX)联用。
强直性脊柱炎
托法替布缓释片适用于一种或多种TNF阻滞剂疗效不足或对其无法耐受的活动性强直性脊柱炎 (AS) 成人患者。
使用限制:不建议将托法替布缓释片与生物DMARD 类药物或强效免疫抑制剂(如硫唑嘌呤和环孢霉素)联用。
11 mg(按C16H20N6O计)
重要用药说明
- 请勿在淋巴细胞绝对计数低于500细胞/mm3、中性粒细胞绝对计数(ANC)低于1000细胞/mm3或血红蛋白水平低于9 g/dL的患者中开始托法替布缓释片用药。
- 出现淋巴细胞减少症、中性粒细胞减少症和贫血症时,建议中断给药(见【注意事项】,【不良反应】)。
- 如果患者发生严重感染,在感染得到控制之前应该中断托法替布缓释片给药 (见【注意事项】)。
- 托法替布缓释片与食物同服或不同服均可。
- 托法替布缓释片应整粒吞服。请勿压碎、掰开或咀嚼。
针对类风湿关节炎、银屑病关节炎和强直性脊柱炎的推荐剂量
表1列出了托法替布缓释片的成人推荐日剂量和针对接受CYP2C19和/或CYP3A4抑制剂治疗的;中度或重度肾功能损害(包括但不限于正在接受血液透析的重度肾功能不全患者)或中度肝功能损害;以及伴随有淋巴细胞减少症、中性粒细胞减少症或贫血症患者的剂量调整。
表1:针对类风湿关节炎1、银屑病关节炎和强直性脊柱炎患者1患者的托法替布推荐剂量
| 成人患者 | 托法替布缓释片11 mg每天一次 |
接受以下用药的患者:
| 减量至托法替布片5 mg每天一次 |
下列患者:
| 减量至托法替布片5 mg每天一次 对于正在接受血液透析的患者,应在透析日进行透析后给药。如果在透析操作前给药,不建议在患者透析后补充给药。 |
| 经重复检测确认淋巴细胞计数低于500细胞/mm3的患者 | 停药 |
| ANC介于500至1000细胞/mm3之间的患者 | 中断给药 当ANC高于1000时,重新给药11 mg每天两次 |
| ANC低于500细胞/mm3的患者 | 停药 |
| 血红蛋白水平低于8 g/dL或降低超过2 g/dL的患者 | 中断给药,直至血红蛋白数值恢复正常。 |
1托法替布缓释片在类风湿关节炎和强直性脊柱炎患者中可与甲氨蝶呤或其他非生物改善病情抗风湿药(DMARD)联合使用。
*不建议重度肝功能损伤患者使用托法替布缓释片。
从托法替布片转用托法替布缓释片
接受托法替布片 5 mg每天两次治疗的患者可在最后一次服用托法替布片 5 mg的下一剂转用托法替布缓释片 11 mg每天一次治疗。
以下具有临床意义的不良反应在说明书中其他章节描述:
- 严重感染(见【注意事项】)
- 恶性肿瘤和淋巴增殖性疾病(见【注意事项】)
- 血栓形成(见【注意事项】)
- 胃肠道穿孔(见【注意事项】)
- 超敏反应(见【注意事项】)
- 实验室检查异常(见【注意事项】)
临床试验经验
因为不同的临床研究是在不同的条件下进行的,所以一种药物在临床研究中观察到的不良反应发生率不能与另一种药物在临床研究中的发生率进行直接比较,因而不能预测在患者群体更广泛的临床实践中观察到的发生率。
类风湿关节炎
虽然已对其他剂量进行了研究,但托法替布缓释片的推荐剂量为11 mg,每天一次。托法替布缓释片 22 mg每天一次 不应用于类风湿关节炎 。在RA安全性研究1中,1455例患者接受托法替布5 mg每天两次治疗,1456例患者接受托法替布10 mg每天两次治疗,1451例患者接受TNF阻滞剂治疗,中位治疗时间为4.0年(见【临床试验】)。
下面的数据包括两项2期和五项3期双盲、安慰剂对照、多中心临床试验。在这些试验中,患者随机分组情况为托法替布单药治疗:5 mg,每天两次(292例患者)和10 mg,每天两次(306例患者);联合用药:托法替布 5 mg,每天两次(1044例患者)和10 mg,每天两次(1043例患者)与DMARD类联用(包括甲氨蝶呤);以及安慰剂组(809例患者)。所有七项安慰剂对照研究的方案都有这样一个前提,即服用安慰剂的患者要在第3个月或第6个月根据患者的缓解情况(疾病活动度未得到控制的)或研究设计接受托法替布治疗,从而使不良事件不能总是准确的归因于一种指定的治疗。因此,某些分析遵循的是在给定的时间间隔,将安慰剂和托法替布两组患者中根据研究设计或患者缓解情况而改变了治疗的患者从安慰剂组纳入托法替布组。基于前3个月的药物暴露情况在安慰剂和托法替布之间进行比较,基于前12个月的药物暴露情况在托法替布 5 mg每天两次和托法替布 10 mg每天两次之间进行比较。
长期安全性人群包括所有参加了一项双盲、安慰剂对照试验(包括早期开发阶段的研究),然后被纳入了两项长期安全性研究之一的患者。长期安全性研究的研究设计允许根据临床判断结果来调整托法替布的剂量。这限制了从剂量方面对长期安全性数据的解释。
最常见的严重不良反应是严重感染(见【注意事项】)。
双盲、安慰剂对照试验中,在0至3个月的药物暴露期间,因任何不良反应而停止治疗的患者比例托法替布组为4%,安慰剂组为3%。
总体感染情况
这七项安慰剂对照试验中,在0至3个月的药物暴露期间,5 mg每天两次治疗组和10 mg每天两次治疗组内感染的总体发生率分别为20%和22%,安慰剂组为18%。
随托法替布报告的最常见感染有上呼吸道感染、鼻咽炎、泌尿系统感染(分别为4%,3%和2%的患者)。
严重感染
这七项安慰剂对照试验中,在0至3个月的药物暴露期间,安慰剂组患者报告了1例严重感染(0.5次每100患者年),接受托法替布 5 mg或10 mg每天两次的患者中报告了11例严重感染(1.7次每100患者年)。5 mg每天两次托法替布治疗组和10 mg每天两次托法替布治疗组合并后与安慰剂组相减,得到的治疗组之间的发生率差异(以及相应的95%置信区间)为1.1(-0.4,2.5)次每100患者年。
这七项安慰剂对照试验中,在0至12个月药物暴露期间,5 mg每天两次托法替布治疗组报告了34例严重感染(2.7次每100患者年),10 mg每天两次托法替布治疗组报告了33例严重感染(2.7次每100患者年)。10 mg每天两次托法替布治疗组减去5 mg每天两次治疗组,得到的治疗组之间的发生率差异(以及相应的95%置信区间)为-0.1(-1.3,1.2)次每100患者年。
最常见的严重感染包括肺炎、蜂窝组织炎、带状疱疹,泌尿系统感染(见【注意事项】)。
结核病
这七项安慰剂对照试验中,在0至3个月的药物暴露期间,安慰剂组、5 mg每天两次托法替布治疗组和10 mg每天两次托法替布治疗组患者均未报告结核病。
这七项安慰剂对照试验中,在0至12个月药物暴露期间,5 mg每天两次托法替布治疗组患者报告了0例结核病,10 mg每天两次托法替布治疗组患者报告了6例结核病(0.5次每100患者年)。10 mg每天两次托法替布治疗组减去5 mg每天两次治疗组,得到的治疗组之间的发生率差异(以及相应的95%置信区间)为0.5(0.1,0.9)次每100患者年。
还报告了播散型结核病例。诊断出结核病之前的中位托法替布暴露时间为10个月(范围从152天至960天)(见【注意事项】)。
机会性感染(不包括结核病)
这七项安慰剂对照试验中,在0至3个月的药物暴露期间,安慰剂组、5 mg每天两次托法替布治疗组和10 mg每天两次托法替布治疗组患者均未报告机会性感染。
这七项安慰剂对照试验中,在0至12个月药物暴露期间,5 mg每天两次托法替布治疗组患者报告了4例机会性感染(0.3次每100患者年),10 mg每天两次托法替布治疗组患者报告了4例机会性感染(0.3次每100患者年)。10 mg每天两次托法替布治疗组减去5 mg每天两次治疗组,得到的治疗组之间的发生率差异(以及相应的95%置信区间)为0(-0.5,0.5)次每100患者年。
诊断出机会性感染之前的中位托法替布暴露时间为8个月(范围从41天至698天)(见【注意事项】)。
恶性肿瘤
这七项安慰剂对照试验中,在0至3个月的药物暴露期间,安慰剂组报告了0例恶性肿瘤(不包括非黑色素瘤皮肤癌癌[NMSC]),5 mg每天两次托法替布治疗组和10 mg每天两次托法替布治疗组患者共报告了2例(0.3次每100患者年)。5 mg每天两次托法替布治疗组和10 mg每天两次托法替布治疗组合并后与安慰剂组相减,得到的治疗组之间的发生率差异(以及相应的95%置信区间)为0.3(-0.1,0.7)次每100患者年。
这七项安慰剂对照试验中,在0至12个月药物暴露期间,5 mg每天两次托法替布治疗组报告了5例恶性肿瘤(不包括NMSC)(0.4次每100患者年),10 mg每天两次托法替布治疗组患者报告了7例(0.6次每100患者年)。10 mg每天两次托法替布治疗组减去5 mg每天两次托法替布治疗组,得到的治疗组之间的发生率差异(以及相应的95%置信区间)为0.2(-0.4,0.7)次每100患者年。这些恶性肿瘤之一是一例淋巴瘤,在0至12个月期间,出现于托法替布10 mg每天两次治疗组的1例患者。
最常见的恶性肿瘤,包括长期扩展研究期间观察到的恶性肿瘤,为肺癌和乳腺癌,其次为胃癌、结直肠癌、肾细胞癌、前列腺癌、淋巴瘤、恶性黑色素瘤(见【注意事项】)。
实验室检查异常
淋巴细胞减少症
在临床安慰剂对照试验中,在前3个月的药物暴露期间,5 mg每天两次托法替布治疗组和10 mg每天两次托法替布治疗组合并后,经检测确认的绝对淋巴细胞计数下降至低于500细胞/mm3的患者为0.04%。
经检测确认的淋巴细胞计数低于500细胞/mm3与治疗和严重感染的发生率增加有关(见【注意事项】)。
中性粒细胞减少症
在临床安慰剂对照试验中,在前3个月的药物暴露期间,5 mg每天两次托法替布治疗组和10 mg每天两次托法替布治疗组合并后,经检测确认的ANC下降至低于1000细胞/mm3的患者为0.07%。
没有在任何治疗组中观察到ANC下降至低于500细胞/mm3。
中性粒细胞减少症和严重感染的发生之间没有明确关系。
在长期的安全性人群中,ANC确定性下降的模式和发生率与在临床对照试验中观察到的发生率保持一致(见【注意事项】)。
肝酶升高
在托法替布治疗组患者中观察到了肝酶确定性增高至大于3倍正常上限(3xULN)。在出现肝酶增高的患者中,治疗方案调整后,如减少DMARD合并用药的剂量,中断托法替布治疗或降低托法替布剂量,可使肝酶降低或正常化。
在安慰剂对照、单药治疗试验中(0-3个月),安慰剂组、5 mg每天两次托法替布治疗组和10 mg每天两次托法替布治疗组中观察到的ALT或AST升高的发生率无显著差异。
在使用DMARD做背景治疗的对照试验中(0-3个月),在安慰剂组、5 mg每天两次托法替布治疗组和10 mg每天两次托法替布治疗组中分别观察1.0%、1.3%和1.2%的患者ALT升高到3倍正常值上限之上。在这些试验中,在安慰剂组、5 mg每天两次托法替布治疗组和10 mg每天两次托法替布治疗组中AST升高到3倍正常值上限之上的患者比例分别为0.6%,0.5%和0.4%。
10 mg每天两次托法替布治疗组报告了1例药源性肝损伤,治疗持续时间大约为2.5个月。该患者出现症状性AST和ALT值升高超过3倍ULN,并且胆红素升高超过2倍ULN,需要住院治疗和肝活检。
血脂升高
在安慰剂对照临床试验中,在药物暴露一个月时观察到血脂参数(总胆固醇、低密度脂蛋白胆固醇、高密度脂蛋白胆固醇、甘油三酯)呈剂量相关性升高,其后保持稳定。在安慰剂对照临床试验中,前3个月药物暴露期间的血脂参数变化总结如下:
- 5 mg每天两次托法替布治疗组的平均LDL胆固醇增加了15%,10 mg每天两次托法替布治疗组的平均LDL胆固醇增加了19%。
- 5 mg每天两次托法替布治疗组的平均HDL胆固醇增加了10%,10 mg每天两次托法替布治疗组的平均HDL胆固醇增加了12%。
- 托法替布治疗组患者中的平均LDL/HDL比值基本保持不变。
在安慰剂对照临床试验中,升高的LDL胆固醇和ApoB随着他汀类药物治疗而相应缓解,下降至治疗前水平。
在长期安全性人群中,血脂参数的升高情况与安慰剂对照临床试验中所观察到的结果保持一致。
血清肌酐升高
在安慰剂对照临床试验中,在托法替布治疗组观察到了剂量相关性血清肌酐升高。在12个月的合并性安全性分析中血清肌酐的平均增幅为<0.1 mg/dL;然而,随着长期扩展研究中暴露时间的增加,高达2%的患者因为研究方案规定的停药标准而停止托法替布治疗,即肌酐增高超过基线值的50%。尚未明确所观察到的血清肌酐升高现象的临床意义。
其他不良反应
在联用或不联用DMARD的情况下,5 mg每天两次托法替布治疗组或10 mg每天两次托法替布治疗组患者中发生率≥2%并比安慰剂组的报告比例至少高出1%的不良反应,如表2所示。
表2:托法替布联用或不联用DMARD(0-3个月)治疗类风湿关节炎临床试验中的常见不良反应*
| 托法替布 5 mg每天两次 | 托法替布 10 mg每天两次** | 安慰剂 | |
|---|---|---|---|
| 首选术语 | N =1336 (%) | N =1349 (%) | N =809 (%) |
| 上呼吸道感染 | 4 | 4 | 3 |
| 鼻咽炎 | 4 | 3 | 3 |
| 腹泻 | 4 | 3 | 2 |
| 头痛 | 4 | 3 | 2 |
| 高血压 | 2 | 2 | 1 |
| N代表来自七项临床试验的随机分组和接受治疗的患者。 * 接受任一托法替布剂量治疗的患者中≥2%患者报告且比安慰剂组报告的比例高出≥1%。 ** 托法替布片 10 mg 每天两次的剂量不应用于类风湿关节炎。 | |||
发生在安慰剂对照和开放式扩展研究中的其他不良反应包括:
血液及淋巴系统疾病:贫血
感染及侵染类疾病:憩室炎
代谢及营养类疾病:脱水
精神病类:失眠
各类神经系统疾病:感觉异常
呼吸系统、胸及纵隔疾病:呼吸困难,咳嗽,鼻窦充血,间质性肺病(仅限于类风湿关节炎患者,并且某些是致命性的)
胃肠系统疾病:腹痛,消化不良,呕吐,胃炎,恶心
肝胆系统疾病:肝脂肪变性
皮肤和皮下组织类疾病:皮疹,红斑,瘙痒
各种肌肉骨骼及结缔组织疾病:肌肉骨骼疼痛,关节痛,肌腱炎,关节肿胀
良性、恶性和性质不明的肿瘤(包括囊肿和息肉):非黑色素瘤皮肤癌
全身性疾病及给药部位各种反应:发热,疲劳,外周水肿
银屑病关节炎
在有活动性银屑病关节炎(PsA)患者中进行的2项双盲、III期临床试验中研究了托法替布 5 mg每天两次和10 mg每天两次给药方案。尽管曾研究了托法替布的其他剂量治疗方案,但托法替布缓释片的推荐剂量是11 mg每天一次。托法替布10 mg每天两次的剂量不应用于银屑病关节炎。
研究PsA-I(NCT01877668)的持续时间为12个月,入组了对非生物DMARD反应不足及未接受过TNF阻滞剂治疗的患者。研究PsA-I包括为期3个月的安慰剂对照期同时也包括了连续12个月每两周一次皮下给药阿达木单抗40 mg的给药组。
研究PsA-II(NCT01882439)的持续时间为6个月,入组了对至少1种获批TNF阻滞剂反应不足的患者。该临床试验包括为期3个月的安慰剂对照期。
在这些合并III期临床试验中,238例患者被随机分配至托法替布5 mg每天两次治疗组,236例患者被随机分配至托法替布10 mg每天两次治疗组。要求临床试验中的所有患者均接受稳定剂量的非生物DMARD治疗[多数(79%)接受甲氨蝶呤]。随机分配至托法替布治疗组的研究人群(474例患者)包括45例(9.5%)≥65岁的患者和66例(13.9%)基线时有糖尿病的患者。
在有活动性银屑病关节炎且接受托法替布治疗患者中观察到的安全性特征与在类风湿关节炎患者中的观察结果一致。
强直性脊柱炎
在一项确证性双盲安慰剂对照III期临床试验(研究AS-I)和一项剂量范围II期临床试验(研究AS-II)中,在活动性强直性脊柱炎(AS)患者中对托法替布5 mg每天两次给药进行了研究。
研究AS-I (NCT03502616)的持续时间为48周,入组了对至少2种NSAID疗效不足的患者。研究AS-I包括一个为期16周的双盲阶段,患者接受托法替布5 mg或安慰剂每天两次给药,以及一个为期32周的开放性治疗阶段,所有患者均接受托法替布5 mg每天两次给药。
研究AS-II(NCT01786668)的持续时间为16周,入组了对至少2种NSAID疗效不足的患者。该临床试验包括12周的治疗期,患者接受托法替布2 mg、5 mg、10 mg或安慰剂每天两次给药。
在II期和III期合并临床试验中,共有420例患者接受了托法替布2 mg、5 mg或10 mg每天两次治疗。其中,316例患者接受托法替布5 mg每天两次治疗,最长持续48周。在合并后的双盲阶段,185例患者随机接受托法替布5 mg每天两次治疗,187例接受安慰剂,最长持续16周。允许合并使用稳定剂量的非生物制剂DMARD、NSAID或皮质类固醇(≤10 mg/天)进行治疗。随机分配并接受托法替布治疗的研究人群包括13例(3.1%)年龄≥65岁的患者和18例(4.3%)基线时患有糖尿病的患者。
在接受托法替布治疗的AS患者中观察到的安全性特征与在RA患者中观察到的安全性特征一致。
与接受5 mg每天两次的患者相比,接受托法替布治疗10 mg每天两次的患者中观察到剂量依赖性不良反应,包括以下各项:带状疱疹感染、严重感染和NMSC。
上市后经验
在托法替布的批准后使用期间已发现以下不良反应。由于这些不良反应由规模不确定的人群自发报告,因此并不总能可靠地估算其频率或确定与药物暴露的因果关系。
免疫系统异常:药物性超敏反应(观察到如血管性水肿和荨麻疹等事件)。
皮肤和皮下组织疾病:痤疮。
无
严重感染
在接受托法替布治疗的患者中曾报道过细菌、分枝杆菌、侵袭性真菌、病毒或其他机会致病菌引起的严重感染,偶有致死性感染。随托法替布报告的最常见严重感染包括肺炎、蜂窝组织炎、带状疱疹、泌尿道感染、憩室炎和阑尾炎。在机会性感染中,随托法替布报告的有结核和其他分枝杆菌感染、隐球菌病、组织胞浆菌病、食道念珠菌感染、肺囊虫病、多发性皮肤带状疱疹、巨细胞病毒感染、BK病毒感染以及李氏杆菌病。有些患者表现为播散性感染,而非局部性疾病,并且往往同时服用了免疫抑制剂,如甲氨蝶呤或皮质类固醇。
也可能发生临床研究中没有报道的其他严重感染(例如,球孢子菌病)。
避免在严重活动性感染患者,包括局部感染患者中开始托法替布缓释片用药。在以下患者中开始托法替布缓释片用药之前应该考虑治疗的风险和获益:
- 患有慢性或复发性感染
- 曾有结核病接触史
- 具有严重或机会性感染史
- 曾在结核病或分枝杆菌流行地区居住或旅游
- 患有可能使其易于受感染的基础病症
使用托法替布缓释片治疗期间和之后应该密切监测所有患者是否出现发生感染的症状和体征。如果患者出现严重感染、机会性感染或脓毒症,应该中断托法替布缓释片给药。使用托法替布缓释片治疗期间发生新发感染的患者应该进行适用于免疫功能低下患者的及时和完整的诊断性检测;应该开始适当的抗菌治疗,并且对患者进行密切监测。
也建议有慢性肺部疾病史或患有间质性肺疾病的患者慎用,因为这些患者更容易发生感染。
感染风险可能随着淋巴细胞减少程度的增加而增加,在评估个体患者感染风险时应考虑淋巴细胞计数。针对淋巴细胞减少症,建议根据【用法用量】项下淋巴细胞计数标准停药和进行监测。
结核病
开始托法替布缓释片给药之前以及给药期间,应该根据适用的指南,对患者进行潜伏性或活动性感染的评价和检测。
在具有潜伏性或活动性结核病既往病史的患者中开始进行托法替布缓释片给药之前,还应该考虑进行抗结核治疗,在这些患者中,不能确认一个充分疗程,并且虽然患者的潜伏性结核病检测结果呈阴性,但仍存在结核病感染的风险因素。建议咨询结核病治疗专科医生,以便帮助决定针对某一患者个体开始抗结核治疗是否适当。
应该密切监测患者是否出现结核病的症状和体征,包括开始治疗前潜伏性结核感染检测结果呈阴性的患者。
在托法替布缓释片给药之前,应该使用标准的抗分枝杆菌疗法对潜伏性结核病患者进行治疗。
病毒再激活
在托法替布的临床研究中观察到了病毒再激活现象,包括疱疹病毒再激活病例(如带状疱疹)。在接受托法替布治疗的患者中已报告乙型肝炎再激活的上市后病例。尚未明确托法替布缓释片对慢性病毒性肝炎再激活的影响。临床试验中排除了乙型或丙型肝炎筛查结果呈阳性的患者。在开始托法替布缓释片治疗之前,应根据临床指导原则进行病毒性肝炎筛查。在接受托法替布缓释片治疗的患者中,带状疱疹风险会升高,且在接受托法替布治疗的日本和韩国患者中风险似乎更高。
死亡
在一项大型、随机、上市后安全性研究(RA 安全性研究 1)中,观察到接受托法替布 5 mg 每天两次或托法替布 10 mg 每天两次治疗的 50 岁及以上的具有至少一个心血管风险因素的类风湿关节炎患者的全因死亡率(包括心源性猝死)高于接受 TNF 阻滞剂治疗的患者。在托法替布 5 mg 每天两次、托法替布 10 mg 每天两次和 TNF 阻滞剂治疗组中,每 100 患者年的全因死亡发生率分别为 0.88、1.23 和 0.69(见【临床试验】)。在开始或继续使用托法替布治疗前,应考虑个体患者的获益与风险。
托法替布缓释片22 mg 每天一次不应用于类风湿关节炎、银屑病关节炎或强直性脊柱炎。
恶性肿瘤及淋巴增生性疾病
在托法替布的临床研究中观察到了恶性肿瘤,包括淋巴瘤和实体瘤(见【不良反应】)。
在 RA 安全性研究 1 中,观察到托法替布 5 mg 每天两次或托法替布 10 mg 每天两次治疗组患者的恶性肿瘤(不包括 NMSC)发生率高于 TNF 阻滞剂组。在托法替布 5 mg 每天两次、托法替布 10 mg 每天两次和 TNF 阻滞剂治疗组中,每 100 患者年的恶性肿瘤(不包括 NMSC)发生率分别为 1.13、1.13 和 0.77。吸烟患者或既往有吸烟经历的患者面临更高风险(见【临床试验】)。
在托法替布 5 mg 每天两次和托法替布 10 mg 每天两次治疗组患者中,观察到淋巴瘤和肺癌(RA 安全性研究 1 中所有恶性肿瘤事件的子集)发生率高于 TNF 阻滞剂治疗组。每 100 患者年的淋巴瘤发生率分别为 0.07(托法替布 5 mg 每天两次)、0.11(托法替布 10mg 每天两次)和 0.02(TNF 阻滞剂)。吸烟患者或既往有吸烟经历的患者中,每 100 患者年的肺癌发生率分别为 0.48(托法替布 5 mg 每天两次)、0.59(托法替布 10 mg 每天两次)和 0.27(TNF 阻滞剂)(见【临床试验】)。
在开始或继续使用托法替布治疗前,应考虑个体患者的获益与风险,特别是在已知具有恶性肿瘤(不包括已成功治愈的 NMSC)、在治疗期间发生恶性肿瘤以及吸烟患者或既往有吸烟经历的患者中。托法替布缓释片22 mg每天一次不应用于类风湿关节炎 、银屑病关节炎或强直性脊柱炎。
在两项AS的安慰剂对照临床研究中,420例接受托法替布联用或不联用非生物制剂 DMARD治疗长达48周的患者中有0例患恶性肿瘤(不包括NMSC),187例接受安慰剂联用或不联用非生物制剂DMARD治疗长达16周的患者中有0例患恶性肿瘤。
2 期 B 阶段,在首次进行肾移植的患者中展开了对照型剂量范围研究,所有患者都接受了巴利昔单抗诱导治疗、高剂量皮质激素以及霉酚酸类药品,在 218 例使用托法替布治疗的患者中观察到 5 例(2.3%)EB 病毒相关性移植后淋巴增生性疾病,而 111 例环孢霉素治疗组患者中为 0 例。
在临床研究和上市后中观察到其他恶性肿瘤,包括但不限于肺癌、乳腺癌、黑色素瘤、前列腺癌和胰腺癌。
非黑色素瘤皮肤癌
在接受托法替布治疗的患者中已有非黑色素瘤皮肤癌(NMSC)的报告。建议对皮肤癌风险增高的患者进行定期的皮肤检查。
重大心血管不良事件
在 RA 安全性研究 1 中,50 岁及以上的具有至少一项心血管风险因素的类风湿关节炎患者在接受托法替布 5 mg 每天两次或托法替布 10 mg 每天两次治疗后,重大心血管不良事件(MACE),(定义为心源性死亡、非致命性心肌梗死[MI]和非致命性卒中)的发生率高于 TNF 阻滞剂治疗组。每 100 患者年的 MACE 发生率分别为 0.91(托法替布 5 mg 每天两次)、1.11(托法替布 10 mg 每天两次)和 0.79(TNF 阻滞剂)。每 100 患者年的致命性或非致命性心肌梗死发生率分别为 0.36(托法替布 5 mg 每天两次)、0.39(托法替布 10mg 每天两次)和 0.20(TNF 阻滞剂)(见【临床试验】)。吸烟患者或既往有吸烟经历的患者面临更高风险。
在开始或继续使用托法替布治疗前,应考虑个体患者的获益与风险,特别是在吸烟患者或既往有吸烟经历的患者中,以及具有其他心血管风险因素患者中。应告知患者严重心血管事件的症状及其应对措施。如果患者发生心肌梗死或卒中,应停用托法替布。托法替布缓释片22 mg每天一次不应用于类风湿关节炎、银屑病关节炎或强直性脊柱炎。
血栓形成
在接受托法替布和其他 Janus 激酶(JAK)抑制剂(用于治疗炎症状态)治疗的患者中,发生了血栓形成(包括肺栓塞(PE)、深静脉血栓形成(DVT)和动脉血栓形成)。大 多数这些事件症状严重,部分导致死亡(见【注意事项】)。
在 RA 安全性研究 1 中,50 岁及以上的具有至少一个心血管风险因素的类风湿关节炎 患者中接受托法替布 5 mg 每天两次或托法替布 10 mg 每天两次治疗,观察到这些事件的 发生率高于接受 TNF 阻滞剂治疗的患者。每 100 患者年的 DVT 发生率分别为 0.22(托法 替布 5 mg 每天两次)、0.28(托法替布 10 mg 每天两次)和 0.16(TNF 阻滞剂)。每 100 患者年的 PE 发生率分别为 0.18(托法替布 5 mg 每天两次)、0.49(托法替布 10 mg 每天 两次)和 0.05(TNF 阻滞剂)(见【临床试验】)。
托法替布缓释片22 mg每天一次不应用于类风湿关节炎、银屑病关节炎或强直性脊柱炎。
立即评估有血栓形成症状的患者,并在出现血栓形成症状的患者中停用托法替布缓释 片。
应避免将托法替布缓释片用于血栓形成风险可能增加的患者。
胃肠道穿孔
托法替布的临床研究中已报道了胃肠道穿孔事件,但JAK抑制作用在这些事件中所起的作用不明。在这些研究中,许多类风湿关节炎患者正在接受非甾体类抗炎药物(NSAID)背景治疗。
胃肠道穿孔风险可能增加的患者(例如,具有憩室炎病史或正在接受NSAID的患者)应该慎用托法替布缓释片。应该对新发腹部症状的患者及时进行评价,以便及早识别胃肠道穿孔(见【不良反应】)。
超敏反应
在接受托法替布缓释片治疗的患者中已观察到可能反映药物性超敏反应的血管性水肿和荨麻疹等反应。部分为严重事件。如果发生严重超敏反应,应立即停用托法替布,同时评估可能的诱因或引起反应的原因(见【不良反应】)。
实验室检查异常
淋巴细胞异常
在12个月的治疗期间,在药物暴露一个月时,出现托法替布治疗相关性初始淋巴细胞增多,随后逐渐下降,平均绝对淋巴细胞计数大约比基线低10%。淋巴细胞计数低于500细胞/mm3时引起严重感染的发生率增加。
避免在淋巴细胞计数低(即低于500细胞/mm3)的患者中开始托法替布缓释片治疗。在发生确定性淋巴细胞绝对计数低于500细胞/mm3的患者中,不建议使用托法替布缓释片治疗。
在基线时以及之后每3个月对淋巴细胞计数监测一次。基于淋巴细胞计数建议的剂量调整参见【用法用量】。
中性粒细胞减少症
与安慰剂相比,托法替布治疗与中性粒细胞减少症(低于2000细胞/mm3)的发生率增加有关。
避免在中性粒细胞计数低(即ANC低于1000细胞/mm3)的患者中开始托法替布缓释片治疗。对于出现ANC持续处于500-1000细胞/mm3的患者,中断托法替布缓释片给药直至ANC大于或等于1000细胞/mm3。在出现ANC小于500细胞/mm3的患者中,不推荐使用托法替布缓释片治疗。
在基线时以及治疗4-8周后监测中性粒细胞计数,此后每3个月监测一次。基于ANC结果建议的剂量调整参见【用法用量】。
贫血
避免在血红蛋白水平低(即低于9 g/dL)的患者中开始托法替布缓释片治疗。在治疗时出现血红蛋白水平低于8 g/dL或血红蛋白水平降幅大于2g/dL的患者中,应该中断托法替布缓释片治疗。
在基线时以及治疗4-8周后监测血红蛋白,此后每3个月监测一次。基于血红蛋白结果建议的剂量调整参见【用法用量】。
肝酶升高
与安慰剂组相比,托法替布治疗与肝酶升高的发生率上升有关。这些异常大多数出现于使用DMARD(主要是甲氨蝶呤)为背景治疗的研究项目中。
建议对肝功能检查项目进行常规监测,迅速调查肝酶升高的原因,以识别潜在的药物性肝损伤病例。如果怀疑出现药物性肝损伤,则应中断托法替布缓释片给药直至排除此诊断结果。
血脂升高
托法替布治疗与血脂参数的升高呈剂量依赖性,包括总胆固醇、低密度脂蛋白(LDL)胆固醇和高密度脂蛋白(HDL)胆固醇。一般在6周内观察到最大影响。LDL/HDL胆固醇比值无临床相关变化。这些血脂参数升高对心血管疾病发病率和死亡率的影响尚未确定。
应该在开始托法替布缓释片治疗约4-8周后进行血脂参数的评估。
根据临床指导原则对患者进行高脂血症管理。
疫苗接种
避免活疫苗接种与托法替布缓释片给药同时进行。活疫苗接种和托法替布治疗开始之间的间隔应符合目前关于免疫抑制药物的疫苗接种指南。
一例患者在接种减毒活疫苗(Zostavax)16天后,开始托法替布(5 mg,每天两次)治疗2天后发生了水痘带状疱疹病毒疫苗株感染。该患者未接触过水痘病毒,因为该患者在基线检查时没有既往水痘感染史和没有抗水痘抗体。患者在停用托法替布并使用标准剂量的抗病毒药物治疗后恢复。
在开始托法替布缓释片治疗之前,要依照现行的免疫指导原则进行免疫接种。
使用诸如托法替布缓释片的不变形缓释制剂的胃肠道梗阻风险
与任何其他不变形物质一样,已患有严重胃肠狭窄的患者(病理性或医源性)应慎用托法替布缓释片。在使用其他不变形缓释剂型药物的已知胃肠狭窄患者中,罕见梗阻症状的报告。
糖尿病患者用药
由于糖尿病患者人群中的感染发生率通常较高,因此治疗糖尿病患者时应谨慎。
肾功能损害
中度和重度损害
与接受托法替布治疗的肾功能正常患者相比,接受托法替布治疗的中度和重度肾功能损害患者的托法替布血药浓度更高。因此在中度或重度肾功能损害患者(包括但不限于正在接受血液透析的重度肾功能不全患者)中,建议调整托法替布缓释片剂量(见【用法用量】)。
轻度损害
轻度肾功能损害患者不需要调整剂量。
肝功能损害
重度损害
尚未在重度肝功能损害患者中研究托法替布缓释片;因此,不建议重度肝功能损害患者使用托法替布缓释片。
中度损害
与接受托法替布治疗的肝功能正常患者相比,接受托法替布治疗的中度肝功能损害患者的托法替布血药浓度更高(见【临床药理】)。升高的血药浓度可能会增加某些不良反应的风险。因此,在中度肝功能损害患者中,建议调整托法替布缓释片剂量(见【用法用量】)。
轻度损害
轻度肝功能损害患者不需要调整托法替布缓释片的剂量。
乙型或丙型肝炎血清学
尚未在乙型肝炎病毒或丙型肝炎病毒血清学检查结果呈阳性的患者中研究托法替布缓释片的安全性和有效性。
孕妇
风险总结
妊娠期暴露登记(11例暴露患者入组)、药物警戒和已发表文献中托法替布缓释片用药的现有数据不足以得出与药物相关的重大出生缺陷、流产或其他母体或胎儿不良结局风险的结论。在妊娠期,母体和胎儿都面临着与类风湿关节炎相关的风险(见临床注意事项)。
尚未在适用人群中得出重大出生缺陷和流产的背景风险。所有妊娠女性均有发生出生缺陷、流产或其他不良结局的背景风险。在美国普通人群中,临床确诊妊娠发生重大出生缺陷和流产的背景风险分别为2 - 4%和15 - 20%。
临床注意事项
疾病相关母体和/或胚胎/胎儿风险
已发表数据表明,在患类风湿关节炎的女性中,疾病活动度增加与出现不良妊娠结局风险相关。不良妊娠结局包括早产(妊娠37周前分娩)、低出生体重儿(低于2500 g)以及出生时相对于胎龄较小。
哺乳期
风险总结
基于已发表数据,认为托法替布存在于人乳中。托法替布对母乳喂养婴 儿影响的数据仅限于少量病例且未报告不良影响。尚无对乳汁生成有影响的数据。鉴于在接受托法替布缓释片治疗的成人中观察到严重不良反应,如严重感染风险增加,应告知患者,不建议在治疗期间和末次托法替布缓释片给药至少36小时内(约6个消除半衰期)进行母乳喂养。
生育力
对于具有生育能力的女性,应计划生育和避孕。
托法替布缓释片在儿童患者中的安全性和有效性尚未建立。
在参加全球五项临床研究的3315例患者中,总计有505例类风湿关节炎患者为65岁及以上,包括71例75岁以上的患者。托法替布治疗组65岁及以上的受试者中,严重感染的发生率高于65岁以下的受试者。由于一般情况下老年人群中的感染发病率较高,故用于老年人的治疗时应谨慎(见【注意事项】)。
表3列出了与托法替布缓释片合并用药时具有临床重要的药物相互作用的药物以及预防或管理药物相互作用的说明。
表3: 与其他药物合并用药时影响托法替布缓释片的临床相关相互作用
| 强效CYP3A4抑制剂(如酮康唑) | |
|---|---|
| 临床影响 | 托法替布暴露量增加 |
| 干预 | 建议调整托法替布缓释片剂量 (见【用法用量】,【临床药理】图2) |
| 中等CYP3A4抑制剂与强效CYP2C19抑制剂(如氟康唑)合并用药 | |
| 临床影响 | 托法替布暴露量增加 |
| 干预 | 建议调整托法替布缓释片剂量 (见【用法用量】,【临床药理】图2) |
| 强效CYP3A4诱导剂(如利福平) | |
| 临床影响 | 托法替布暴露量减少并可能导致临床反应缺失或减少 |
| 干预 | 不建议与托法替布缓释片合并用药 (见【临床药理】图2) |
| 免疫抑制药物(如硫唑嘌呤、他克莫司、环孢霉素) | |
| 临床影响 | 免疫抑制风险增加;尚未在类风湿关节炎、银屑病关节炎或强直性脊柱炎患者中开展与生物DMARD或强效免疫抑制的合并用药的研究。 |
| 干预 | 不建议与托法替布缓释片合并用药 (见【适应症】,【临床药理】图2) |
没有针对托法替布缓释片过量的专用解毒剂。在药物过量的情况下,建议监测患者体征和不良反应症状。
在一项接受血液透析的终末期肾病(ESRD)受试者研究中,血浆托法替布浓度在血液透析期内下降更为快速,并且通过透析机清除量/进入透析机的血流总量计算的透析效率较高[平均值(标准差)= 0.73(0.15)]。但由于托法替布主要经非肾脏途径清除,因此通过血液透析产生的总消除分数较低,从而限制了血液透析在治疗托法替布缓释片过量方面的价值。
托法替布缓释片口服给药后,在4小时内达到血浆药物浓度峰值,清除半衰期约为6-8小时。每天一次给药后,在48小时内达到稳态浓度,药物蓄积可以忽略不计。托法替布缓释片11 mg每天一次的AUC和Cmax与托法替布片5 mg每天两次相当。
表4: 多次口服给药后托法替布/托法替布缓释片的药代动力学参数
| PK 参数a (CV%) | 托法替布 | 托法替布缓释片 |
|---|---|---|
| 给药方案 | 5 mg 每天两次 | 11 mg 每天一次 |
| AUC24 (ng·hr/mL) | 263.4 (15) | 269.0 (18) |
| Cmax (ng/mL) | 42.7 (26) | 38.2 (15) |
| Cmin (ng/mL) | 1.41 (40) | 1.07 (69) |
| Tmax(小时) | 1.0 (0.5 至 14.0b) | 4.0 (3.0 至 4.0) |
a 数值表示几何平均值,Tmax 除外,其显示为中位值(范围)。
缩略语:AUC24 = 时间零点至 24 小时浓度时间曲线下面积;Cmax = 最高血药浓度;Cmin = 最低血药浓度;Tmax = 至 Cmax 的时间;CV = 变异系数。
b 超过 12 小时的数值在(每天两次托法替布给药方案的早晨给药后 12 小时后)晚间给药之后获取。
吸收
托法替布的绝对口服生物利用度为74%。托法替布与高脂肪饮食合用时,AUC没有变化,而Cmax降低了32%。在临床试验中,托法替布给药不受食物影响(见【用法用量】)。
托法替布缓释片与高脂肪饮食合用时,AUC没有变化,而Cmax增加了27%,Tmax延长了约1小时。
在一项纳入26名中国健康男性(含18至55岁)的生物等效性研究中,证实空腹状态托法替布缓释片11 mg 每天一次在单次给药和稳态条件下,AUC及Cmax均与托法替布片10 mg (5 mg,每天两次) 给药后的AUC及Cmax等效。
分布
静脉给药后的分布容积为87 L。托法替布的蛋白结合率约为40%。托法替布主要与白蛋白结合,看起来不与α1酸性糖蛋白结合。托法替布在红细胞和血浆之间均匀分布。
代谢和排泄
托法替布的清除机制为,约70%肝脏代谢,30%的母体药物经肾脏排泄。托法替布的代谢主要由CYP3A4介导,同时CYP2C19有少量贡献。在人体放射性标记研究中,原型托法替布占总循环放射性的65%以上,余下的35%归因于8个代谢产物,各占不到8%的总放射性。托法替布的药理活性是母体分子引起的。
特殊人群
考虑到患者之间的肾功能差异(即,肌酐清除率),根据年龄、体重、性别和种族,患者人群中作为群体药代一部分的协变量评价表明,没有临床相关性托法替布暴露量变化(图1)。观察到体重和分布容积之间的关系大致呈线性,导致体重较轻的患者中的浓度峰值(Cmax)较高而浓度谷值(Cmin)较低。然而,这种差异不认为具有临床相关性。
托法替布的肾和肝功能损伤及其他内在因素对托法替布药代动力学的影响如图1所示。
图1:内因对托法替布药代动力学的影响
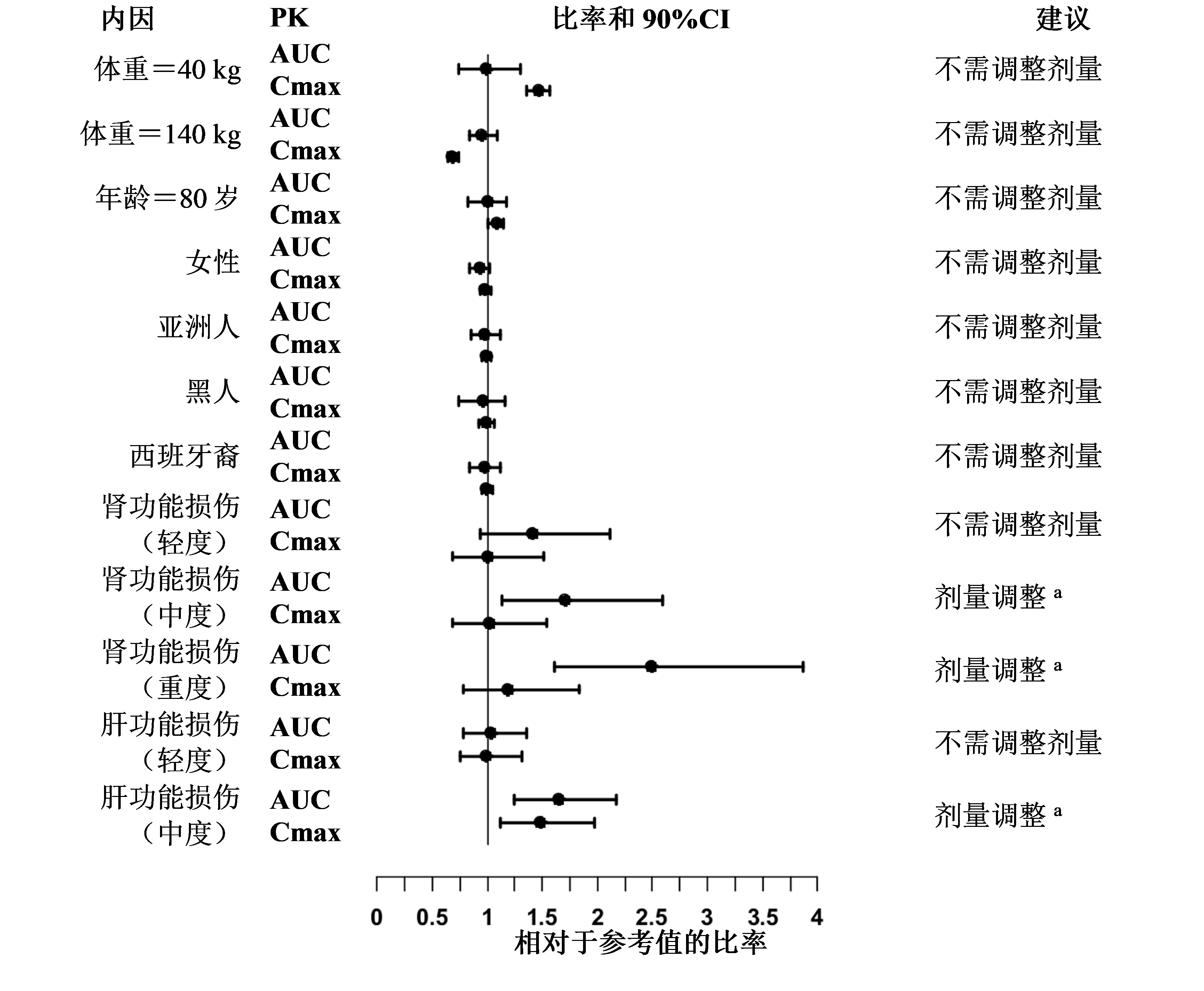
注:体重、年龄、性别和种族的参考比较值分别为70kg、55岁、男性和白种人;肾功能和肝功能损伤数据的参考组是肾和肝功能正常的受试者。
a 在类风湿关节炎、银屑病关节炎或强直性脊柱炎患者中的剂量调整(见【用法用量】)。
在通过血液透析维持的ESRD受试者中,平均AUC较既往的健康受试者数据高出约40%,这与托法替布的肾脏清除率约占总清除率的30%的情况相符。在通过血液透析维持的ESRD且患有类风湿关节炎、银屑病关节炎或强直性脊柱炎的患者中推荐剂量调整(见用法用量)。
药物相互作用
托法替布缓释片影响其他药物药代的可能性
体外研究表明,在10 mg每天给药两次的剂量下,浓度相当于稳态Cmax时,托法替布不能显著性抑制或诱导主要的人体药物代谢CYP酶类(CYP1A2,CYP2B6,CYP2C8,CYP2C9,CYP2C19,CYP2D6和CYP3A4)的活性。这些体外实验结果通过一项人体药物相互作用研究得到了证实,该项研究显示,与托法替布合用时,咪达唑仑(一种高度敏感的CYP3A4底物)的药代动力学没有变化。
体外研究表明,在10 mg每天给药两次的剂量下,浓度超过250倍稳态Cmax时,托法替布不能显著性抑制主要的人体药物代谢尿苷5'-二磷酸葡糖醛酸转移酶(UGT)[UGT1A1、UGT1A4、UGT1A6、UGT1A9和UGT2B7]的活性。
在类风湿关节炎患者中,托法替布的口服清除率不随时间变化,表明托法替布不会使类风湿关节炎患者中的CYP酶活性正常化。因此,与托法替布缓释片联合用药预期不会在类风湿关节炎患者中导致CYP底物的代谢出现临床相关性增加。
体外数据表明,在治疗浓度下,托法替布抑制转运体,如P-糖蛋白、有机阴离子或阳离子转运体的可能性低。
托法替布给药后,合并用药的推荐药物如图2所示。
图2.托法替布对其他药物药代动力学的影响
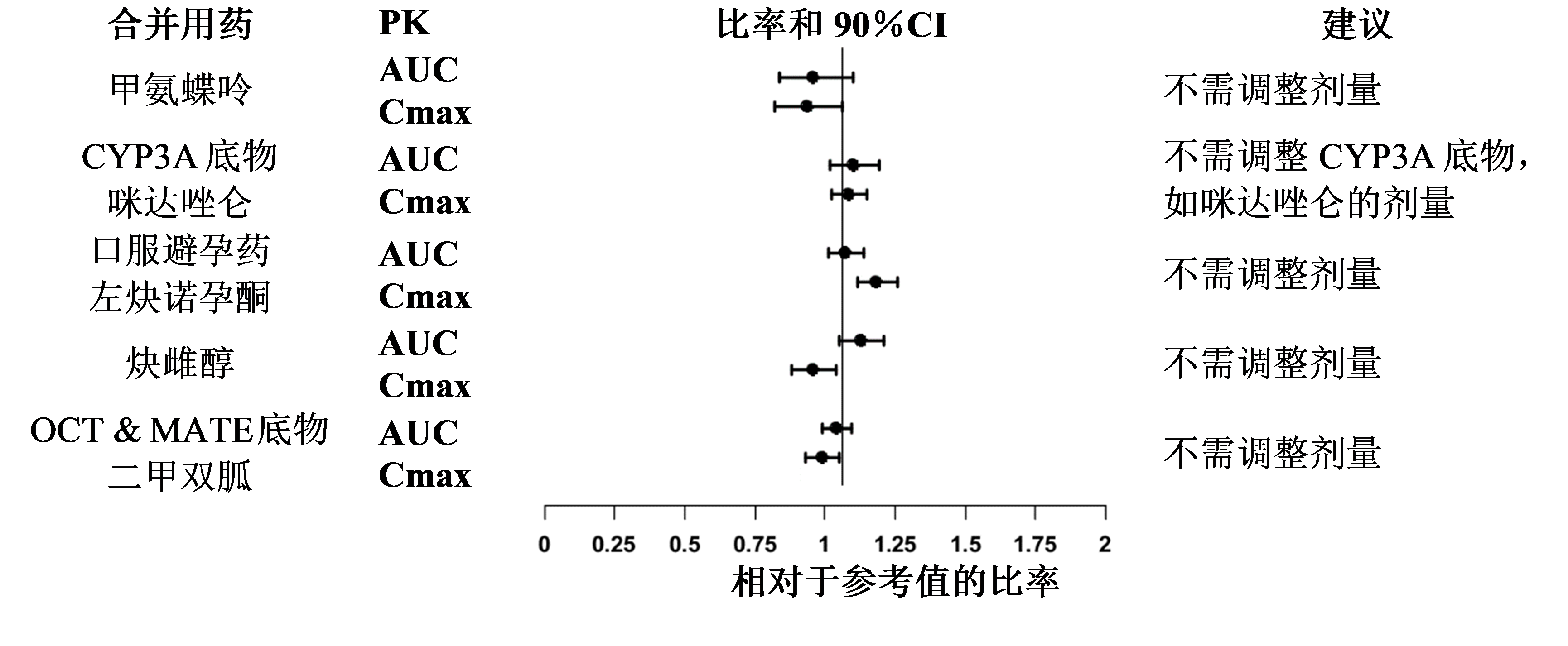
注:参考组是单独合并用药给药;OCT=有机阳离子转运体;
MATE=多药和有毒化合物排泄
其他药物影响托法替布药代动力学的可能性
由于托法替布由CYP3A4代谢,故而可能与抑制或诱导CYP3A4的药物发生相互作用。单独CYP2C19抑制剂或P-糖蛋白抑制剂不太可能大幅改变托法替布的药代动力学(见图3)。
图3.其他药物对托法替布药代动力学的影响
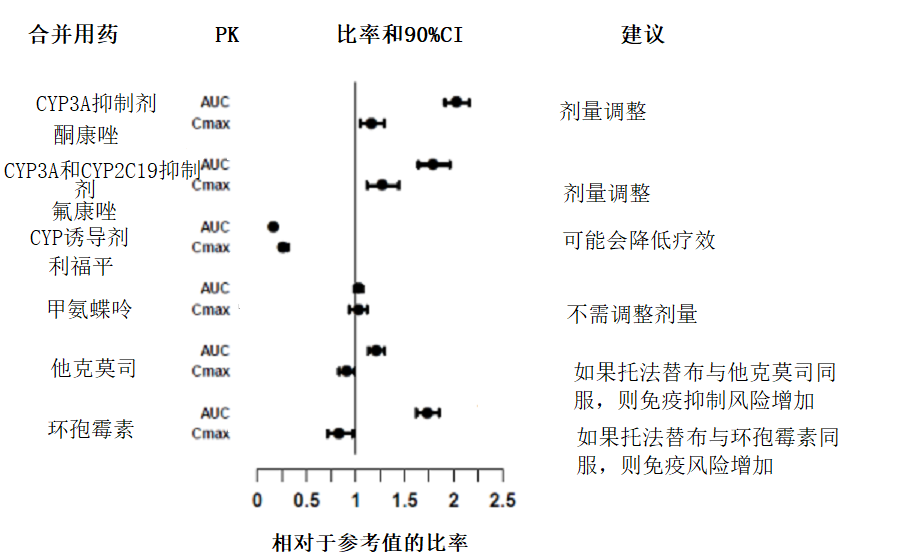
注:参考组是托法替布单独用药
a (见【用法用量】,【药物相互作用】)。
类风湿关节炎
托法替布临床开发项目包括四项验证性试验。虽然已对其他剂量进行了研究,但托法替布的推荐剂量为5 mg,每天两次。托法替布10 mg每天两次不应用于类风湿关节炎。
验证性试验
研究RA-I是一项为期12个月的试验,其中792例非生物制剂DMARD疗效不足的中度至重度活动性类风湿关节炎患者在背景DMARD治疗(不包括强效免疫抑制治疗,如硫唑嘌呤或环孢菌素)的基础上联合托法替布 5或10 mg每天两次给药,或安慰剂给药。在第3个月的访视中,所有无应答反应的患者都以盲法方式进入到第二阶段的预定治疗,即托法替布 5或10 mg,每天两次。在第6个月结束时,所有安慰剂组的患者都以盲法方式进入到第二阶段的预定治疗。主要终点是在第6个月达到ACR20疗效反应、第3个月时HAQ-DI变化以及第6个月DAS28-4(ESR)比率小于2.6的患者比例。
研究RA-II是一项在717例MTX治疗效应不足的中度至重度活动性类风湿关节炎患者中进行的为期12个月的试验。患者在背景MTX治疗的基础上联合托法替布 5或10 mg给药,每天两次,阿达木单抗40 mg皮下注射,每隔一周一次,或安慰剂。安慰剂组患者按研究I的方式进行。主要终点是第6个月时达到ACR20疗效反应、第3个月时HAQ-DI,第6个月时DAS28-4(ESR)低于2.6的患者比例。
研究RA-III是一项为期2年,在第1年进行了一次计划性分析,其中797例MTX疗效不足的中度至重度活动性类风湿关节炎患者在背景MTX治疗的基础上加用托法替布 5或10 mg,每天两次,或安慰剂给药。安慰剂组患者按研究I的方式推进。主要终点是第6个月达到ACR20疗效反应、第6个月van der Heijde改良的总Sharp评分(mTSS)与基线平均差、第3个月的HAQ-DI以及第6个月DAS28-4(ESR)低于2.6的患者比例。
研究RA-IV是一项为期6个月的试验,其中399例对至少一种批准上市的TNF-阻断性生物制剂反应不足的中度至重度活动性类风湿关节炎患者在背景MTX治疗的基础上联合托法替布 5或10 mg,每天两次,或安慰剂给药。在第3个月的访视中,所有随机接受安慰剂治疗的患者都以盲法方式进入到第二阶段的预定治疗,即托法替布 5或10 mg,每天两次。主要终点是第3个月达到ACR20疗效反应、HAQ-DI以及DAS28-4(ESR)低于2.6的患者比例。
临床应答率
研究RA-III和RA-IV中实现ACR20、ACR50、ACR70应答的托法替布治疗组患者百分比如表5所示。研究RA-I和RA-II的结果相似。在RA-I至IV试验中,患者使用托法替布 5mg每天两次治疗,在联用/不联用背景DMARD治疗的情况下,第3个月和第6个月时,与安慰剂相比,具有更高的ACR20、ACR50、ACR70应答率。在2周内即观察到了高于安慰剂组的ACR20反应率。在为期12个月的试验中,在6个月和12个月时,托法替布治疗组患者的ACR反应率一致。
表5:出现ACR疗效反应的患者比例
| 患者百分比 | ||||
|---|---|---|---|---|
| MTX反应不足者c | TNF阻断剂反应不足者d | |||
| 研究III | 研究IV | |||
Na
| 安慰剂+甲氨蝶呤 160 | 托法替布 5 mg,每天两次+MTX 321 | 安慰剂+甲氨蝶呤 132 | 托法替布 5 mg,每天两次+MTX 133 |
ACR20 第3个月 第6个月 |
27% 25% |
55% 50% |
24% NAb |
41% 51% |
ACR50 第3个月 第6个月 |
8% 9% |
29% 32% |
8% NA |
26% 37% |
ACR70 第3个月 第6个月 |
3% 1% |
11% 14% |
2% NA |
14% 16% |
a N是随机分组接受治疗的患者人数。
b NA:不适用,研究IV中因为安慰剂组的推进,导致没有3个月之后的安慰剂治疗的数据。
c MTX反应不足,定义为存在的剩余疾病活动性足以满足入选标准。
d 至少一种肿瘤坏死因子阻断剂因为缺乏有效性和/或不能耐受而反应不足。
在研究RA-III中,第6个月时,与单独MTX治疗相比,使用托法替布 5 mg每天两次加MTX治疗的患者实现疾病缓解的比例更大,指标为DAS28-4(ESR)小于2.6(表6)。
表6:DAS28-4(ESR)小于2.6的患者比例和剩余活动性关节数
| 研究III | ||
|---|---|---|
DAS28-4(ESR)小于2.6
| 安慰剂+MTX 160 | 托法替布 5 mg每天两次+MTX 321 |
| 第6个月的缓解者比例(n) | 1%(2) | 6%(19) |
| 缓解者,0个活动性关节的比例(n) | 50%(1) | 42%(8) |
| 缓解者,1个活动性关节的比例(n) | 0 | 5%(1) |
| 缓解者,2个活动性关节的比例(n) | 0 | 32%(6) |
| 缓解者,3个活动性关节的比例(n) | 50%(1) | 21%(4) |
研究RA-III的ACR反应标准组成要素的结果如表7所示。在研究RA-I、II和IV中观察到的托法替布结果类似。
表7:第3个月时的ACR反应组成要素
| 研究III | ||||
|---|---|---|---|---|
| 托法替布 5 mg 每天两次+MTX N=321 | 安慰剂+MTX N=160 | ||
| 组成要素(平均值)a | 基线 | 第3个月a | 基线 | 第3个月a |
| 压痛关节数(0-68) | 24 (14) | 13 (14) | 23 (13) | 18 (14) |
| 肿胀关节数(0-66) | 14 (8) | 6 (8) | 14 (9) | 10 (9) |
| 疼痛b | 58 (23) | 34 (23) | 55 (24) | 47 (24) |
| 患者总体评估b | 58 (24) | 35 (23) | 54 (23) | 47 (24) |
| 残疾指数(HAQ-DI)c | 1.41 (0.68) | 0.99 (0.65) | 1.32 (0.67) | 1.19 (0.68) |
| 医生总体评估b | 59 (16) | 30 (19) | 56 (18) | 43 (22) |
| CRP(mg/L) | 15.3 (19.0) | 7.1 (19.1) | 13.7 (14.9) | 14.6 (18.7) |
a所示数据为第3个月时的平均值(标准差)。
b视觉模拟评分:0=最好,100=最差。
c健康评估问卷残疾指数:0=最好,3=最差;20个问题;类别:穿衣和梳洗,起立,吃饭,走路,卫生,达到,抓握和活动。
按访视次数给出的研究RA-III中的ACR20反应的百分比如图4所示。在研究RA-I、II和IV中观察到的托法替布反应情况类似。
图4:按访视次数给出的研究RA-III中的ACR20反应的百分比
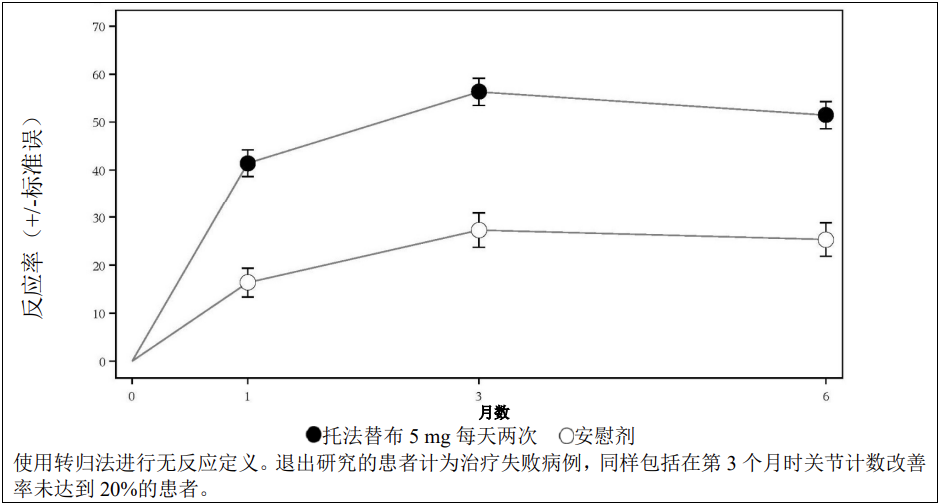
月数
放射影像反应
两项研究评估了托法替布对关节结构性损伤的作用。在研究RA-III中,关节结构性损伤的进展采用放射影像评估,并以第6和12个月时mTSS及其组成部分(即侵蚀评分和关节间隙狭窄评分)相对于基线的变化表示。研究还对无放射影像进展(mTSS变化小于或等于0)的患者比例进行了评估。
在研究RA-III中,托法替布5 mg每天两次的剂量给药时,减轻了结构性损伤平均进展方面(没有统计学意义)。这些结果见表8。侵蚀评分和关节间隙狭窄评分分析结果与总体结果一致。
在安慰剂加MTX组中,74%的患者在第6个月时无放射影像进展,与之相比,托法替布 5 mg每天两次加MTX组中有84%的患者放射影像无进展。
表8:第6和12个月时的放射影像变化
| 研究III | |||
|---|---|---|---|
| 安慰剂 N=139 平均值(SD)a | 托法替布 5 mg,每天两次 N=277 平均值(SD)a | 托法替布5 mg,每天两次 与安慰剂的平均差b(CI) | |
mTSSc 基线 第6个月 |
33 (42) 0.5 (2.0) |
31 (48) 0.1 (1.7) |
- -0.3 (-0.7, 0.0) |
aSD = 标准差
b托法替布减安慰剂或 MTX 最小二乘均数差值(95% CI = 95%置信区间)
c 第 6 和 12 个月的数据为相对于基线的平均变化。
身体功能缓解
通过HAQ-DI衡量的身体功能改善情况。接受5mg每天两次托法替布的患者证明第3个月时,与安慰剂相比,身体功能自基线的改善程度较大。
研究RA-II中,第3个月时HAQ-DI自基线的改善与安慰剂组的平均差异(95% CI),在每天两次5 mg 托法替布治疗组患者中为-0.22(-0.35,-0.10)。研究RA-I、III和IV中得到的结果相似。在12个月的试验中,第6和12个月时,托法替布治疗组患者中的HAQ-DI结果一致。
其他健康相关结果
总体健康状况采用健康调查简表(SF-36)进行评估。在研究RA-III和RA-IV中,与安慰剂组相比,接受托法替布 5 mg每天两次的患者在第3个月时的躯体健康总评(PCS)、精神健康总评(MCS)以及SF-36的所有8个领域相对于基线均表现出较大的改善。
银屑病关节炎
评估托法替布疗效和安全性的临床开发项目包括在816例18岁及以上患者中进行的2项多中心、随机、双盲、安慰剂对照验证性试验(PsA-I和PsA-II)。尽管也研究了其他剂量,但托法替布的推荐剂量为5 mg每天两次。托法替布10 mg每天两次不应用于银屑病关节炎的治疗。所有患者均有至少6个月的活动性银屑病关节炎病史(基于银屑病关节炎的分类标准[CASPAR])、至少3处压痛/疼痛关节和至少3处肿胀关节及活动性斑块型银屑病。2项临床试验中接受随机化和治疗的患者在筛选时表现出不同的银屑病关节炎亚型,包括<5处关节或不对称性受累(21%)、≥5处关节累计(90%)、远端指间(DIP)关节受累(61%)、残毁性关节炎(8%)和脊椎炎(19%)。这些临床试验中的患者有平均(SD)7.7(7.2)年的银屑病关节炎诊断。80%和53%的患者分别有基线肌腱附着点炎和指(趾)炎。所有患者均需在基线时接受稳定剂量的非生物DMARD治疗(79%接受甲氨蝶呤,13%接受柳氮磺胺吡啶,7%接受来氟米特,1%接受其他非生物DMARD)。两项临床试验的主要终点均为第3个月时的ACR20反应和HAQ-DI较基线的变化。
研究PsA-I是一项为期12个月的临床试验,其中入组了422例对非生物DMARD反应不足(67%和33%的患者分别对1种非生物DMARD和2种及以上非生物DMARD反应不足)和未接受过TNF阻滞剂治疗的患者。以2:2:2:1:1的比例使患者分别随机分配接受托法替布5 mg每天两次、托法替布10 mg每天两次、阿达木单抗40 mg皮下给药每两周一次、安慰剂至托法替布5 mg每天两次治疗序列或安慰剂至托法替布10 mg每天两次治疗序列;将研究药物添加至非生物DMARD背景治疗中。第3个月访视时,随机分配至安慰剂组的所有患者均以盲态进入预先确定的托法替布5 mg或10 mg每天两次治疗。研究PsA-I并未设计用于证实托法替布相比于阿达木单抗的非劣效性或优效性。
研究PsA-II是一项为期6个月的临床试验,其中入组了394例对至少1种获批TNF阻滞剂反应不足的患者(66%、19%和15%的患者分别对1种、2种和3种及以上TNF阻滞剂反应不足)。以2:2:1:1的比例使患者分别随机分配接受托法替布5 mg每天两次、托法替布10 mg每天两次、安慰剂至托法替布5 mg每天两次治疗序列或安慰剂至托法替布10 mg每天两次治疗序列;将研究药物添加至背景非生物DMARD治疗中。第3个月访视时,安慰剂组患者均以盲态进入预先确定的托法替布5 mg或10 mg每天两次治疗(与研究PsA-I一致)。
临床应答率
第3个月时,与安慰剂相比,研究PsA-I中接受托法替布5 mg每天两次治疗的患者具有更高的ACR20、ACR50、ACR70应答率(p≤0.05),研究PsA-II 中接受托法替布5 mg每天两次治疗的患者具有更高的ACR20和ACR50应答率(p≤0.05);研究PsA-II中,托法替布5 mg每天两次组的ACR70应答率也高于安慰剂组,但与安慰剂相比的差异没有统计学意义(p>0.05)(表9 和表 10)。
表9:研究PsA-I中达到ACR疗效反应的患者比例*[非生物DMARD反应不足者(未接受过TNF阻滞剂治疗)]
| 治疗组 | 安慰剂 | 托法替布 5 mg 每天两次 | |
|---|---|---|---|
| Na | 105 | 107 | |
| 应答率 | 应答率 | 相比安慰剂的差异(%) 及95% CI | |
| 第3个月 ACR20 ACR50 ACR70 | 33% 10% 5% | 50% 28% 17% | 17.1 (4.1, 30.2) 18.5 (8.3, 28.7) 12.1 (3.9, 20.2) |
将数据缺失的受试者处理为无应答者。
* 受试者接受1种合并非生物DMARD。
a N为随机分组且接受治疗的患者人数。
表10:研究PsA-II中达到ACR应答的患者比例*(TNF阻滞剂反应不足者)
| 治疗组 | 安慰剂 | 托法替布 5 mg 每天两次 | |
|---|---|---|---|
| Na | 131 | 131 | |
| 应答率 | 应答率 | 相比安慰剂的差异(%) 及95% CI | |
| 第3个月 ACR20 ACR50 ACR70 | 24% 15% 10% | 50% 30% 17% | 26.0 (14.7, 37.2) 15.3 (5.4, 25.2) 6.9 (-1.3, 15.1) |
将数据缺失的受试者处理为无应答者。
* 受试者接受1种合并非生物DMARD。
a N为随机分组且接受治疗的患者人数。
两项研究中ACR反应标准组成要素较基线的改善见表 11。
表11:研究PsA-I和PsA-II中基线和第3个月时的ACR应答组成要素
| 非生物DMARD反应不足者(未接受过TNF阻滞剂治疗) | TNF阻滞剂反应不足者 | |||
|---|---|---|---|---|
| 研究PsA-I* | 研究PsA-II* | |||
| 治疗组 | 安慰剂 | 托法替布 5 mg 每天两次 | 安慰剂 | 托法替布 5 mg 每天两次 |
| 基线时的N | 105 | 107 | 131 | 131 |
| ACR组成要素a 压痛/疼痛关节数量(0-68) 基线 第3个月 | 20.6 14.6 | 20.5 12.2 | 19.8 15.1 | 20.5 11.5 |
| 肿胀关节数量(0-66) 基线 第3个月 | 11.5 7.1 | 12.9 6.3 | 10.5 7.7 | 12.1 4.8 |
| 关节炎疼痛的患者评估b 基线 第3个月 | 53.2 44.7 | 55.7 34.7 | 54.9 48.0 | 56.4 36.1 |
| 关节炎的患者总体评估b 基线 第3个月 | 53.9 44.4 | 54.7 35.5 | 55.8 49.2 | 57.4 36.9 |
| HAQ-DIc 基线 第3个月 | 1.11 0.95 | 1.16 0.81 | 1.25 1.09 | 1.26 0.88 |
| 关节炎的医生总体评估b 基线 第3个月 | 53.8 35.4 | 54.6 29.5 | 53.7 36.4 | 53.5 27.0 |
| CRP(mg/L) 基线 第3个月 | 10.4 8.6 | 10.5 4.0 | 12.1 11.4 | 13.8 7.7 |
*受试者接受1种合并非生物DMARD。
a所示数据为基线和第3个月时的平均值。
b 视觉模拟评分(VAS):0=最好,100=最差。
c HAQ-DI=健康评估问卷残疾指数:0=最好,3=最差;20个问题;类别:穿衣和梳洗,起立,吃饭,走路,卫生,伸手,抓握和活动。
按访视给出的研究PsA-I中的ACR20应答者百分比如图5所示。在研究PsA-II中观察到相似的反应。两项研究均在基线后首次访视时(第2周)观察到托法替布对ACR20反应的改善。
图5:按访视次数给出的研究RA-III中的ACR20反应的百分比*
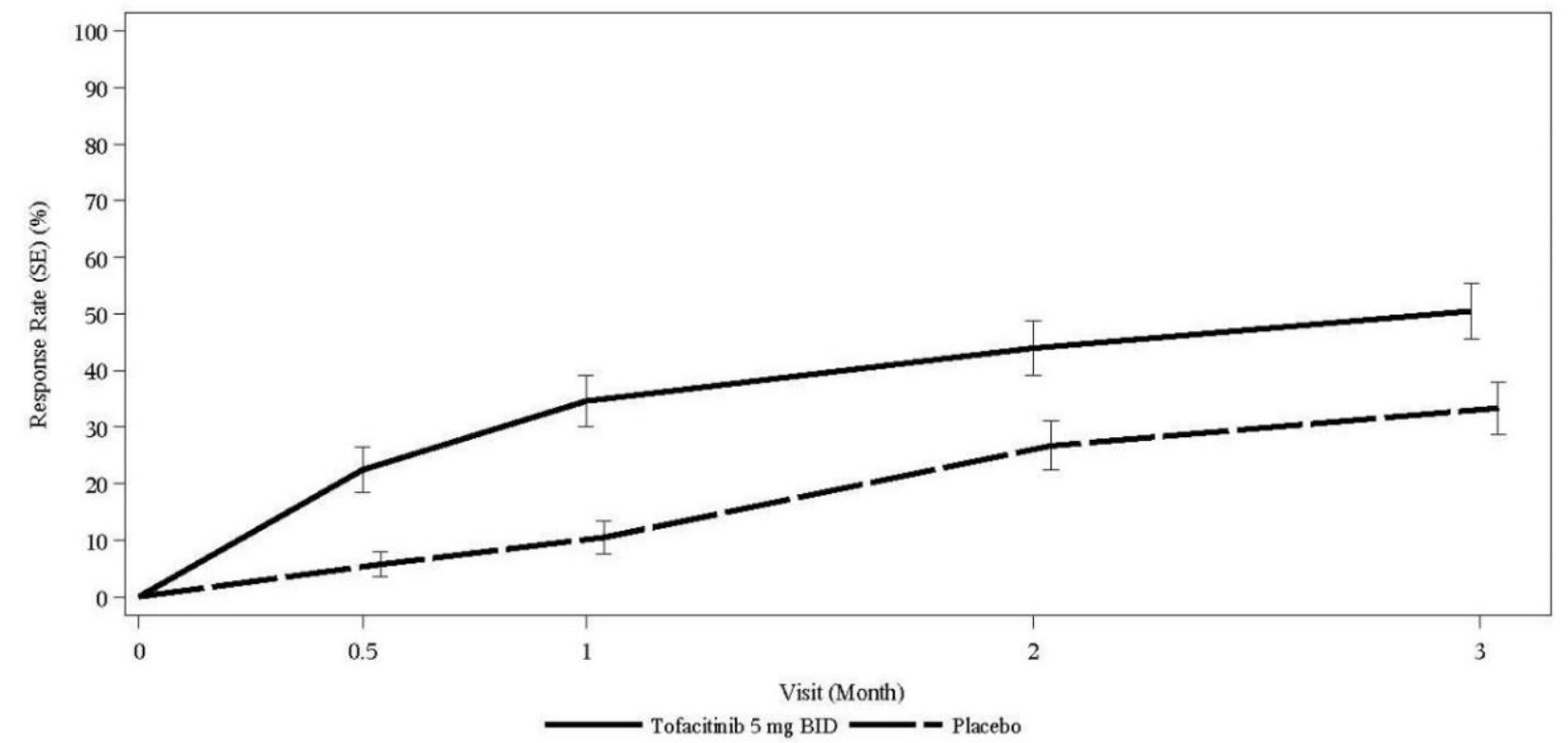
BID=每天两次;SE=标准误。
将数据缺失的受试者处理为无应答者。
* 受试者接受1种合并非生物DMARD。
活动性银屑病关节炎患者接受托法替布治疗后观察到肌腱附着点炎和指(趾)炎的获益证据。
身体功能
通过HAQ-DI衡量身体功能改善情况。接受5 mg每天两次托法替布的患者证明第3个月时,与安慰剂相比,身体功能较基线的改善程度明显较大(p≤0.05)(表12)。
表12:研究PsA-I和PsA-II中HAQ-DI较基线的变化
| 第3个月时HAQ-DI较基线变化的最小二乘均值 | ||||
|---|---|---|---|---|
| 非生物DMARD反应不足者b (未接受过TNF阻滞剂治疗) | TNF阻滞剂反应不足者c | |||
| 研究PsA-I* | 研究PsA-II* | |||
| 治疗组 | 安慰剂 | 托法替布 5 mg 每天两次 | 安慰剂 | 托法替布 5 mg 每天两次 |
| Na | 104 | 107 | 131 | 129 |
| LSM较基线的变化 | -0.18 | -0.35 | -0.14 | -0.39 |
| 与安慰剂相比的差异(95% CI) | - | -0.17 (-0.29, -0.05) | - | -0.25 (-0.38, -0.13) |
*受试者接受1种合并非生物DMARD。
a N为统计分析中的受试者总人数。
b因缺乏疗效和/或不能耐受而对至少1种非生物DMARD反应不足。
c因缺乏疗效和/或不能耐受而对至少1种TNF阻滞剂反应不足。
在研究PsA-I中,第3个月时托法替布5 mg每天两次和安慰剂组的HAQ-DI应答率(应答定义为较基线的改善≥0.35)分别为53%和31%。在研究PsA-II中观察到相似的应答率。
其他健康相关结果
总体健康状况采用健康调查简表(SF-36)进行评估。在研究PsA-I和PsA-II中,与安慰剂组相比,接受托法替布5 mg每天两次的患者第3个月时的身体健康总评(PCS)较基线出现较大的改善,但该结果未见于心理健康总评(MCS)中。接受托法替布5 mg每天两次的患者在身体功能、身体疼痛、精力和社会功能维度报告的改善均大于安慰剂组,但在体格健康状况导致的角色局限性、一般健康感知、情绪问题导致的角色局限性或心理健康方面未见一致结果。
放射影像反应
尚未根据PsA-I的研究结果确定药物在银屑病关节炎中对放射影像进展抑制的治疗作用。
强直性脊柱炎
进行疗效和安全性评估的托法替布临床开发项目包括一项安慰剂对照确证性试验(研究AS-I)和一项剂量范围试验(研究AS-II)。患者存在活动性疾病定义为即使接受了非甾体抗炎药(NSAID)、皮质类固醇或改善病情的抗风湿药(DMARD)治疗,但Bath强直性脊柱炎疾病活动度指数(BASDAI)和背痛评分(BASDAI问题2)依然≥4分。
确证性试验(研究AS-I)
研究AS-I是一项在269例至少对2种NSAID疗效不足(临床疗效不足或不耐受)的成人患者中开展的随机、双盲、安慰剂对照、为期48周的临床试验。对患者进行随机分组,盲态接受16周的托法替布5 mg每天两次或安慰剂治疗,然后均额外接受32周的托法替布5 mg每天两次治疗。主要终点是评估第16周达到ASAS20应答的患者比例。
从基线至第16周,分别约有7%和21%的患者合并使用甲氨蝶呤或柳氮磺吡啶。22%的患者对1种或2种TNF阻滞剂疗效不足。
临床应答
第16周时,与安慰剂相比,接受托法替布5 mg每天两次治疗的患者在ASAS20、ASAS40和ASAS 5/6应答方面获得了较大改善(表13)。
表13:第16周的ASAS20、ASAS40和ASAS 5/6应答,研究AS-I
安慰剂 (N=136) | 托法替布5 mg每天两次 (N=133) | 与安慰剂的差异 (95% CI) | |
|---|---|---|---|
| ASAS20 应答率*,% | 29 | 56 | 27 (16, 38)** |
| ASAS40 应答率*,% | 13 | 41 | 28 (18, 38)** |
| ASAS 5/6 应答率,% | 7 | 44 | 36 (27, 46)** |
* 控制 I 类错误。
** p 值< 0.0001。
如表14所示,与安慰剂相比,托法替布5 mg每天两次治疗组,ASAS应答分项和其他疾病活动度指标改善较大。
表14:第16周时的ASAS分项和其他疾病活动度指标,研究AS-I
| 安慰剂 (N=136) | 托法替布5 mg 每天两次(N=133) | ||||
|---|---|---|---|---|---|
| 基线 (平均值) | 第16周 (较基线的 LSM 变化) | 基线 (平均值) | 第16周 (较基线的 LSM 变化) | 与安慰剂的差异 (95% CI) | |
| ASAS分项 | |||||
| -患者的疾病活动度总评分(0-10)a,* | 7.0 | -0.9 | 6.9 | -2.5 | -1.6 (-2.07, -1.05)** |
| -脊柱疼痛总评分(0-10)a,* | 6.9 | -1.0 | 6.9 | -2.6 | -1.6 (-2.10, -1.14)** |
| -BASFI(0-10)b,* | 5.9 | -0.8 | 5.8 | -2.0 | -1.2 ( -1.66, -0.80)** |
| -炎症(0-10)c,* | 6.8 | -1.0 | 6.6 | -2.7 | -1.7 ( -2.18, -1.25)*** |
| BASDAI评分d,* | 6.5 | -1.1 | 6.4 | -2.6 | -1.4 ( -1.88, -1.00)** |
| BASMIe,* | 4.4 | -0.1 | 4.5 | -0.6 | -0.5 ( -0.67, -0.37)** |
| hsCRPf,*(mg/dL) | 1.8 | -0.1 | 1.6 | -1.1 | -1.0 ( -1.20, -0.72)** |
| ASDAScrpg,* | 3.9 | -0.4 | 3.8 | -1.5 | -1.1 ( -1.28, -0.89)** |
* 控制 I 类错误。
** p< 0.0001。
a 在数值型评定量表上进行测评,0 =无活动性或无疼痛,10 =活动性非常强或疼痛最严重。
b Bath 强直性脊柱炎功能指数采用数值型评定量表进行测量,0 =容易,10 =不可能。
c 炎症是 BASDAI 中 2 项患者报告的强直自我评估平均值。
d Bath 强直性脊柱炎疾病活动度指数总分。
e Bath 强直性脊柱炎计量指数。
f 超敏 C 反应蛋白。
g 强直性脊柱炎疾病活动度评分与 C 反应蛋白。
LSM =最小二乘均值
在第2周首次观察到了ASAS20的应答改善。按访视列出的获得ASAS20应答的患者百分比见图6。
图6:直至第16周ASAS20应答随时间的变化,研究AS-I
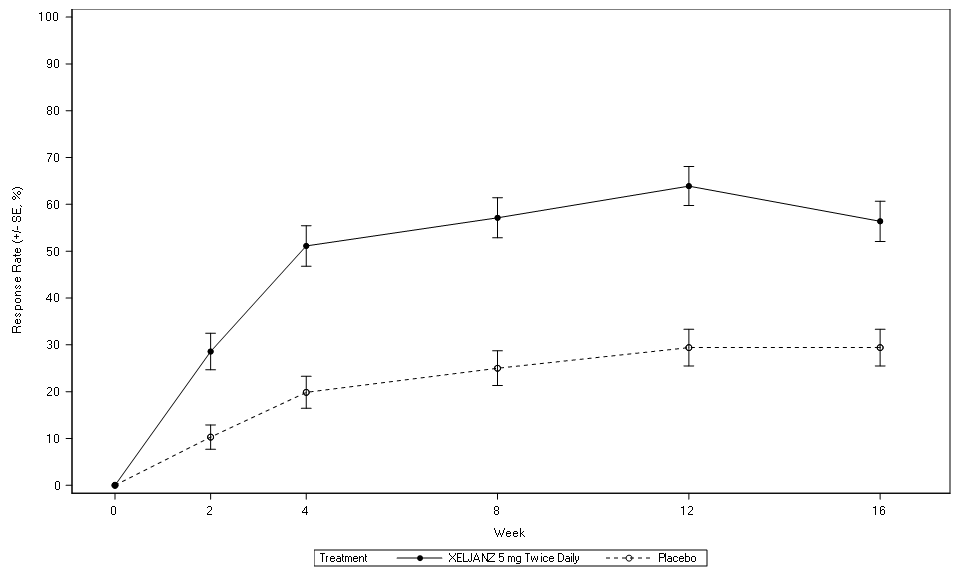
SE=标准误。
将缺失数据的患者视为非应答者。
其他健康相关结果
在第16周时,与接受安慰剂治疗的患者相比,接受托法替布5 mg每天两次治疗的患者的强直性脊柱炎生活质量(ASQoL)(安慰剂组为-2.0,托法替布组为-4.0)和慢性疾病治疗的功能评估-疲乏(FACIT-F)(分别为3.1和6.5)较基线获得了较大的改善。与接受安慰剂治疗的患者相比,接受托法替布5 mg每天两次治疗的患者在健康调查简表(SF-36)、身体健康总评(PCS)、身体功能、身体角色、身体疼痛、总体健康和社会功能维度较基线改善持续较大,但第 16 周时心理健康总评(MCS)、活力、情感职能和心理健康维度除外。
安全性研究
在 50 岁及以上的具有至少一项心血管风险因素的类风湿关节炎患者中开展了一项随机开放性试验(RA 安全性研究 1),以评价两个托法替布剂量组(5 mg 每天两次[N=1455]和 10 mg 每天两次[N=1456])相比 TNF 阻滞剂对照组(N=1451)的安全性。协同主要终点为裁定 MACE(定义为心源性死亡、非致命性 MI 和非致命性卒中)和裁定恶性肿瘤(不包括非黑色素瘤皮肤癌);根据研究设计,对于各协同主要终点中托法替布合并剂量组与TNF 阻滞剂对照组的风险比,排除了预定的风险界值 1.8。独立委员会根据预先定义的标准(裁定)对协同主要终点进行了设盲评价。研究采用事件驱动设计,期间持续随访患者,直到主要结果事件累积到足够数量。其他终点包括死亡率、严重感染和血栓栓塞事件。研究随访期的中位数为 4.0 年。
研究人群的平均年龄为 61 岁(范围:50 至 88 岁)。大多数患者为女性(78%)和白种人(77%)。患者确诊类风湿关节炎的平均时长为 10 年,肿胀和触痛关节计数的中位数分别为 11 和 15。心血管风险因素包括吸烟史(当前或既往)(48%)、高血压(66%)、高密度脂蛋白< 40 mg/dL (12%)、糖尿病(17%)、早发冠心病家族史(15%)、存在与类风湿关节炎相关的关节外疾病(37%)以及冠状动脉疾病史(11%)。
根据托法替布合并剂量与 TNF 阻滞剂的主要比较结果,研究未达到非劣效性标准,因为 95% CI 上限超出了预定的非劣效性标准 1.8(对于 MACE,95% CI 上限为 1.94;对于除 NMSC 之外的恶性肿瘤,95% CI 上限为 2.09)。
表 15 列出了各协同主要终点和其他终点的研究结果。在托法替布的两个剂量组中,死亡、MACE、恶性肿瘤、严重感染和血栓栓塞事件风险均有所升高。
表 15: RA 安全性研究 1 的结果
| 终点 | 托法替布 5 mg 每天两次 N=1455 PY=5490 | 托法替布 10 mg 每天两次 N=1456 PY=5298 | TNF阻滞剂 N=1451 PY=5468 |
|---|---|---|---|
| MACE, n [IR] HR (95% CI)* | 50 [0.91] 1.16 (0.77, 1.74) | 59 [1.11] 1.41 (0.95, 2.10) | 43 [0.79] |
| MI†,n [IR] HR (95% CI)* | 20 [0.36] 1.81 (0.87, 3.79) | 21 [0.39] 1.97 (0.95, 4.09) | 11 [0.20] |
| 卒中†,n [IR] HR (95% CI)* | 18 [0.33] 0.89 (0.47, 1.69) | 21 [0.39] 1.08 (0.59, 2.00) | 20 [0.36] |
| 心源性死亡,n [IR] HR (95% CI)* | 18 [0.32] 1.20 (0.60, 2.37) | 25 [0.47] 1.71 (0.90, 3.24) | 15 [0.27] |
| 恶性肿瘤(不包括NMSC),n [IR] HR (95% CI)* | 62 [1.13] 1.47 (1.00, 2.18) | 60 [1.13] 1.48 (1.00, 2.19) | 42 [0.77] |
| 恶性肿瘤(不包括 NMSC) (吸烟患者或既往有吸烟经历的患者中)†† | 41 [1.53] | 48 [1.91] | 25 [0.99] |
| HR (95% CI)* | 1.55 (0.94, 2.55) | 1.94 (1.19, 3.14) | |
| 所有死亡事件 HR (95% CI)* | 49 [0.88] 1.29 (0.84, 1.96) | 66 [1.23] 1.79 (1.20, 2.66) | 38 [0.69] |
| 严重感染 HR (95% CI)* | 155 [2.95] 1.17 (0.93, 1.47) | 184 [3.65] 1.44 (1.15, 1.80) | 133 [2.52] |
| DVT HR (95% CI)* | 12 [0.22] 1.33 (0.56, 3.15) | 15 [0.28] 1.72 (0.75, 3.92) | 9 [0.16] |
| PE HR (95% CI)* | 10 [0.18] 3.32 (0.91, 12.08) | 26 [0.49] 8.95 (2.71, 29.56) | 3 [0.05] |
| VTE HR (95% CI)* | 18 [0.33] 1.50 (0.72, 3.10) | 36 [0.68] 3.10 (1.61, 5.96) | 12 [0.22] |
| ATE HR (95% CI)* | 51 [0.93] 1.13 (0.76, 1.69) | 55 [1.04] 1.26 (0.85, 1.87) | 45 [0.83] |
| TE HR (95% CI)* | 67 [1.23] 1.19 (0.84, 1.70) | 86 [1.65] 1.60 (1.14, 2.23) | 56 [1.03] |
注:数据监查委员会出于安全性问题的考虑终止了托法替布 10 mg 每天两次方案,正在接受治疗的患者已从托法替布 10 mg 换为托法替布 5 mg。“托法替布 10 mg 每天两次”列包括随机分配到托法替布 10 mg 每天两次剂量组的患者的所有事件和随访信息。托法替布缓释片22 mg每天一次不应用于类风湿关节炎、银屑病关节炎或强直性脊柱炎。
N 表示患者人数;n 表示发生事件的患者人数。
IR 表示每 100 人年(PY)的发生率。
†MI 和卒中包括致命性和非致命性事件。
††纳入了当前吸烟患者和既往有吸烟经历的患者的恶性肿瘤(不包括 NMSC)数据和分析。随机分配到托法替布 5 mg、托法替布 10 mg 和 TNF 阻滞剂组的当前吸烟患者和既往有吸烟经历 的患者分别为 720 例、704 例和 679 例。
*托法替布与 TNF 阻滞剂的 HR (95%) CI(单变量 Cox 比例风险模型)。
NMSC:非黑色素瘤皮肤癌;MACE:重大心脏不良事件;HR:风险比;DVT:深静脉血栓形成;PE:肺栓塞;VTE:静脉血栓栓塞,为首次发生 VTE,定义为裁定 DVT 和裁定 PE 的复合事件;ATE:动脉血栓栓塞;TE:血栓栓塞,为首次发生 TE,定义为裁定 VTE 和非裁定 ATE 的复合事件。
在托法替布 5 mg 每天两次和托法替布 10 mg 每天两次治疗组患者中,观察到淋巴瘤和肺癌(RA 安全性研究 1 中所有恶性肿瘤事件的子集)发生率高于 TNF 阻滞剂治疗组。在接受托法替布 5 mg 每天两次、托法替布 10 mg 每天两次和 TNF 阻滞剂的患者中,分别有 4 例、6 例和 1 例报告淋巴瘤(每 100 患者年的发生率[IR]分别为 0.07、0.11 和 0.02)。在接受托法替布 5 mg 每天两次、托法替布 10 mg 每天两次和 TNF 阻滞剂的吸烟患者或既往有吸烟经历患者中,分别有 13 例、15 例和 7 例患者报告肺癌(每 100 患者年的 IR 分别为 0.48、0.59 和 0.27)。
托法替布缓释片22 mg每天一次不应用于类风湿关节炎、银屑病关节炎或强直性脊柱炎。
药理作用
托法替布是一种Janus激酶(JAK)抑制剂。JAK属于胞内酶,可传导细胞膜上的细胞因子或生长因子-受体相互作用所产生的信号,从而影响细胞造血过程和细胞免疫功能。在该信号转导通路内,JAK磷酸化并激活信号转导因子和转录激活因子(STAT),从而调节包括基因表达在内的细胞内活动。托法替布在JAK这一点对该信号转导通路进行调节,防止STAT磷酸化和激活。JAK酶通过配对JAK(如,JAK1/JAK3,JAK1/JAK2,JAK1/TyK2,JAK2/JAK2)传递细胞因子信号。托法替布抑制JAK1/JAK2、JAK1/JAK3和JAK2/JAK2组合酶的体外活性,IC50分别为406、56和1377 nM。但特定JAK组合酶与治疗有效性的相关性尚未明确。
毒理研究
遗传毒性
在代谢酶的存在下,托法替布人淋巴细胞体外染色体畸变试验结果为阳性,在没有代谢酶存在时结果阴性。托法替布Ames试验、CHO-HGPRT试验、大鼠微核试验和大鼠肝细胞程序外DNA合成(UDS)试验结果均为阴性。
生殖毒性
大鼠给予托法替布约为推荐剂量5mg每天两次17倍的暴露水平,或约为10mg每天2次剂量的8.3倍(以经口给药10 mg/kg/天剂量的AUC计),可见着床后丢失率增加,生育力降低。托法替布在等于推荐剂量5mg每天两次,或约为10mg每天两次剂量的0.5倍暴露水平(以经口给药1 mg/kg/天剂量的AUC计),未见对雌性大鼠生育力明显影响。托法替布在约为推荐剂量5mg每天两次)的133倍暴露水平,或约为10mg每天两次剂量的67倍的暴露水平(以经口100 mg/kg/天剂量的AUC计),对雄性生育力、精子活力、精子浓度未见明显影响。
大鼠胚胎-胎仔发育毒性试验中,妊娠大鼠在胎仔器官形成期给予托法替布推荐剂量5mg每天两次的约146倍,或约为最大推荐剂量10mg每天两次的73倍(以大鼠经口给药100mg/kg/天AUC计)的药物暴露水平可见致畸作用。致畸作用包括外部畸形和软组织畸形,分别为全身水肿和室间隔膜部缺损,以及骨骼畸形或变异(颈椎弓缺失;股骨、腓骨、肱骨、桡骨、肩胛骨、胫骨和尺骨弯曲;胸骨裂;肋骨缺失;股骨畸形;分叉肋;融合肋骨;融合胸骨节;胸椎半椎体畸形)。此外,着床后丢失增加,包括早期和晚期再吸收,由此导致活胎数减少,平均胎仔体重下降。在推荐剂量5mg每天两次约58倍的暴露水平,或最大推荐剂量10mg每天两次约29倍的剂量(以妊娠大鼠经口给药30 mg/kg/天的AUC计)在大鼠中未见发育毒性。
兔胚胎-胎仔发育毒性试验中,妊娠兔在胎仔器官形成期给予托法替布约为推荐剂量5mg每天两次的13倍,或最大推荐剂量10mg每天两次约6.3倍(以兔经口给药30mg/kg/天的AUC计)的药物暴露水平具有致畸作用,未见母体毒性。致畸作用包括胸腹裂、脐膨出、室间隔膜部缺损、颅/骨骼畸形(小口,小眼球)、中线和尾部缺陷。此外,与晚期再吸收有关的着床后丢失增加。药物暴露水平约为推荐剂量5mg每天两次的3倍,或约为最大推荐剂量10mg每天两次的1.5倍(以妊娠兔经口给药10mg/kg/天的AUC计)时,未见发育毒性。
围产期毒性试验中,大鼠在妊娠期第6天至哺乳期第20天给予托法替布,在约为推荐剂量5mg每天两次的73倍暴露水平,或约为最大推荐剂量10mg每天两次的36倍(以大鼠经口给药剂量为50mg/kg/天的AUC计),窝仔数减少、出生后生存率降低以及幼仔体重下降。在约为推荐剂量5mg每天两次的17倍,或约为最大推荐剂量10mg每天两次的8.3倍(以大鼠经口给药剂量为10mg/kg /天的AUC计)的暴露水平,对F1代大鼠行为和学习、性成熟以及交配并产生活F2代胎仔能力未见明显影响。
致癌性
RasH2转基因小鼠6个月致癌性试验中,托法替布约为推荐剂量5mg每天两次的34倍或约为最大推荐剂量10mg每天2次的17倍(以经口给药200 mg/kg/天的剂量的AUC计)水平时,未见致癌性。
SD大鼠经口给药2年致癌性试验中,托法替布在大于或等于30 mg/kg/天的剂量下(暴露水平以推荐剂量5mg每天两次的AUC计约42倍,或以10mg每天两次的AUC计约21倍),可见良性睾丸间质细胞瘤、冬眠瘤(褐色脂肪组织恶性肿瘤)和良性胸腺瘤。良性睾丸间质细胞瘤与人体的相关性风险尚未明确。
猴39周重复给药毒性试验中,托法替布暴露水平约为推荐剂量5mg每天两次的6倍时,或约为剂量10mg每天两次的3倍(以经口给药5 mg/kg剂量每天两次的AUC计)可见淋巴瘤。托法替布暴露水平为推荐剂量5mg每天两次的1倍,或约为剂量10mg每天两次的0.5倍(以经口给药1 mg/kg每天两次的AUC计)未见淋巴瘤。
密封,不超过30°C保存。
高密度聚乙烯瓶装。
14片/瓶;30片/瓶;
36个月
进口药品注册标准JX20170327
国药准字HJ20210071
名 称:Pfizer Inc.
注册地址:66 Hudson Boulevard East, New York, NY 10001 United States of America
企业名称:Viatris Pharmaceuticals LLC
生产地址:Road #2 Km 58.2, Barceloneta, PUERTO RICO 00617
名 称:Viatris Pharmaceuticals LLC
包装厂地址:Road 689 KM 1.9 Vega Baja, Puerto Rico 00693
名 称:辉瑞投资有限公司
地 址:上海市南京西路1168号中信泰富广场36层
联系方式:400 910 0055
2021年09月07日
2022年04月28日;2022年10月18日;2023年02月07日;2023年07月04日;2024年01月09日;2024年11月14日;2025年07月01日