
引分子标志物与ccRCC预后分层
在前篇的概述中我们提到,在过去十年里,转移性肾细胞癌(mRCC)的治疗发生了巨大的变革。(点此查看肾癌基因检测和个体化精准治疗(一))
现有的治疗选择已经不断丰富,分子病理学方面发现了大量的肿瘤异质性信息,这些不同的基因突变与患者预后密切相关,于是药物研发也围绕这些生物标记物开展了大量工作。
本篇重点关注分子标志物与肾癌预后分层的关系。
引言
肾癌是来源于肾小管上皮细胞的一种实体肿瘤,其中约70%肾细胞癌为透明细胞肾癌(ccRCC)。90%以上的ccRCC病例中都会发现染色体3p25处von Hippel Lindau肿瘤抑制基因(VHL)的突变。染色体3p的缺失导致VHL突变,并且容易发生第3号染色体上其他基因的继发突变事件,包括染色质修饰的肿瘤抑制基因PBRM1和BAP1。PBRM1是仅次于VHL的第二大突变基因,在该基因中获得的突变与BAP1的功能丧失事件基本上没有重叠,两个基因的改变影响了50%以上的透明细胞肾癌患者。越来越多的数据分析表明BAP1和PBRM1的突变状态是ccRCC癌症特异性预后的预测因素。同样,回顾性研究表明,在其他一些反复突变的基因中获得性突变,如SETD2、KDM5C、TP53和TERT,可能对使用标准药物的转移性疾病患者的预后有影响。由于多种原因,VHL基因表达状态没有被证明是一个有用的预后标记,包括VHL基因突变导致其功能几乎完全丧失,高频率的突变或表观遗传沉默限制了它在基因组分类中的应用[1]。
TP53/BAP1/PBRM1与ccRCC预后分层
2018年柳叶刀上(LANCET ONCOLOGY)的一篇回顾性研究,对晚期肾细胞癌的预后分层相关基因进行了分析,并优化了MSKCC预后风险评估模型。数据来源于COMPARZ和RECORD-3两项晚期肾细胞癌的临床试验。
研究者们首先分析了COMPARZ中357名mRCC患者的基因突变图谱与总生存期OS的关系,发现TP53或BAP1基因发生突变的ccRCC患者总生存期更短,预后较差;而PBRM1基因发生突变,总生存期更长,提示预后较好(图1)。接着,根据突变状态和临床结果的分析,研究者们优化了MSKCC模型,将TP53、BAP1、PBRM1作为独立预后指标加入预后评估的模型中,并在另一项258名mRCC患者的RECORD-3 临床试验中得到了验证(图2)[1]。
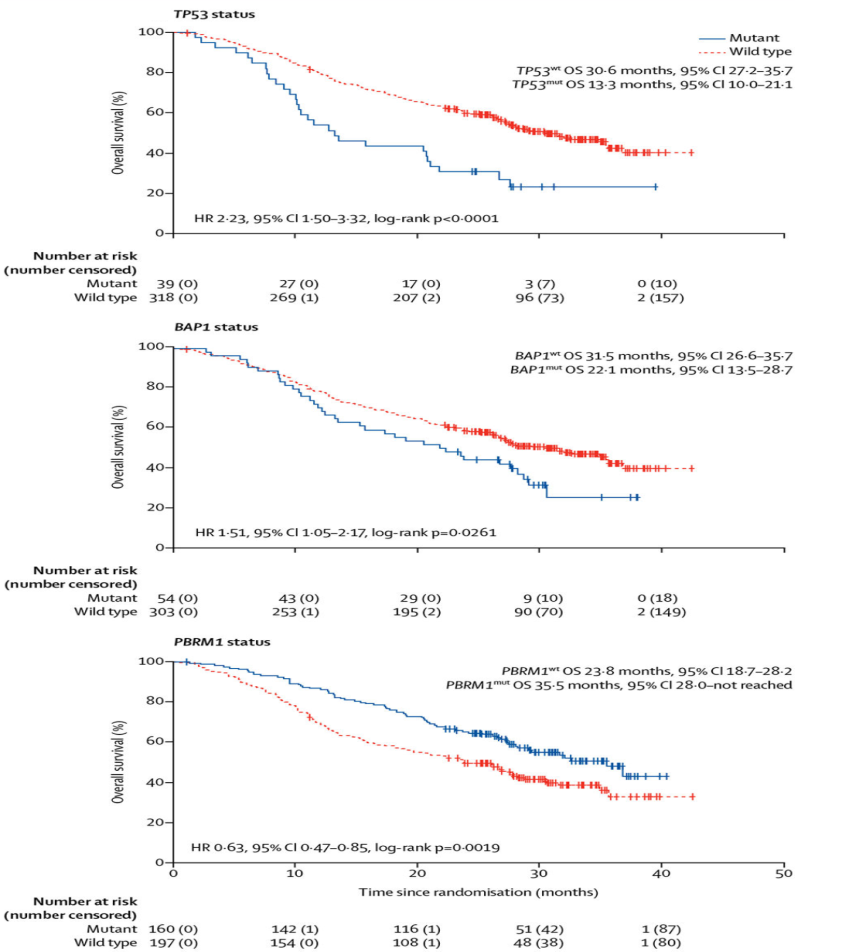
图 1 :不同突变状态的中位总生存[1]

图 2 :不同风险状态和模型划分的总生存率[1]
TP53/BAP1/CDKN2A/TERT/SETD2与ccRCC预后分层
2018年cell reports的一篇文章,对TCGA数据库中488例ccRCC患者进行了综合的分子特征分析,同样分析了高频突变基因与ccRCC预后的关系,验证了TP53或BAP1突变的患者总生存期比较短,另外发现CDKN2A基因的突变也和预后较差有关(图3)[2]。此外19年发表在EU FOCUS的一篇文章对147例ccRCC进行回顾性研究,分析了TERT基因启动子区域突变与预后的关系,研究发现TERT主要的突变类型为启动子突变,在ccRCC的发生频率是12.3%,且TERT基因启动子区域突变的ccRCC患者生存期较短,与预后较差有关(图4)。这篇文章中还对ccRCC的其他高频突变基因进行了预后相关的统计学分析,发现SETD2基因突变的ccRCC患者,复发风险高;而BAP1基因突变的ccRCC患者,生存期更短(图5)[3]。
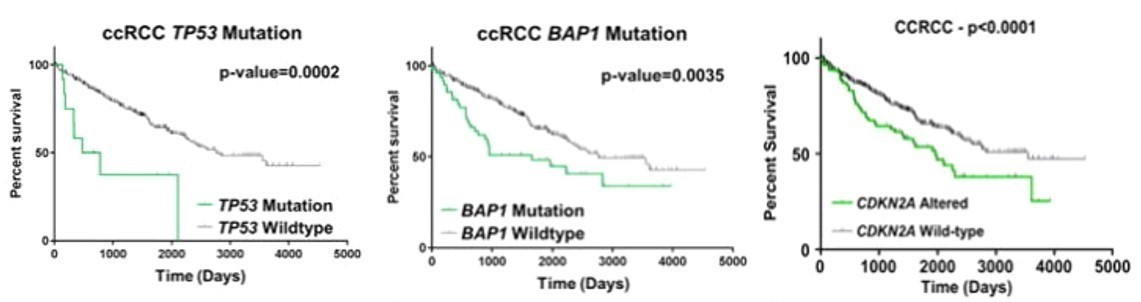
图 3 :不同组织学亚型ccRCC患者总生存期[2]
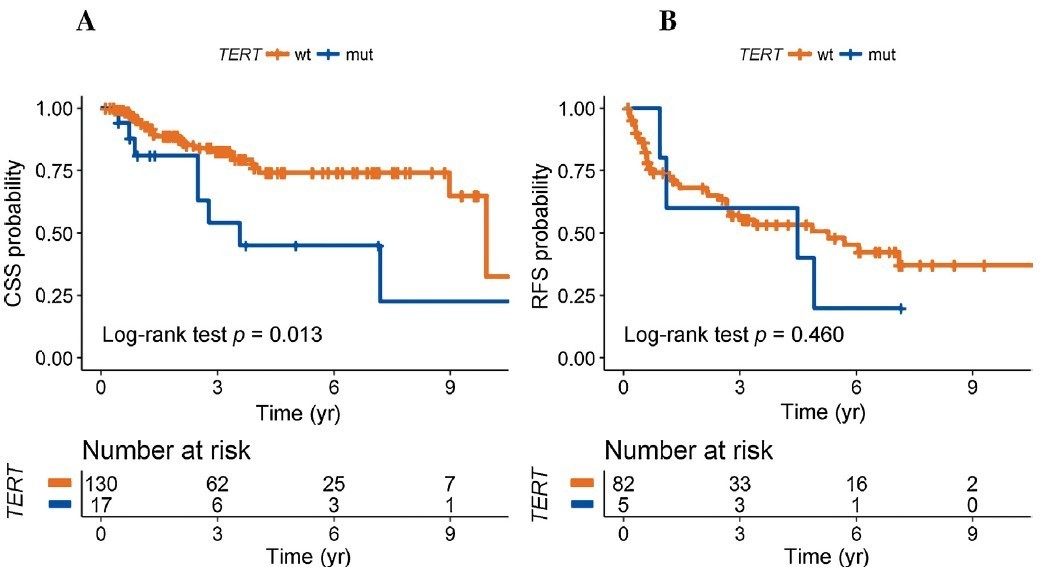
图 4 :透明细胞肾癌患者的(A)肿瘤特异生存率(CSS)和(B)无复发生存率(RFS)的TERT状态[3]
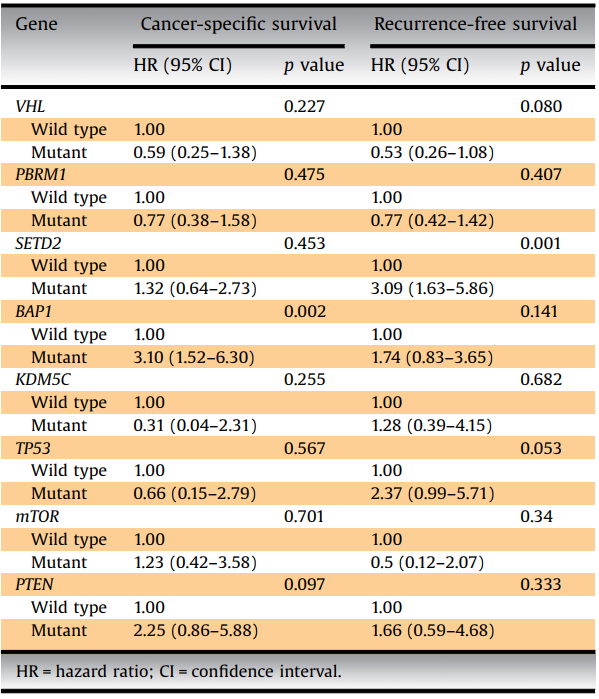
图 5 :单变量Cox回归结果分析突变与肾细胞癌野生型、突变型患者肿瘤特异性和无复发生存率的关系[3]
总结
在肾细胞癌的研究中,组织学基因改变的重要性不可低估。目前数据提示TP53、BAP1、CDKN2A基因发生突变、TERT基因启动子区域突变患者预后较差,SETD2基因突变复发风险高;而PBRM1基因发生突变,提示预后较好。肾癌临床转归及预后还存在一些不确定因素,分子标志物可以作为临床重要参数的有益补充。我们需要积极探索RCC诊断及预后的肿瘤分子标志物,以个体化地评估并预测RCC的恶性生物学行为及患者预后。
参考文献:
-
1. Voss MH, et al. Genomically annotated risk model for advanced renal-cell carcinoma: a retrospective cohort study. Lancet Oncol. 2018 Dec;19(12):1688-1698.
2. Ricketts CJ, et al. The Cancer Genome Atlas Comprehensive Molecular Characterization of Renal Cell Carcinoma. Cell Rep. 2018 Apr 3;23(1):313-326.e5.
3. Casuscelli J, et al. Characterization and Impact of TERT Promoter Region Mutations on Clinical Outcome in Renal Cell Carcinoma. Eur Urol Focus . 2019 Jul;5(4):642-649.
致谢
感谢辉瑞医学部王莹博士和医学信息部在文章撰写过程中提供材料和文献的帮助。

原创作者 董培
中山大学肿瘤防治中心
副主任医师
相关任职 :
中南大学-哈佛大学联合培养博士,硕士生导师;
中国临床肿瘤学会(CSCO)青委委员;广东省抗癌协会泌尿生殖系委员会委员;广东省医师协会泌尿生殖委员会委员;广东省泌尿生殖协会泌尿肿瘤学分会委员
专业方向 :
中山大学肿瘤防治中心泌尿肿瘤MDT核心成员;擅长各种泌尿系肿瘤的综合诊治,肾癌全程管理专家,微创保肾治疗复杂性肾肿瘤,转移性晚期肾癌的个体化综合治疗
本文原创作者为董培医师,已获得作者授权发布。
相关阅读
【RCC前沿· 新时空】肾癌基因检测和个体化精准治疗(一)
【RCC前沿·新时空】关注罕见类型肾癌-来自2020ESMO的一点提示
【RCC前沿·新时空】新型雷达的应用:循环肿瘤细胞在肾癌进展预测中的作用
【RCC前沿·新时空】见微知治——循环肿瘤细胞在肾癌疗效评价中的应用
【RCC前沿·新时空】循环肿瘤细胞指导的肾癌M0(i+)分期研究


