
近年来,乳腺癌相关心脏病防治已成为改善患者长期预后的关键突破点。在乳腺癌治疗所致心脏损伤中,缺血性心脏病(IHD)最为显著——肿瘤微环境介导的全身炎症反应不仅会诱发IHD,还可能进一步提升心肌梗死的发生风险。值得注意的是,这种影响具有双向性,IHD同样会促进肿瘤恶性进展,具体表现为:心肌梗死既会增加乳腺癌发病风险,还会诱导特异性免疫细胞浸润乳腺组织,进而加速肿瘤进展;而部分IHD治疗可能促进乳腺癌转移并使其向更具侵袭性的表型转化。尽管乳腺癌与IHD分属不同系统疾病,但二者的相互作用增加了抗肿瘤治疗和IHD管理的难度,最终导致患者生存率降低。因此,本文旨在系统阐述乳腺癌与IHD的相互作用及其潜在机制,为改善乳腺癌或IHD患者的临床预后提供理论依据[1]。
一. 抗癌与护心的拉锯战
近年来,随着乳腺癌系统治疗的进步,患者预后显著改善,但非乳腺癌相关死亡的比例却逐年上升,其中心血管疾病已成为乳腺癌患者的重要死因。美国SEER数据库分析表明,在老年乳腺癌患者中,心血管疾病死亡率(15.9%,95% 置信区间[CI]:15.6-16.2)已超过乳腺癌本身(15.1%,95% CI:14.8-15.4)。大型队列研究同样证实,随着早期乳腺癌患者生存期延长,心血管疾病已取代乳腺癌成为首要死亡原因。这表明乳腺癌幸存者面临更高的心血管疾病风险,这可能与抗肿瘤治疗密切相关[1]。
在肿瘤相关心血管疾病中,心脏损伤最为常见,临床表现为心力衰竭、心律失常、心肌炎等多种症状。值得注意的是,IHD在乳腺癌幸存者中尤为高发。一项纳入13,348例乳腺癌患者的研究(中位随访8年)显示,986例发生心血管事件的患者中,冠心病占比高达74.6%(736例)。同时,缺血性心脏损伤进展迅速且病情凶险,临床诊治难度大,一旦进展为心肌梗死,往往预后不良,致残率和死亡率居高不下,严重威胁患者长期生存。更值得关注的是,心肌梗死患者的恶性肿瘤发生风险较普通人群增加46%(风险比[HR]=1.46;95% CI:1.21-1.77),提示IHD可能与乳腺癌发病风险存在双向影响[1]。
二. 乳腺癌与IHD的恶性循环
肿瘤与心血管疾病存在诸多共同的危险因素,如肥胖、吸烟、慢性炎症等。然而最新研究揭示了一个值得关注的现象:乳腺癌患者发生心肌缺血(HR=1.8,95% CI:1.0-3.1)和心肌梗死(HR=2.9,95% CI:1.9-4.2)的风险显著高于普通人群。这一发现提示,除共同的危险因素外,乳腺癌本身可能通过独特的病理机制促进IHD的发生,进而增加心肌梗死发生风险。进一步研究发现,肿瘤发生会诱导机体免疫反应,导致肿瘤坏死因子-α(TNF-α)、白细胞介素-1β(IL-1β)、白细胞介素-6(IL-6)等促炎细胞因子大量释放。这些细胞因子不仅直接损伤血管内皮细胞,更因冠状动脉及其分支血管的血供特性而产生显著的病理影响,从而加速乳腺癌患者IHD的进展(图1A)[1]。
同时,IHD也会对乳腺癌的发生发展造成影响,既增加发病风险,又促进疾病进展和复发。最新研究揭示了心肌梗死的促肿瘤机制:心肌梗死后,心脏间质基质细胞会释放含有特定生物分子的细胞外囊泡,这些分子(如骨桥蛋白、IL-6、半乳糖凝集素-3[GAL-3]、TNF-α、血管内皮生长因子[VEGF]等)虽然对心脏具有修复作用,但同时也会促进乳腺癌的进展(图1B)。纽约大学的研究进一步表明,心肌梗死可导致免疫细胞重编程,诱导部分免疫细胞呈现免疫抑制表型,从而引起全身免疫失调,加速乳腺癌的进展和转移。此外,IHD引起的代谢改变同样可能促进肿瘤进展,其主要的无氧糖酵解代谢途径会导致乳酸积累,进而促进肿瘤增殖和转移,最终对预后产生不利影响。临床数据分析显示,在确诊后发生心血管事件(如心肌梗死或卒中)的早期乳腺癌患者中,乳腺癌复发风险增加59%(HR=1.59,95% CI:1.23-2.05),死亡风险增加60%(HR=1.6,95% CI:1.15-2.22)[1]。
这些证据表明,乳腺癌与IHD并非两种独立疾病,而是存在相互作用:乳腺癌可能通过激活全身炎症反应系统来触发和加速IHD;反之,IHD也会促进乳腺癌的发生发展,并显著增加复发风险。
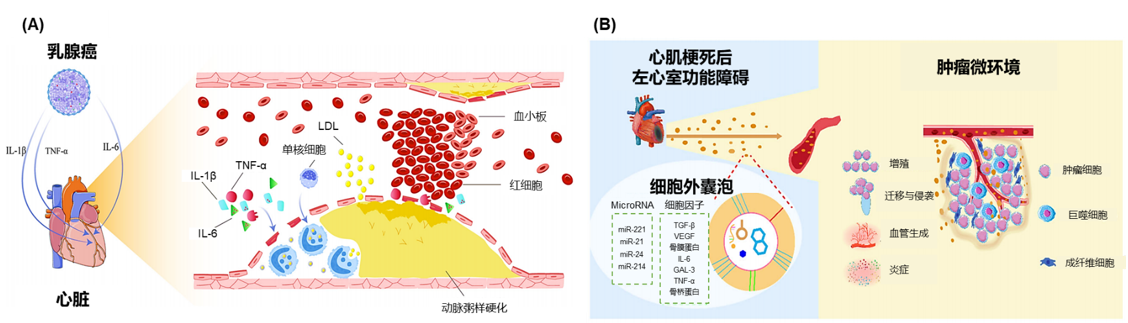
IL-1β,白细胞介素-1β;TNF-α,肿瘤坏死因子-α;IL-6,白细胞介素-6;LDL,低密度脂蛋白;TGF-β,转化生长因子-β;VEGF,血管内皮生长因子;GAL-3,半乳糖凝集素-3;MicroRNA,微小核糖核酸
图1. 乳腺癌与IHD的相互作用机制图[1]
三. 乳腺癌治疗和IHD管理的双向影响
乳腺癌治疗与IHD管理之间的相互作用表现为双向影响:一方面,乳腺癌的化疗、内分泌治疗及放疗等抗肿瘤方案可能通过诱发动脉粥样硬化和血管痉挛导致IHD;另一方面,IHD的常用治疗药物(如他汀类药物、P2Y12抑制剂、尿激酶型纤溶酶原激活物和维生素B3等)也可能促进乳腺癌的疾病恶化和转移扩散(图2,表1)[1]。
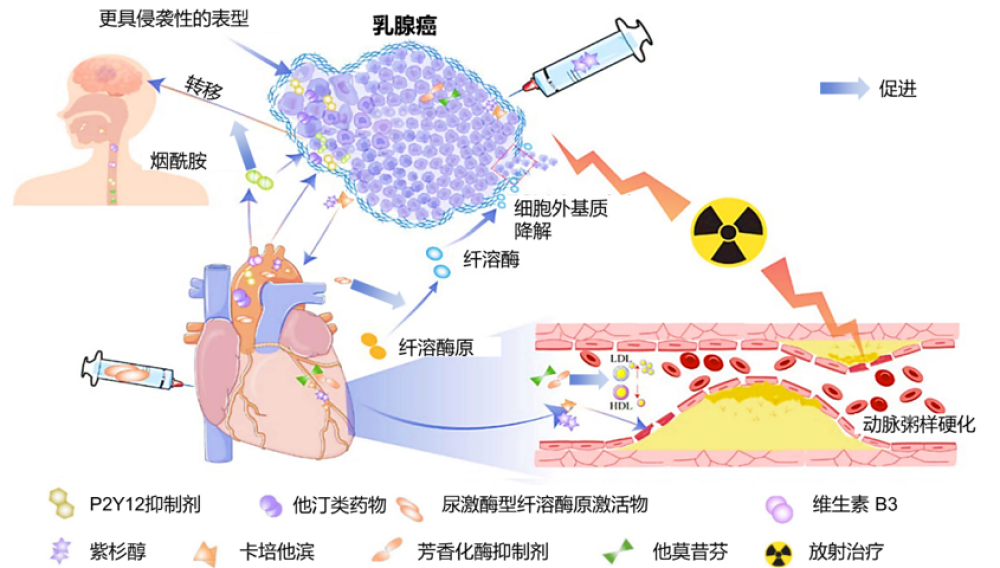
图2. 乳腺癌治疗与IHD管理之间的相互作用机制图[1]
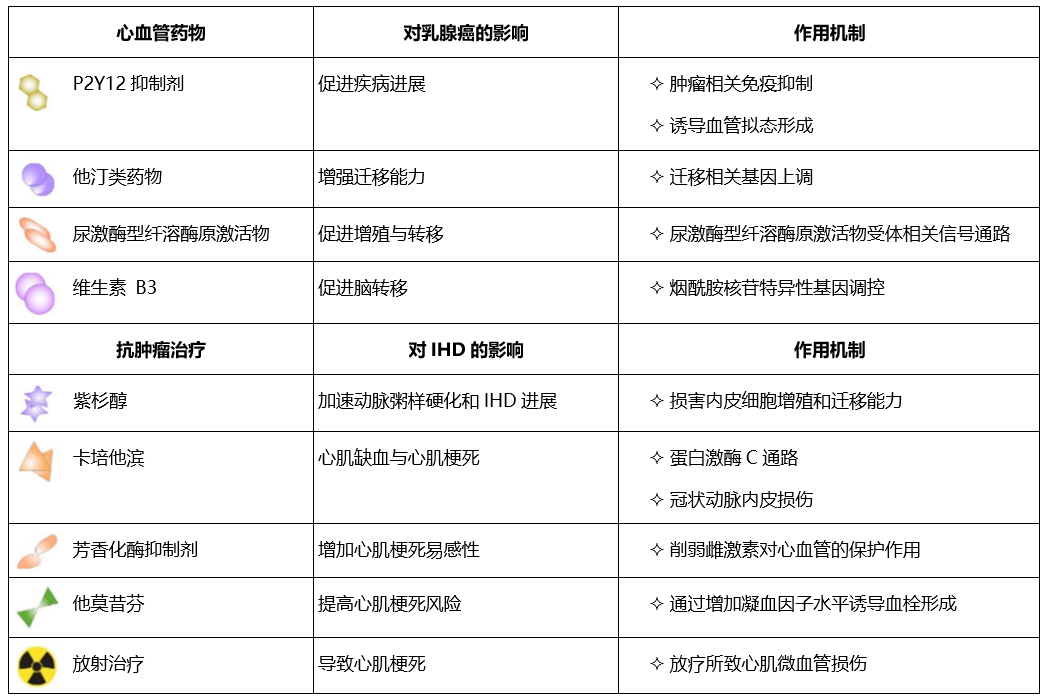
表1. 乳腺癌治疗与IHD管理之间的相互作用[1]
四. 破局策略:多学科协同管理
在乳腺肿瘤心脏病学领域,如何防治肿瘤治疗相关性心血管疾病是一个需要肿瘤科医师和心脏科医师共同关注,即需要多学科交叉研究的新兴领域。为获得最佳临床结局需在癌症治疗方案与心血管病监测策略之间达成平衡[2]。因此,在选择抗肿瘤治疗方案时,应尽可能避免导致IHD的方案。同时,在抗肿瘤治疗过程中,必须密切监测患者的心电图变化及IHD相关症状,通常建议在辅助治疗前通过心电图、超声心动图检查和心脏损伤标志物对心功能进行全面评估,一旦出现IHD症状,应及时采取干预措施[1]。
化疗:化疗药物可能导致长期的心脏不良反应,影响患者的生活质量。因此,对于心功能异常患者,在化疗结束后仍应继续对患者心功能进行随诊随访,高危患者则应提高随诊随访频率。如果患者使用化疗药物期间发生有临床症状的心脏不良反应,或无症状但左室射血分数<45%亦或较基线下降幅度>15%,可考虑检测心肌肌钙蛋白T,必要时应先停药并充分评估患者的心脏功能,后续治疗应慎重[3]。
内分泌治疗:接受内分泌治疗的乳腺癌患者,其血脂受到卵巢功能异常以及内分泌治疗药物的双重影响,容易出现血脂代谢异常,尤其是绝经后的乳腺癌患者,血脂异常的发生率明显升高[2]。一项前瞻性队列研究显示,对于绝经后的激素受体阳性早期乳腺癌患者,与非甾体类芳香化酶抑制剂(AI)药物比较,甾体类AI药物显著降低36%的血脂事件发生风险(P=0.018)。因此,对于血脂异常的绝经后乳腺癌患者,治疗时可选择对血脂影响较小的内分泌治疗药物。同时,当患者血脂管理不理想时,建议与内分泌科或心血管科专家共同制定适当的干预方案,同时对疗效和依从性进行监测[3]。
放疗:放疗相关心脏不良反应的潜伏期较长,早期缺乏明显的临床表现,应在放疗后长时间内随诊心肌酶、心电图、超声心动图等辅助检查,以及时发现心包病变、心肌病、冠状动脉病变、心律失常等。目前尚缺乏放疗相关心脏不良反应的特异性治疗方案。因此,在制定放疗决策时,应尽量降低正常心脏组织的照射体积和照射剂量,并减少放疗相关心脏不良反应的危险因素。对于已经出现放疗相关心脏不良反应的患者,可尝试应用抗炎、抗血栓、营养心肌、他汀类药物和血管紧张素转化酶抑制剂等治疗,其临床应用价值仍需进一步探索[3]。
五. 未来展望
尽管大多数针对乳腺癌和IHD的治疗可能存在相互作用,但部分药物显示出对两种疾病的双重治疗潜力[1]:
钠-葡萄糖协同转运蛋白2(SGLT2)抑制剂主要应用于糖尿病治疗,但最新证据表明其在肿瘤管理和心血管疾病方面均具有获益作用。基础研究显示,SGLT2抑制剂通过阻滞细胞周期和诱导细胞凋亡,对乳腺癌细胞具有显著抗增殖作用。在心血管疾病方面,SGLT2抑制剂可使动脉粥样硬化性心血管疾病患者的死亡风险降低13%(HR=0.87,95% CI:0.78-0.97)。
依维莫司联合AI在激素受体阳性、人表皮生长因子受体-2阴性乳腺癌中显示出良好效果。值得注意的是,依维莫司在心血管领域也有应用,依维莫司洗脱支架通过药物与支架的协同作用,能有效预防支架植入后再狭窄和血栓形成。
β受体阻滞剂作为心血管疾病常用药物,可有效降低心肌梗死复发风险并短期缓解心绞痛。值得注意的是,其还能通过破坏细胞周期进程和周期蛋白稳态水平来抑制乳腺癌细胞增殖。因此,上述药物因其在IHD和BC管理中的双重获益,可能成为极具前景的治疗选择。
总结
乳腺癌与IHD并非完全独立的疾病,两者存在显著的相互影响。一方面,乳腺癌的发生会触发并加速冠状动脉粥样硬化进程,最终导致IHD,增加乳腺癌患者的死亡风险;另一方面,IHD可能促进乳腺癌的发生并加速其进展。然而,目前这些发现主要基于回顾性分析,乳腺癌与IHD相互作用的具体机制尚未完全阐明。因此,需要开展更严谨的临床与基础研究,以进一步揭示乳腺癌与IHD之间的相互作用关系及其分子机制,这将有助于改善乳腺癌患者的长期生存,并降低IHD患者的肿瘤发生风险。
除疾病本身外,乳腺癌与IHD的治疗方案也存在交互影响。大多数乳腺癌治疗手段(如放疗、化疗和内分泌治疗)会促进IHD的发生发展;而IHD的临床管理(如溶栓和抗血小板治疗)也可能加速BC的进展。因此,深入探究抗肿瘤治疗与IHD管理之间的相互作用机制,将有助于优化治疗策略,从而改善BC和/或IHD患者的预后。
参考文献
- Luo Y, Liu J, Qu P, et al. The crosstalk of breast cancer and ischemic heart disease[J]. Cell Death Discov. 2025 Apr 18;11(1):185.
- 沈赞,邵志敏,中华医学会肿瘤学分会肿瘤支持康复治疗学组,中国乳腺癌相关心脏病诊疗共识编写委员会 . 中国乳腺癌相关心脏病诊疗共识(2022年版)[J]. 中国癌症杂志, 2022, 32 (10):1016-1036.
- 国家肿瘤质控中心乳腺癌专家委员会, 北京乳腺病防治学会健康管理专业委员会. 中国乳腺癌随诊随访与健康管理指南(2022版) [J] . 中华肿瘤杂志, 2022, 44(1) : 1-28.



