
这一期的开头我们先复习一下如何确诊胃肠间质瘤(GIST)。(【GIST前沿 ·新时空】如何确诊胃肠间质瘤?)
看过上一期的朋友,一定知道GIST的确诊来源于免疫组化,也就是说,只要是来源于胃肠道间叶组织的肿瘤,如果免疫组化指标CD117和DOG-1检测结果为阳性,即可诊断为GIST。(【GIST前沿·新时空】胃肠间质瘤基因检测的临床意义(一) )
新世纪20年来,GIST的诊治策略发生了翻天覆地的变化,从有别于其他消化道肿瘤到领先于其他消化道肿瘤,目前更成为其他消化道肿瘤诊治领域学习的标杆。这一切的原因并非因为GIST的确诊,而是因为找到了GIST肿瘤产生的“开关”,这就是KIT和PDGFR-α基因。简单来说,85%-90%的GIST存在KIT或PDGFR-α基因的突变(和正常不同),而靶向药物针对这两个基因不同类型的突变(如不同外显子的突变)进行抑制,从而可以使大部分患者取得较好也较为持久的临床疗效。
1. KIT或PDGFR-α的突变和肿瘤形成
让我们先来看下面这张图(图一)。
这张图很形象的描述了KIT或PDGFR-α蛋白的结构、功能、突变和成瘤。首先,KIT和PDGFR-α两个蛋白本身从结构和功能上高度相似,我们只需要明白其中一个即可。以KIT为例,基本分为细胞膜外区,跨膜蛋白区,近细胞膜区(英文缩写JMD,非常重要)、ATP结合区和活化环区。从功能上来说,正常的KIT(蓝色)平时处于非激活状态,以单体的形式存在,而只有在配体(黄色)存在的情况下,两个单体才能聚合形成二聚体,从而激活产生功能,促进细胞的增生和分裂。而发生基因突变的KIT蛋白(红色)则无需配体存在,即可形成二聚体,激活下游信号通路,促使细胞异常增殖,抑制凋亡,这是一种失控状态,细胞将不受控制的生长,最终形成肿瘤。

图一:KIT或PDGFR-α激活突变1
再进一步细化来看,正常的KIT(蓝色)之所以能保持平衡状态而没有不受控制形成GIST,主要在于正常的近膜区(JMD)具有抑制功能,可以抑制活化环区形成活性构象(图二)。近膜区(JMD)的氨基酸由Exon11编码,因此,一旦Exon11发生了突变,这种抑制功能丧失,近膜区(JMD)解除了对激酶域的活化环的抑制。当活化环摆动到开放位置时,ATP就可以接触到ATP结合区,ATP作为磷酸化反应的供体,下游的通路打开,细胞不受控制地增生,GIST继而形成。
当然,KIT或PDGFR-α突变二聚化后产生了一系列下游的变化,这个就复杂了。有兴趣的朋友可看图三,当KIT/PDGFR-α这个开关一旦打开,至少从三个方向导致细胞内一系列的变化。目前已经用于临床上的药物都是针对KIT/PDGFR-α这个总开关的,而针对下游支路的药物也有研发,但相对少且疗效不佳。
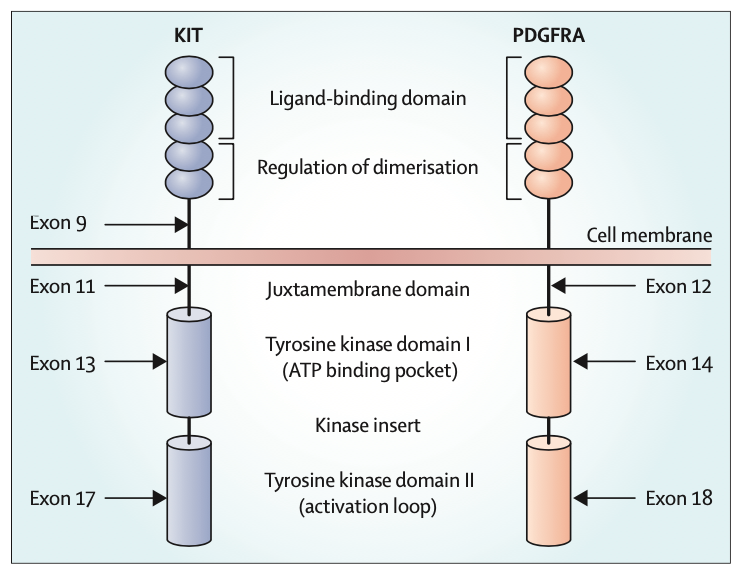
图二:KIT和PDGFR-α的结构2
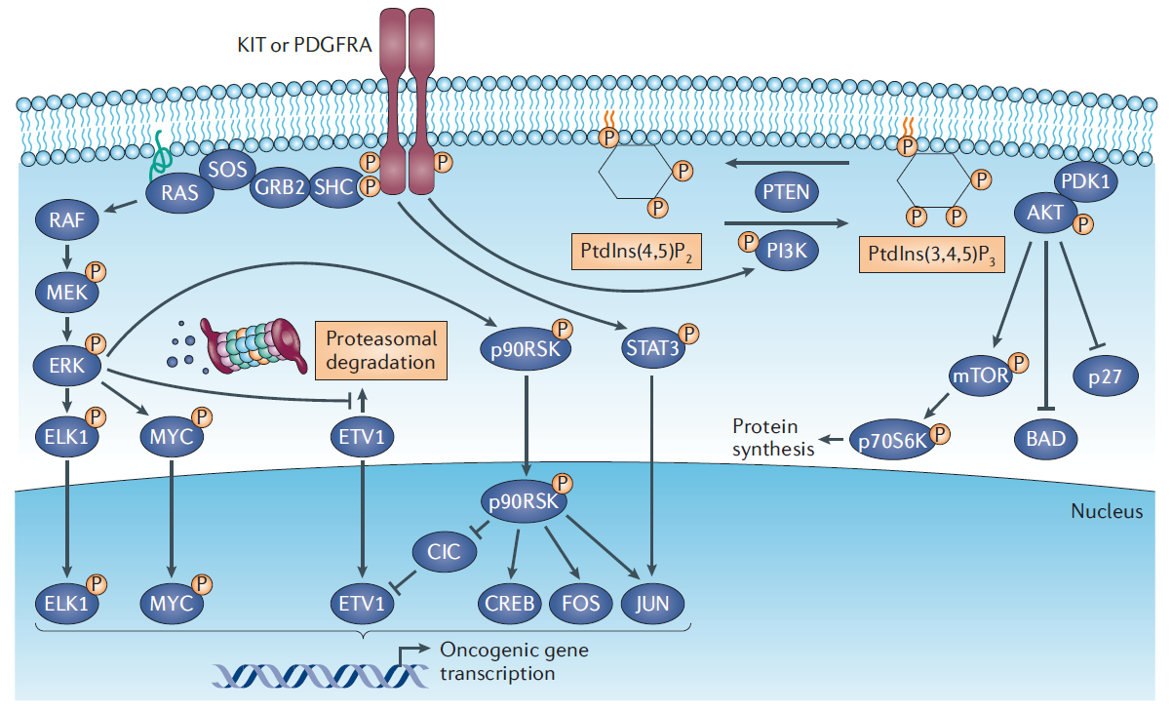
图三:KIT和PDGFR-α突变型GIST中的肿瘤产生的信号通路1
2. 野生型GIST的定义
上一期说过,基因检测有一代测序和二代测序之分。一般情况下,一代测序检测KIT的四个外显子,即Exon9/11/13/17;检测PDGFR-α的两个或三个外显子,即Exon12/(14)/18。我们通常所说的野生型GIST,即这6个或7个外显子的核苷酸序列和正常情况相同,没有检测出突变。
理解了这个概念以后,就有必要和大家探讨一下所谓的“假”野生型GIST。所谓“假”野生型GIST,即一代测序没有检测出上述6个或7个外显子突变,但事实上却存在KIT或PDGFR-α基因的突变,这部分患者的基因检测结果非常可能误导医生给出不适当甚至错误的治疗措施。那么“假”野生型GIST产生的主要原因是什么呢?
以下罗列几种临床上常见的“假”野生型GIST产生的原因。
原因一 : 肿瘤细胞少
基因检测首先需要提取肿瘤细胞内的DNA,而如果各种原因导致肿瘤细胞少,可以提取的DNA自然相应减少,如果超过了测序技术的敏感度,自然没办法测出突变。临床上这种原因导致的“假”野生型并非罕见。那么什么情况下肿瘤细胞会少呢?比如细针穿刺组织活检,本来组织就很少,还要进行常规染色和免疫组化染色,自然很难保证足够量的肿瘤细胞进行DNA的提取。再比如有些经过伊马替尼治疗的患者,肿瘤出现大范围的坏死退缩,比例超过90%到95%,也很难保证足够的肿瘤细胞进行DNA的提取。还有一种情况就是时间太久的组织标本,这些组织虽然肿瘤细胞足够,但长时间存放导致DNA降解而无法检测出正确结果。
原因二:检测技术的瑕疵
上一期在谈“GIST基因检测的临床意义”时,关于一代基因测序和二代基因测序的区别笔者曾提到过,即一代基因测序只检测6个或7个外显子,而且一般也只是检测这6个或7个外显子的热点突变区域。如果一个GIST患者存在Exon11突变,但突变区域并非在热点区域550-570bp之间,那么一代基因测序的结果就会给出“假”野生型GIST的结论。
“假”野生型的完全避免很难做到,但我们还是可以尽可能降低其发生的比例。
邵逸夫医院分子病理中心的做法包括:
- 野生型结果的复核,即需要两次检测结果一致方可以出报告;
- 二代测序技术的应用,进行KIT和PDGFR-α全外显子序列的检测,避免非热点区域突变的遗漏;
- 定期回顾群体的检测数据,如果某一时段野生型GIST比例过高,则需要分析其原因。
目前,经过二代基因测序的69例GIST患者,四重野生型(包括KIT、PDGFR-α、SDH、NF-1、BRAF和K-RAS)的比例已经降到了3%。
我个人推荐所有可获取标本的GIST都进行基因检测,其结果对于后续诊断治疗帮助极大。如果你不信,就别错过我下一期的分析。
参考文献
1. Corless Christopher L,Barnett Christine M,Heinrich Michael C,Gastrointestinal stromal tumours: origin and molecular oncology.[J] .Nat Rev Cancer, 2011, 11: 865-78.
2. Joensuu Heikki,Hohenberger Peter,Corless Christopher L,Gastrointestinal stromal tumour.[J] .Lancet, 2013, 382: 973-83.

原创作者 钱浩然
浙江大学医学院附属邵逸夫医院普外科
主任医师
相关经历 :
中国医师协会外科医师分会胃肠间质瘤专家委员会委员,中国抗癌学会胃肠间质瘤专业委员会委员,CSCO-GIST专家委员会委员,浙江省抗癌学会胃肠道间质瘤协作组秘书
临床专业方向 :
胃癌、大肠癌和胃肠间质瘤的基础和临床研究
本文原创作者为钱浩然医师,已获得作者授权发布。
相关阅读


